Статья дает базовое представление о том, как в современном мире создаются лекарства. Рассмотрены история драг-дизайна, основные понятия, термины и технологии, применяющиеся в этой сфере. Особое внимание уделено роли вычислительной техники в этом наукоемком процессе. Описаны методы поиска и валидации биологических мишеней для лекарственных препаратов, высокопроизводительный скрининг, процессы клинических и доклинических испытаний лекарств а также применение компьютерных алгоритмов.
Драг-дизайн: история
Индустрия направленного конструирования новых лекарственных препаратов, или, как этот процесс называют, калькируя с английского за неимением такого же короткого и удобного русского термина, драг-дизайн (drug - лекарственный препарат, design - проектирование, конструирование) - сравнительно молодая дисциплина, но все же не настолько молодая, как это принято считать .
Рисунок 1. Пауль Эрлих, впервые выдвинувший гипотезу о существовании хеморецепторов и их возможного использования в медицине.
Национальная библиотека медицины США
К концу девятнадцатого века химия достигла значительной степени зрелости. Была открыта таблица Менделеева, разработана теория химической валентности, теория кислот и оснований, теория ароматических соединений. Этот несомненный прогресс дал толчок и медицине. Новые химические продукты - синтетические краски, производные смол, начали использоваться в медицине для дифференциального окрашивания биологических тканей. В 1872–1874 годах в Страсбурге, в лаборатории известного анатома Вильгельма Валдеера, студент-медик Пауль Эрлих (рис. 1), изучавший селективную окраску тканей, впервые выдвинул гипотезу о существовании хеморецепторов - специальных тканевых структур, специфически взаимодействующих с химическими веществами, и постулировал возможность использования этого феномена в терапии различных заболеваний. Позже, в 1905 году, эта концепция была расширена Дж. Лэнгли, предложившим модель рецептора как генератора внутриклеточных биологических импульсов, который активируется агонистами и инактивируется антагонистами.
Этот момент можно считать рождением хемотерапии и новым витком в фармакологии, и в 20-м веке это привело к беспрецедентному успеху в клинической медицине. Одним из самых громких достижений фармакологической промышленности 20-го века можно по праву назвать пенициллин, антибиотик, открытый в 1929 году Александром Флемингом и исследованный впоследствии Чейном и Флори. Пенициллин, обладающий антибактериальным действием, сослужил человечеству незаменимую службу в годы Второй мировой войны, сохранив жизни миллионам раненых.
Пораженные успехом пенициллина, многие фармацевтические компании открыли собственные микробиологические подразделения, возлагая на них надежды по открытию новых антибиотиков и других лекарств. Последовавшие успехи биохимии привели к тому, что стало возможным теоретически предсказывать удачные мишени для терапевтического воздействия, а также модификации химических структур лекарств, дающих новые соединения с новыми свойствами. Так, антибиотик сульфаниламид в результате ряда исследований дал начало целым семействам гипогликемических, диуретических и антигипертензивных препаратов. Драг-дизайн поднялся на качественно новый уровень, когда разработка новых лекарственных соединений стала не просто плодом работы воображения химиков, а результатом научного диалога между биологами и химиками.
Новый прорыв был связан с развитием молекулярной биологии, позволившей привлечь к разработкам информацию о геноме, клонировать гены, кодирующие терапевтически важные биологические мишени и экспрессировать их белковые продукты.
Завершение ознаменовавшего начало нового тысячелетия проекта «геном человека», в результате которого была прочитана полная информация, содержащаяся в ДНК человека, явилось настоящим триумфом раздела биологической науки, получившей название «геномика». Геномика дает совершенно новый подход к поиску новых терапевтически важных мишеней, позволяя искать их непосредственно в нуклеотидном тексте генома.
Геном человека содержит 12000–14000 генов, кодирующих секретируемые белки. На данный момент в фармацевтической промышленности используется не более 500 мишеней. Существуют исследования, говорящие, что многие заболевания являются «мультифакторными», то есть обуславливаются дисфункцией не одного белка или гена, а 5–10 связанных между собой белков и кодирующих их генов. Исходя из этих соображений можно заключить, что количество исследуемых мишеней должно увеличиться минимум в 5 раз.
Биохимическая классификация исследуемых в настоящее время биологических мишеней и их численное соотношение представлены на рисунке 2. Особо следует отметить, что бóльшую (>60%) долю рецепторов составляют мембранные G-белок сопряженные рецепторы (GPCR , G-protein coupled receptors ), а суммарный объем продаж лекарств, направленных на взаимодействие с ними, равняется 65 млрд. долл. ежегодно, и продолжает расти.
Основные понятия

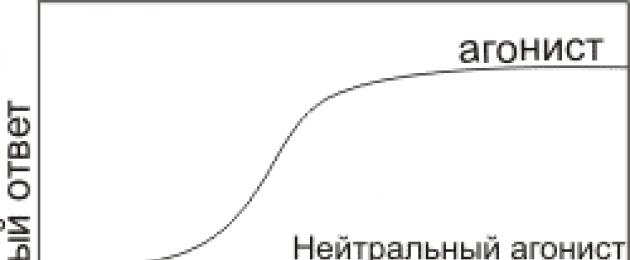
Рисунок 3. Три типа влияния лигандов на клеточный ответ: увеличение ответа (положительный агонгист ), постоянство ответа, но конкурирование за связывании с другими лигандами (нейтральный агонист ) и уменьшение ответа (антагонист ).
Основные понятия, используемые в драг-дизайне - это мишень и лекарство . Мишень - это макромолекулярная биологическая структура, предположительно связанная с определенной функцией, нарушение которой приводит к заболеванию и на которую необходимо совершить определенное воздействие. Наиболее часто встречающиеся мишени - это рецепторы и ферменты. Лекарство - это химическое соединение (как правило, низкомолекулярное), специфически взаимодействующее с мишенью и тем или иным образом модифицирующее клеточный ответ, создаваемый мишенью.
Если в качестве мишени выступает рецептор, то лекарство будет, скорее всего, его лигандом, то есть соединением, специфическим образом взаимодействующим с активным сайтом рецептора. В отсутствие лиганда рецептор характеризуется собственным уровнем клеточного ответа - так называемой базальной активностью.
По типу модификации клеточного ответа лиганды делят на три группы (рис. 3):
- Агонисты увеличивают клеточный ответ.
- Нейтральные агонисты связываются с рецептором, но не изменяют клеточный ответ по сравнению с базальным уровнем.
- Обратные агонисты, или антагонисты понижают клеточный ответ.
Степень взаимодействия лиганда с мишенью измеряют аффинностью, или сродством. Аффинность равна концентрации лиганда, при которой половина мишеней связана с лигандом. Биологической же характеристикой лиганда является его активность, то есть та концентрация лиганда, при которой клеточный ответ равен половине максимального.
Определение и валидация мишени
Один из самых ранних и самых важных этапов драг-дизайна - выбрать правильную мишень, воздействуя на которую можно специфическим образом регулировать одни биохимические процессы, по возможности не затрагивая при этом другие. Однако, как уже было сказано, такое не всегда возможно: далеко не все заболевания являются следствием дисфункции только одного белка или гена.
С наступлением постгеномной эры, определение мишеней происходит с использованием методов сравнительной и функциональной геномики. На основании филогенетического анализа в геноме человека выявляются гены, родственные генам, функции чьих белковых продуктов уже известны, и эти гены могут быть клонированы для дальнейшего исследования.
Однако мишени, чьи функции определены лишь гипотетически, не могут служить отправной точкой для дальнейших исследований. Необходима многоступенчатая экспериментальная валидация, в результате которой может быть понята конкретная биологическая функция мишени применительно к фенотипическим проявлениям исследуемой болезни.
Существует несколько методов экспериментальной валидации мишеней:
- геномные методы заключаются в подавлении синтеза мишени в тестовой системе путем получения мутантов с генным нокаутом (в которых ген мишени попросту отсутствует) или использования РНК-антисмысловых последовательностей, «выключающих» тот или иной ген;
- мишени можно инактивировать с помощью моноклональных антител или облучая мишень, модифицированную хромофором, лазерным излучением;
- мишени можно инактивировать с помощью низкомолекулярных лигандов-ингибиторов;
- также можно непосредственно производить валидацию мишени, устанавливая ее взаимодействие с тем или иным соединением методом плазмонного резонанса.
Уровень валидации мишени повышается с числом модельных животных (специальных генетических линий лабораторных животных), в которых модификация мишени приводит к желаемому фенотипическому проявлению. Высшим уровнем валидации является, несомненно, демонстрация того, что модификация мишени (например, блокирование или нокаут рецептора или ингибирование фермента) приводит к клинически идентифицируемым и воспроизводимым симптомам у человека, однако, понятно, такое можно наблюдать достаточно редко.
Кроме того, при выборе мишени не следует забывать о таком явлении, как полиморфизм - то есть о том, что ген может существовать в разных изоформах у разных популяций или рас людей, что приведет к разному эффекту лекарства на разных больных.
Когда мишень уже найдена и проверена на валидность, начинаются непосредственные исследования, результатом которых являются многочисленные структуры химических соединений, лишь немногим из которых суждено стать лекарствами.
Исследование всех возможных с химической точки зрения лигандов («химическое пространство») невозможно: простая прикидка показывает, что возможно не менее 10 40 различных лигандов, в то время как с момента возникновения вселенной прошло лишь ~10 17 секунд. Поэтому на возможную структуру лигандов накладывается ряд ограничений, который существенно сужает химическое пространство (оставляя его, тем не менее, совершенно необъятным). В частности, для сужения химического пространства накладываются условия подобия лекарству (drug-likeness ), которые в простом случае можно выразить правилом пяти Липинского, согласно которому соединение, чтобы «быть похожим» на лекарство, должно:
- иметь менее пяти атомов-доноров водородной связи;
- обладать молекулярным весом менее 500;
- иметь липофильность (log P - коэффициент распределения вещества на границе раздела вода-октанол) менее 5;
- иметь суммарно не более 10 атомов азота и кислорода (грубая оценка количества акцепторов водородной связи).
В качестве стартового набора лигандов, исследуемых на способность связываться с мишенью, обычно используют так называемые библиотеки соединений, либо поставляемые на коммерческой основе специализирующимися на этом компаниями, либо содержащиеся в арсенале фармацевтической компании, проводящей разработку нового лекарства или заказавшей его у сторонней фирмы. Такие библиотеки содержат тысячи и миллионы соединений. Этого, конечно, совершенно недостаточно для тестирования всех возможных вариантов, но этого, как правило, и не требуется. Задачей на этом этапе исследования является выявление соединений, способных после дальнейшей модификации, оптимизации и тестирования дать «кандидат» - соединение, предназначенное для тестирования на животных (доклинические исследования) и на людях (клинические исследования).
Этот этап осуществляется с помощью высокопроизводительного скрининга (in vitro ) или его компьютерного (in silico ) анализа - высокопроизводительного докинга.
Комбинаторная химия и высокопроизводительный скрининг
Скринингом называется оптимизированная конвейеризованная процедура, в результате которой большое количество химических соединений (>10 000) проверяется на аффинность или активность по отношению к специальной тестовой (имитирующей биологическую) системе. По производительности различают разные виды скрининга:
- низкопроизводительный (10000–50000 образцов);
- среднепроизводительный (50000–100000 образцов);
- высокопроизводительный (100000–5000000+ образцов).
Для скрининга как для «промышленной» процедуры очень критична эффективность, стоимость и время, потраченное на операцию. Как правило, скрининг производится на роботизированных установках, способных работать в круглосуточном и круглогодичном режиме (рис. 4).

Рисунок 4. Аппаратура, используемая для высокопроизводительного скрининга. А - Роботизированная пипетка, в автоматическом высокопроизводительном режиме наносящая образцы тестируемых соединений в плашку с системой для скрининга. Типичное количество углублений на плашке - тысячи. Объем системы в одной лунке - микролитры. Объем вносимого образца - нанолитры. Б - Установка для высокопроизводительного скрининга и считывания флуоресцентного сигнала Mark II Scarina. Работает с плашками, содержащими 2048 углублений (NanoCarrier). Полностью автоматическая (работает в круглосуточном режиме). Производительность - более 100 000 лунок (образцов) в день.
Принцип скрининга достаточно прост: в плашки, содержащие тестовую систему (например, иммобилизованная мишень или специальным образом модифицированные целые клетки), робот раскапывает из пипетки исследуемые вещества (или смесь веществ), следуя заданной программе. Причем на одной плашке могут находиться тысячи «лунок» с тестовой системой, и объем такой лунки может быть очень мал, так же как и объем вносимой пробы (микро- или даже нанолитры).
Потом происходит считывание данных с плашки, говорящее о том, в какой лунке обнаружена биологическая активность, а в какой - нет. В зависимости от используемой технологии детектор может считывать радиоактивный сигнал, флюоресценцию (если система построена с использованием флуоресцентных белков), биолюминесценцию (если используется люциферин-люциферазная система или ее аналоги), поляризацию излучения и многие другие параметры.
Обычно в результате скрининга количество тестируемых соединений сокращается на 3–4 порядка. Соединения, для которых в процессе скрининга выявлена активность выше заданного значения, называются прототипами. Однако следует понимать, что такие «удачи» еще очень и очень далеки от конечного лекарства. Лишь те из них, которые сохраняют свою активность в модельных системах и удовлетворяют целому ряду критериев, дают предшественников лекарств, которые используются для дальнейших исследований.
Как уже было сказано, даже библиотеки, содержащие более миллиона соединений, не в состоянии представить все возможное химическое пространство лигандов. Поэтому при проведении скрининга можно выбрать две различные стратегии: диверсификационный скрининг и сфокусированный скрининг . Различие между ними заключается в составе используемых библиотек соединений: в диверсификационном варианте используют как можно более непохожие друг на друга лиганды с целью охватить как можно большую область химического пространства, при сфокусированном же, наоборот, используют библиотеки родственных соединений, полученных методами комбинаторной химии, что позволяет, зная приблизительную структуру лиганда, выбрать более оптимальный его вариант. Здравый смысл подсказывает, что в масштабном проекте по созданию нового лекарственного препарата следует использовать оба этих подхода последовательно - сначала диверсификационный, с целью определения максимально различных классов удачных соединений, а потом - сфокусированный, с целью оптимизации структуры этих соединений и получения рабочих прототипов.
Если для мишени известно так называемое биологическое пространство, то есть какие-либо характеристики лигандов (размер, гидрофобность и т.д.), которые могут с ней связываться, то при составлении библиотеки тестируемых соединений выбирают лиганды, попадающие в «пересечение» биологического и химического пространств, так как это заведомо повышает эффективность процедуры.
Структуры прототипов, полученные в результате скрининга, далее подвергаются разнообразным оптимизациям, проводимым в современных исследованиях, как правило, в тесном сотрудничестве между различными группами исследователей: молекулярными биологами, фармакологами, моделистами и медицинскими химиками (рис. 5).

Рисунок 5. Фармакологический цикл. Группа молекулярной биологии отвечает за получение мутантных мишеней, группа фармакологии - за измерение данных по активности и аффинности синтезированных лигандов на мишенях дикого типа и мутантных, группа моделирования - за построение моделей мишеней, предсказание их мутаций и предсказание структур лигандов, группа медицинской химии - за синтез лигандов.
С каждым оборотом такого «фармакологического цикла» прототип приближается к предшественнику и затем к кандидату, который уже тестируется непосредственно на животных (доклинические испытания) и на людях - в процессе клинических испытаний.
Таким образом, роль скрининга заключается в существенном сокращении (на несколько порядков) выборки прототипов (рис. 6).

Рисунок 6. Роль высокопроизводительного скрининга в разработке нового лекарственного препарата. Скрининг, будь то его лабораторный (in vitro ) или компьютерный (in silico ) вариант, - главная и наиболее ресурсоемкая процедура по выбору стартовых структур лекарств (прототипов) из библиотек доступных соединений. Выходные данные скрининга часто являются отправной точкой для дальнейшего процесса разработки лекарства.
Клинические исследования
Медицина - это область, в которой ни в коем случае не следует спешить. В особенности, если речь идет о разработке новых лекарственных препаратов. Достаточно вспомнить историю с препаратом Талидамидом, разработанным в конце 50-х в Германии, применение которого беременными женщинами приводило к рождению детей с врожденными пороками конечностей, вплоть до их полного отсутствия. Этот побочный эффект не был вовремя выявлен во время клинических исследований в силу недостаточно тщательного и аккуратного тестирования.
Поэтому в настоящее время процедура тестирования лекарств достаточно сложна, дорога и требует значительного времени (2–7 лет тестирования в клинике и от 100 миллионов долларов на одно соединение-кандидат, см. рис. 7).

Рисунок 7. Процесс разработки нового лекарства занимает от 5 до 16 лет. Затраты на клиническое тестирование одного соединения-кандидата составляют более 100 миллионов долларов США. Суммарная стоимость разработки, с учетом препаратов, не достигших рынка, часто превышает 1 миллиард долларов.
Прежде всего, еще до поступления в клинику, препараты исследуются на токсичность и канцерогенность, причем исследования должны проводиться, кроме систем in vitro , как минимум на двух видах лабораторных животных. Токсичные препараты, само собой, в клинику не попадают, за исключением тех случаев, когда они предназначены для терапии особо тяжелых заболеваний и не имеют пока менее токсичных аналогов.
Кроме того, препараты подвергаются фармакокинетическим исследованиям, то есть тестируются на такие физиологические и биохимические характеристики, как поглощение, распределение, метаболизм и выведение (по-английски обозначается аббревиатурой ADME - Absorption, Distribution, Metabolism and Extraction ). Биодоступность, например, является подхарактеристикой введения препарата в организм, характеризующая степень потери им биологических свойств при введении в организм. Так, инсулин, принимаемый перорально (через рот), имеет низкую биодоступность, так как, будучи белком, расщепляется желудочными ферментами. Поэтому инсулин вводят либо подкожно, либо внутримышечно. По этой же причине часто разрабатывают препараты, действующие аналогично своим природным прототипам, но имеющие небелковую природу.
Юридически процесс клинических исследований новых препаратов имеет очень много нюансов, так как они требуют огромного количества сопроводительной документации (в сумме несколько тысяч страниц), разрешений, сертификаций и т.д. Кроме того, многие формальные процедуры сильно разнятся в разных странах в силу различного законодательства. Поэтому, для решения этих многочисленных вопросов, существуют специальные компании, принимающие от крупных фармацевтических компаний заказ на проведение клинических испытаний и перенаправляющие их в конкретные клиники, сопровождая весь процесс полной документацией и следя, чтобы никакие формальности не были нарушены.
Роль вычислительной техники в драг-дизайне
В настоящее время в драг-дизайне, как и в большинстве других наукоемких областей, продолжает увеличиваться роль вычислительной техники. Следует сразу оговорить, что современный уровень развития компьютерных методик не позволяет разработать новый лекарственный препарат, используя только компьютеры. Основные преимущества, которые дают вычислительные методы в данном случае - это сокращение времени выпуска нового лекарства на рынок и снижение стоимости разработки.
Основные компьютерные методы, используемые в драг-дизайне, это:
- молекулярное моделирование (ММ);
- виртуальный скрининг;
- дизайн новых лекарственных препаратов de novo ;
- оценка свойств «подобия лекарству»;
- моделирование связывания лиганд-мишень.
Методы ММ, основывающиеся на структуре лиганда
В случае, если ничего не известно про трехмерную структуру мишени (что случается достаточно часто), прибегают к методикам создания новых соединений исходя из информации о структуре уже известных лигандов и данных по их активности.
Подход основывается на общепринятой в химии и биологии парадигме, гласящей, что структура определяет свойства. Основываясь на анализе корреляций между структурой известных соединений и их свойствами, можно предсказать структуру нового соединения, обладающего желаемыми свойствами (или же, наоборот, для известной структуры предсказать свойства). Причем, этот подход используется как при модификации известных структур с целью улучшения их свойств, так и при поиске новых соединений используя скрининг библиотек соединений.
Методы определения похожести молекул (или методы отпечатков пальцев) состоят в дискретном учете определенных свойств молекулы, называемых дескрипторами (например, число доноров водородной связи, число бензольных колец, наличие определенного заместителя в определенном положении и т.д.) и сравнивании получившегося «отпечатка» с отпечатком молекулы с известными свойствами (используемой в качестве образца). Степень похожести выражается коэффициентом Танимото, изменяющимся в диапазоне 0–1. Высокая похожесть предполагает близость свойств сравниваемых молекул, и наоборот.
Методы, основывающиеся на известных координатах атомов лиганда, называются методами количественной связи между структурой и активностью (QSAR , Quantitative Structure-Activity Relationship ). Один из наиболее используемых методов этой группы - метод сравнительного анализа молекулярных полей (CoMFA , Comparative Molecular Field Analysis ). Этот метод заключается в приближении трехмерной структуры лиганда набором молекулярных полей, отдельно характеризующих его стерические, электростатические, донорно-акцепторные и другие свойства. CoMFA модель строится на основании множественного регрессионного анализа лигандов с известной активностью и описывает лиганд, который должен хорошо связываться с исследуемой мишенью, в терминах молекулярных полей. Полученный набор полей говорит, в каком месте у лиганда должен быть объемный заместитель, а в каком - маленький, в каком полярный, а в каком - нет, в каком донор водородной связи, а в каком - акцептор, и т.д.
Модель может использоваться в задачах виртуального скрининга библиотек соединений, выступая в данном случае аналогом фармакофора. Самым главным недостатком этого метода является то, что он обладает высокой предсказательной силой лишь на близких классах соединений; при попытке же предсказать активность соединения другой химической природы, чем лиганды, использовавшиеся для построения модели, результат может оказаться недостаточно достоверным.
Схема возможного процесса создания нового лекарства, основывающегося на структуре лиганда, приведена на рисунке 8.

Рисунок 8. Пример молекулярного моделирования, основывающегося на структуре лиганда. Для циклического пептида уротензина II (внизу слева ) определена трехмерная структура методом ЯМР спектроскопии водного раствора (вверху слева ). Пространственное взаиморасположение аминокислотных остатков мотива ТРП-ЛИЗ-ТИР, являющегося важным для биологической функции, было использовано для построения модели фармакофора (вверху справа ). В результате виртуального скрининга найдено новое соединение, демонстрирующее биологическую активность (внизу справа ).
Очевидно, что достоверность моделирования, как и эффективность всего процесса конструирования нового лекарства, можно существенно повысить, если учитывать данные не только о структуре лигандов, но и о структуре белка-мишени. Методы, учитывающие эти данные, носят общее название «драг-дизайн, основывающийся на структурной информации» (SBDD , Structure-Based Drug Design ).
Методы ММ, основывающиеся на структуре белка
В связи с растущим потенциалом структурной биологии, все чаще можно установить экспериментальную трехмерную структуру мишени, или построить ее молекулярную модель, основываясь на гомологии с белком, чья трехмерная структура уже определена.
Наиболее часто используемые методы определения трехмерной структуры биомакромолекул с высоким разрешением (Часто, когда экспериментальная структура мишени все же недоступна, прибегают к моделированию на основании гомологии - методу, для которого показано, что построенная им модель обладает достаточно высоким качеством, если гомология между структурным шаблоном и моделируемым белком не ниже 40%.
Особенно часто к моделированию по гомологии прибегают при разработке лекарств, направленных на G-белок сопряженные рецепторы, так как они, будучи мембранными белками, очень плохо поддаются кристаллизации, а методу ЯМР пока недоступны такие большие белки. Для этого семейства рецепторов известна структура только одного белка - бычьего родопсина, полученная в 2000 г. в Стэнфорде, которая и используется в качестве структурного шаблона в подавляющем числе исследований .
Обычно при исследовании, базирующемся на структурных данных, учитывают также данные по мутагенезу мишени, чтобы установить, какие аминокислотные остатки наиболее важны для функционирования белка и связывания лигандов. Эти сведения особенно ценны при оптимизации построенной модели, которая, будучи лишь производной от структуры белка-шаблона, не может учитывать всей биологической специфики моделируемого объекта.
Трехмерная структура мишени, кроме того, что может объяснить молекулярный механизм взаимодействия лиганда с белком, используется в задачах молекулярного докинга, или компьютерном моделировании взаимодействия лиганда с белком. Докинг использует в качестве стартовой информации трехмерную структуру белка (на данном этапе развития технологии, как правило, конформационно неподвижную), и структуру лиганда, конформационная подвижность и взаиморасположение с рецептором которого моделируется в процессе докинга. Результатом докинга является конформация лиганда, наилучшим образом взаимодействующая с белковым сайтом связывания, с точки зрения оценочной функции докинга, приближающей свободную энергию связывания лиганда. Реально, в силу множества приближений, оценочная функция далеко не всегда коррелирует с соответствующей экспериментальной энергией связывания.
Докинг позволяет сократить затраты средств и времени за счет проведения процедуры, аналогичной высокопроизводительному скринингу, на компьютерных комплексах. Эта процедура называется виртуальным скринингом, и основным ее преимуществом является то, что для реальных фармакологических испытаний нужно приобретать не целую библиотеку, состоящую из миллиона соединений, а только «виртуальные прототипы». Обычно же, с целью избежания ошибок, скрининг и докинг используются одновременно, взаимно дополняя друг друга (рис. 9).

Рисунок 9. Два варианта совместного использования высокопроизводительного скрининга и молекулярного моделирования. Сверху: последовательный итеративный скрининг. На каждом шаге процедуры используется сравнительно небольшой набор лигандов; по результатам скрининга строится модель, объясняющая связь между структурой и активностью. Модель используется для выбора следующего набора лигандов для тестирования. Снизу: «разовый» скрининг. На каждом шаге модель строится по обучающей выборке и используется для предсказаний на тестовой выборке.
С увеличением компьютерных мощностей и появлением более корректных и физичных алгоритмов, докинг будет лучше оценивать энергию связывания белка с лигандом, начнет учитывать подвижность белковых цепей и влияние растворителя. Однако, неизвестно, сможет ли виртуальный скрининг когда-нибудь полностью заменить реальный биохимический эксперимент; если да - то для этого необходим, очевидно, качественно новый уровень алгоритмов, неспособных на сегодняшний день абсолютно корректно описать взаимодействие лиганда с белком.
Одно из явлений, иллюстрирующих несовершенство алгоритмов докинга, - парадокс похожести. Этот парадокс заключается в том, что соединения, структурно совсем немного различающиеся, могут иметь драматически различную активность, и в то же время с точки зрения алгоритмов докинга быть практически неразличимыми.
Прототипы лекарства можно получать не только выбирая из уже подготовленной базы данных соединений. Если есть структура мишени (или хотя бы трехмерная модель фармакофора), возможно построение лигандов de novo, используя общие принципы межмолекулярного взаимодействия. При этом подходе в сайт связывания лиганда помещается один или несколько базовых молекулярных фрагментов, и лиганд последовательно «наращивается» в сайте связывания, подвергаясь оптимизации на каждом шаге алгоритма. Полученные структуры, так же, как и при докинге, оцениваются с помощью эмпирических оценочных функций.
Ограничения применения компьютерных методов
Несмотря на всю свою перспективность, компьютерные методы имеют ряд ограничений, которые необходимо иметь ввиду, чтобы правильно представлять себе возможности этих методов.
Прежде всего, хотя идеология in silico подразумевает проведение полноценных компьютерных экспериментов, то есть экспериментов, результаты которых ценны и достоверны сами по себе, необходима обязательная экспериментальная проверка полученных результатов. То есть, подразумевается тесное сотрудничество научных групп, проводящих компьютерный эксперимент, с другими экспериментальными группами (рис. 5).
Кроме того, компьютерные методы пока не в силах учесть всего разнообразия влияния лекарственного препарата на организм человека, поэтому эти методы не в силах ни упразднить, ни даже существенно сократить клиническое тестирование, занимающее основную долю времени в разработке нового препарата.
Таким образом, на сегодняшний день роль компьютерных методов в драг-дизайне сводится к ускорению и удешевлению исследований, предшествующих клиническим испытаниям.
Перспектива драг-дизайна
Генрих КЛЕХ, директор отдела медицинских исследований и развития Регионального медицинского центра компании "Эли Лилли", профессор Венского университета:
1. Настоящее инновационное лекарство - это принципиально новый препарат, который лечит болезнь по совершенно иному механизму, чем лекарства-предшественники. Именно такие революционные препараты имеют коммерческий успех на современном рынке. За последние годы фармацевтическая медицина сделала большой шаг вперед.
Прежние традиционные препараты, такие, как аспирин, лечили только симптомы болезни, и это была химическая эра фармацевтики. В последние годы гораздо больше внимания исследователи стали уделять влиянию биологических соединений на рецепторы, с помощью чего можно по-настоящему бороться с причиной заболевания. Так сегодня лечат повышенное давление, болезни сердца и желудочно-кишечного тракта. Особенно биопрепараты успешны при лечении рака.
К современной фармацевтике подключилась генетика, изучающая в числе прочего и генные отклонения. По ним фармацевты устанавливают, какова реакция человеческого индивидуума на конкретное лекарство, как классическое, так и новое. Так гораздо конкретнее, чем прежде, разрабатывается схема лечения больного.
2. Существуют достаточно жесткие требования к эффективности нового лекарства, его безопасности. Причем эти требования существенно изменились за последние 20 лет. Прежде для получения лицензии контролирующим органам было достаточно предоставить данные о проведении 2 - 3 тысяч тестов или исследований нового лекарства. Теперь необходимо исследовать препарат на 8 - 10 тысячах людей. Что касается доступности современного препарата, то в принципе она должна быть максимальной. Но постоянный контроль за его приемом со стороны врача тоже необходим, а покупка (согласно сложившейся западной практике) должна осуществляться строго по рецепту.
3. Создание нового лекарства занимает до 14 лет. Это зависит от того, к какому классу относится данный препарат, насколько хорошо известны публике его "предшественники" и т.д. Исследования могут потребовать от 500 миллионов до миллиарда долларов США. Достаточно сказать, что среди исследованных 100 тысяч молекулярных соединений только тысяча может стать основой для нового лекарства. Из них только 100 молекул будут оказывать активное воздействие на организм пациента. Но и среди них 90% оказываются токсичными, так что в широкую продажу попадают только 10 исходных соединений, а коммерческим успехом пользуются только три. Поэтому фармацевтические фирмы, занимающиеся разработкой новых препаратов, вкладывают в исследования от 14 до 20 процентов своей прибыли.
4. Достаточно перспективно сегодня разрабатывать и продвигать продукты фармакогенетики. Во-первых, ими не лечили прежде. Во-вторых, лечение ряда заболеваний во главе с болезнью Альцгеймера традиционными препаратами не давало положительного результата. Кроме того, фармацевтам всего мира нужно форсировать разработку лекарств против рака. Определенные подвижки есть, но люди продолжают страдать от злокачественных заболеваний, а значит нужно продолжать искать от них панацею. Третья область перспективных исследований - это диабет, поскольку пока нет препарата, который бы боролся с первопричиной болезни. Ведь инсулин только гасит ее последствия.
Олег СУПРЯГА, медицинский директор компании "Никомед Россия-СНГ", д.м.н., профессор:
1. Под современным лекарством часто понимают "модное" лекарство, лекарство, созданное с помощью новых технологий. На мой взгляд, современное лекарство - это то, которое предназначено для лечения современных (имеющихся на настоящий момент) болезней. Структура заболеваний, а также доступность тех или иных лекарств в различных экономических и географических регионах мира разная, следовательно, частота применения различных лекарств также разная. Отсюда, определение современного лекарства для каждого региона будет своим.
2. Оно должно отвечать тем критериям качества, безопасности, доступности, которые может позволить себе общество по отношению к своим членам. Как правило, создается национальный (общественный или государственный) орган, которому делегирована функция контроля качества лекарственных средств. Общество с хорошо развитой экономикой и высокими затратами на здравоохранение может осуществлять нетарифное регулирование, ограничивая или закрывая импорт лекарств на свою территорию (рынок) из других менее экономически развитых государств. Тем самым, защищается и своя фармацевтическая промышленность.
3. Разброс затрат на создание нового лекарства составляет от 5 млн долларов США до 1 млрд долларов США и более. В разных странах по-разному, все зависит от тех критериев, которые диктуются обществом или государством, и которые, в свою очередь, определяются уровнем экономического и технологического развития общества, в частности ее фармацевтической промышленности, готовностью общества, государства или отдельных индивидуумов тратить те или иные суммы денег на лекарства, медицину и здравоохранение.
4. Стратегия компании "Никомед" такова, что она передала доклиническую разработку лекарств (Research and Development (R&D) подразделения) другой компании. В настоящее время компания "Никомед" участвует в разработке лекарств, начиная с уровня клинических исследований. Новые перспективные молекулы, успешно преодолевшие стадию доклинических исследований и доведенные до уровня клинических испытаний, лицензируются у специализированных компаний (биотехнологических, научно-исследовательских центров и т.д.).
При этом компания "Никомед" наряду с клиническими испытаниями осуществляет вывод лекарства на рынок (в основном, европейский) и его маркетинговую поддержку и продажи. Перспективными направлениями развития компании "Никомед" остаются кардиология, в т.ч. интервенционная, неврология, эндокринология, педиатрия, ревматология и другие области медицины.
Рустам ИКСАНОВ, директор Центра научных исследований и разработок (ЦНИиР) ОАО «Нижфарм».
1. Сегодня лекарство рассматривается как товар, а значит, оно является элементом рынка, существует по его законам.
2. Прежде всего, современное лекарство должно иметь обоснованную и доказанную безопасность и эффективность. Совершенно справедливо все большее внимание приобретают вопросы качества. За рубежом существуют очень высокие стандарты, распространяющиеся на все этапы разработки нового лекарства, проведения исследований, его производства. Только строгое соблюдение всех норм и правил может обеспечить гарантии соответствия ожидаемых и реальных свойств препарата.
В настоящее время в России также активно внедряются международные стандарты качества. Достаточно серьезным шагом в этом направлении станет, как я надеюсь, внедрение в России в 2005 году стандартов GMP (качественная производственная практика). Сегодня всего лишь несколько компаний в той или иной степени соответствует таким стандартам.
Немаловажным является вопрос доступности лекарств, который не может решаться без вмешательства государства в эту сферу. Пациенты должны иметь гарантию эффективного и безопасного лечения.
3. Новые лекарства проходят долгий путь, прежде чем займут место на аптечной полке. Необходимо не просто разработать лекарственное средство, нужно провести исследования на животных, клинические исследования, получить государственную регистрацию лекарственного средства. Разработка принципиально нового лекарственного средства за рубежом занимает около 10 лет и стоит порядка полумиллиона долларов. К сожалению, не обладая такими средствами, сегодня Россия практически не занимается разработкой принципиально новых лекарственных средств.
Вместе с тем стоит отметить, что научный потенциал для такой работы в России имеется. Хочется надеяться, что он получит необходимое развитие. В основном, российские компании занимаются разработкой воспроизведенных лекарственных средств, так называемых дженериков. Это требует меньших затрат.
4. Без анализа лекарственного рынка, без отслеживания современных тенденций развития стандартов лечения невозможно правильно оценивать перспективы развития фармакологии. Например, наша компания активно использует самые разные маркетинговые исследования, консультации ведущих специалистов для определения своих перспективных направлений.
Трудно найти человека, который в какой-то период жизни не принимал бы лекарство. И в то же время вряд ли многие задумываются над тем, что в лекарстве, как в фокусе линзы, сосредоточиваются достижения фундаментальных наук – органической и неорганической химии, физиологии, биохимии, биофизики, несомненно, фармакологии и комплекса фармацевтических наук. Достижения этих фундаментальных дисциплин благодаря науке о лекарственных веществах входят в практику и служат на благо человека. Поэтому введение в фармакологию, которому и посвящена статья, не только имеет познавательное значение, но и помогает более целенаправленно изучать биологические и химические дисциплины в школе.
Путь лекарства от лаборатории до больного
Создание лекарства начинается обычно в лаборатории химика –специалиста по органическому синтезу или в лаборатории фитохимика. Первый создает пока еще не исследованные соединения, второй выделяет из растений либо индивидуальные химические соединения, либо группу близких по структуре веществ. Затем созданные или выделенные вещества передаются фармакологу, определяющему, обладают ли эти вещества нужным эффектом. Предположим, что фармаколог ищет вещества, обладающие гипотензивным эффектом, т.е. понижающие артериальное давление. Он может идти двумя путями . Первый путь носит название скрининг . При этом фармакологу часто неизвестно даже предположительно, какой химической структурой должно обладать гипотензивное средство, и он испытывает в опытах на животных одно вещество за другим, отсеивая неэффективные (скрининг-сито). Это весьма трудоемкий метод и часто малоэффективный, однако иногда единственно возможный, особенно когда речь идет о разработке новых, неизвестных, групп лекарственных веществ. Скрининг используется для поиска противоопухолевых средств. Впервые он был применен в начале столетия П.Эрлихом для получения противосифилитических средств на основе органических соединений мышьяка.
Чаще используется метод направленного синтеза . Исследователь постепенно накапливает материал, показывающий, какие химические радикалы или иные структуры ответственны за тот или иной вид действия. Одна из основных проблем фармакологии – изучение закономерностей «структура–действие». Все больше накапливается данных, на основании которых составляются программы для компьютеров. Уже с большей долей вероятности можно предсказать характер действия планируемого к синтезу и последующему изучению соединения. Всегда решающим остается эксперимент, но знание общих закономерностей «структура–действие» сокращает путь к успеху.
Итак, предположим, что найдено эффективное средство, способное вызывать гипотензивный эффект, но на этом работа фармаколога не заканчивается. Он должен выяснить, не обладает ли химическое соединение токсическими свойствами, способными проявиться при применении его в качестве лекарственного средства. Фармаколог определяет обычно острую токсичность, т.е. дозу, способную вызвать смерть 50% экспериментальных животных (ЛД 50 – летальная доза); чем меньше эта доза, тем токсичнее вещество. Лекарством может стать только то вещество, терапевтическая (лечебная) доза которого значительно (часто в 20 и более раз) меньше ЛД 50 . Диапазон доз от минимальной эффективной до минимальной токсической свидетельствует о широте терапевтического действия лекарств.
Фармаколог определяет и возможность побочных эффектов при длительном введении лекарства в терапевтических дозах. Проводится определение субхронической токсичности: препарат вводят длительное время – часто до 6 месяцев и более. При этом определяют функции всех систем организма, биохимические показатели крови, проводят патогистологическое исследование органов подопытных животных после окончания введения препарата. Это исследование позволяет судить, не нарушает ли лекарственный препарат функции органов и тканей организма при длительном введении, т.е. безопасна ли длительная терапия этим соединением. Фармаколог определяет и другие возможные токсические эффекты препарата: его влияние на репродуктивную функцию (способность производить потомство), эмбриотоксическое действие (возможность влиять на эмбрион), тератогенное действие (способность вызывать уродства плода), мутагенный эффект. При помощи специальных проб изучают влияние препарата на иммунитет, возможность канцерогенного действия препарата, его аллергенную активность и др.
Одновременно работают и специалисты-провизоры, определяющие наиболее рациональную лекарственную форму. На этом заканчивается этап доклинического исследования препарата. В каждой стране есть официальное учреждение, разрешающее клиническое исследование препарата и последующее использование его в качестве лекарственного средства. В России разрешение на клиническое исследование препарата дает Фармакологический комитет Министерства здравоохранения РФ.
Перед клиницистом, получившим на апробацию лекарственный препарат, стоят те же задачи, что и перед фармакологом, т.е. оценка лечебного эффекта препарата и выяснение возможности побочного действия при его применении. Однако у клинициста возникают трудности, с которыми не сталкивается фармаколог-экспериментатор: сознание человека, принимающего лекарство, может изменить оценку действия лекарства. При некоторых заболеваниях возможно улучшение состояния больного под влиянием внушения и авторитета врача, а также больничного режима, диеты, оказывающих положительное влияние. Поэтому необходимо различать истинный эффект лекарства от влияния сопутствующих лечению факторов. Для этого применяют пробу плацебо (пустышка). Предположим, что одной группе больных, разумеется, не требующих экстренного эффективного лечения, назначают таблетки, содержащие лекарство, а другой группе – аналогичные по виду таблетки, но не содержащие лекарства, – плацебо. Если при этом в результате лечения состояние здоровья улучшится примерно у 60% больных первой группы, а во второй группе – у 30% больных, то налицо значительное превышение действия препарата над плацебо. Следовательно, препарат эффективен. Если же эффект препарата равен плацебо, то следует признать неэффективность препарата. Разработкой препарата занимается сравнительно молодая дисциплина – клиническая фармакология . Если в результате клинических испытаний показано, что препарат эффективен, то врач еще должен оценить возможность побочного действия – нежелательного действия лекарственных веществ. Если, например, врач применяет лекарственное средство для снижения артериального давления и одновременно наблюдает у больного расстройство кишечника при лечении гипотензивным средством, то это и есть пример побочного действия. Степень и выраженность побочного действия бывают такими, что заставляют отказаться от испытания препарата, и тогда дальнейшая разработка препарата прекращается. Однако мало выраженное побочное действие, не несущее непосредственной угрозы здоровью больного, не служит причиной отказа от препарата. Известно, что мочегонные средства, такие как фуросемид, дихлотиазид, снижают концентрацию калия в крови, т.е. вызывают гипокалиемию. Однако такое нарушение коррегируется назначением диеты, богатой этими ионами, либо назначением препаратов калия или других так называемых калийсберегающих диуретиков. Коррекция позволяет успешно лечить больных с сердечно-сосудистыми заболеваниями диуретиками, не беспокоясь о развитии гипокалиемии.
Если клинические испытания прошли успешно, препарат получает разрешение на промышленное производство и применение и поступает в аптечную сеть. Отзывы о нем публикуются в печати, продолжается изучение механизма его действия, и, наконец, препарат занимает должное место в арсенале лекарственных средств. Сложен и долог путь нового лекарства от первого этапа исследования до больного. Чаще всего проходит несколько лет, прежде чем препарат разрешают применять в практике. Из многих тысяч исследованных соединений только некоторые внедряются в практику и получают название лекарственный препарат , хотя, конечно, есть и другие примеры.
Проблемы фармакокинетики
Фармакокинетика – раздел фармакологии, изучающий поведение лекарственных препаратов в организме: их всасывание, распределение, выведение и биотрансформацию . Чтобы лекарственный препарат оказал действие, он должен быть введен в организм. Все пути введения разделяются на две группы: энтеральные и парэнтеральные (от греч. энтерон – желудочно-кишечный тракт). К энтеральным путям введения относится введение через рот (в том числе под язык), в 12-перстную и прямую кишку. К парэнтеральным путям введения, минующим желудочно-кишечный тракт, относится подкожное, внутримышечное, внутривенное введение лекарственных препаратов. Путь введения во многом определяет скорость поступления и выраженность эффекта лекарства.
После введения в организм лекарственное вещество разносится кровью по органам, тканям и жидким средам, но это не значит, что концентрация введенного препарата в каждом органе или ткани одинакова. Равномерному распределению лекарства мешают тканевые барьеры, через которые лекарственные вещества проникают далеко не одинаково. Одним из таких барьеров является гематоэнцефалический: проникновение веществ в центральную нервную систему из крови ограничено, так как ионизированные или нерастворимые в липидах вещества не проникают в мозг через этот барьер. Например, вещества, содержащие четвертичный атом азота, плохо проникают через этот барьер, к таким веществам может быть отнесено биологически активное соединение ацетилхолин. Биологическое значение такого барьера очевидно: проникновение некоторых веществ в мозг из крови существенно нарушило бы его функцию. Поэтому не только биологически активные, но и многие лекарственные вещества (миорелаксанты, ганглиоблокаторы) не проникают через гематоэнцефалический барьер.
Значительно более проницаемым барьером является стенка капилляров, через которую в ткани проникают большинство лекарственных веществ, но не проходят вещества с высоким молекулярным весом, например белок альбумин, имеющий молекулярную массу около 70 000. Эта особенность используется в практике: например, группа веществ высокого молекулярного веса (полиглюкины) применяется в качества кровезаменителей, так как циркулирует в кровяном русле, не проникая в ткани. Плацентарный барьер, отделяющий организм матери от плода, также легко проницаем для лекарств. Поэтому лекарства, вводимые в организм матери, могут оказывать действие и на плод, что необходимо учитывать при проведении терапии беременным женщинам.
Лекарственные вещества, особенно хорошо растворимые в воде, выводятся из организма почками. Летучие вещества выделяются легкими, частично соединения могут выводиться с каловыми массами, а также потовыми железами. Выделение лекарств – одна из причин того, что концентрация препарата в крови падает и эффективность его действия уменьшается.
Кроме того, лекарства подвергаются процессам биотрансформации. Большинство лекарственных веществ растворимы в липидах и представляют собой слабые органические кислоты или основания, которые сравнительно плохо выводятся из организма. Например, после фильтрации в почечных клубочках они реабсорбируются путем диффузии через мембраны и межклеточные соединения клеток канальцев почек. Для быстрого выведения лекарственные вещества должны быть трансформированы в более полярные формы. Поэтому, если в процессе биотрансформации в организме образуются более полярные метаболиты, ионизированные при физиологическом значении pH, менее связанные с белками плазмы, тканевыми белками, они менее способны проникать через мембраны почечного канальца. Поэтому они не подвергаются реабсорбции в почечных канальцах и выделяются с мочой. Этому и служат процессы биотрансформации в организме, которые способствуют выведению лекарства и делают его менее активным.
Химические реакции, участвующие в биотрансформации, разделяются на реакции синтеза (конъюгации) и несинтетические реакции. К первым относятся реакции присоединения к лекарственным веществам продуктов обмена. Известны реакции ацетилирования, т.е. присоединения остатков уксусной кислоты, глюкуроновой и серной кислоты. В реакциях синтеза участвуют и сульфгидрильные группы, связывающие многие органические и неорганические соединения, в частности тяжелые металлы. К неспецифическим реакциям относятся реакции окисления, восстановления и гидролиза.
Ферментные системы, участвующие в биотрансформации, локализованы в печени и эндоплазматическом ретикулуме печеночных клеток. Выделенные в эксперименте, они получили название микросомальные ферменты , поскольку связаны с фракцией микросом, выделяющихся при дифференциальном центрифугировании фрагментов печеночных клеток. Микросомальные ферменты катализируют реакции конъюгации и реакции окисления, в то время как реакции восстановления и гидролиза часто катализируются немикросомальными ферментами.
Активность микросомальных ферментов различна у разных людей и генетически детерминирована, т.е. зависит от генетических особенностей организма. Считают, что величина биотрансформации у отдельных людей может различаться в 6 раз и более, что и определяет индивидуальную чувствительность к препарату. Так, у одних больных необходимый эффект можно достичь дозами, в несколько раз большими, чем у других, и наоборот. Некоторые лекарственные препараты усиливают активность микросомальных ферментов, их называют индукторами , другие – ингибиторы – подавляют их.
Примером значения активности микросомальных ферментов в терапии может служить препарат противотуберкулезного ряда – изониазид. У некоторых больных высока активность микросомальных ферментов, их называют быстрыми инактиваторами изониазида , у других больных эта активность низка, их называют медленными инактиваторами . После шестидневного введения препарата у больных с низкой активностью концентрация изониазида в крови в 2,5 раза выше, чем у первых. У медленных инактиваторов приходится снижать дозу, чтобы не получить нежелательных побочных действий препарата .
Разумеется, «биотрансформируют» лекарства не только печень, но и другие ткани. В результате биотрансформации лекарственные вещества превращаются в метаболиты, которые, как правило, менее активны, чем основное вещество, лучше растворимы и сравнительно легко выводятся из организма почками. Таким образом организм освобождается от введенного лекарства.
Фармакокинетика предусматривает определение скорости инактивации и выделения, оба процесса определяются термином квота элиминации . Она определяет процент вещества от введенной дозы, который метаболизируется и выводится в течение суток. Если этот процент мал, то лекарство при последующих приемах может накапливаться в организме и увеличивать свой эффект. Врач может умело использовать этот феномен, выбирая дозу препарата, которая насыщает организм, затем переходя на меньшую дозу, которая восполняет потерю препарата и носит название поддерживающая доза . Некоторые вещества, например гликозиды наперстянки, применяются именно таким образом.
Продолжение следует
Процесс начинается с получения нового химического состава. Субстанции с комплексной структурой могут быть получены из различных источников, таких как растения (сердечные гликозиды), ткани животных (гепарин), микробные культуры (пенициллин), человеческие клетки (урокиназа), средствами генной инженерии (человеческий инсулин). Человек все глубже проникает в структурно-функциональные взаимосвязи, поиск новых агентов становится более сфокусированным.
Преклиническое тестирование
Преклиническое тестирование собирает информацию о биологических эффектах новых субстанций. Начальный скрининг проводится в биохимико-фармакологических исследованиях или экспериментах на клеточных культурах, изолированных клетках и изолированных органах. Так как эти модели не способны полностью воспроизвести весь комплекс биологических процессов в интактном организме, любое потенциальное лекарство должно быть тестировано на животных. Только опыты на животных могут ответить на вопрос. появляются ли желательные эффекты в нетоксичных или малотоксичных дозах.
Исследование токсичности призвано оценить:
- токсичность при кратковременном и длительном применении,
- возможность генетических повреждений (генотоксичность, мутагенность),
- возможность развития опухолей (онко- и канцерогенность),
- возможность рождения больного плода (тератогенность).
На животных исследуемые соединения испытываются также на поглощение, распределение, метаболизм, и выделение (фармакокинетика). Даже на уровне преклинических исследований отсеивается подавляющее большинство потенциальных лекарственных соединений и остаются только отдельные из них.
Клиническое тестирование
Фаза I
В этой фазе проводится исследование новых препаратов на здоровых лицах с целью определить, наблюдаются ли у человека эффекты, обнаруженные в тестах на животных, выявить взаимоотношения между дозой и эффектом.
Фаза II
Потенциальный новый препарат апробируется на избранных пациентах для определения терапевтической эффективности при заболевании, для которого он предназначен. Положительное действие должно быть явным, а нежелательные эффекты приемлемо малы.
Фаза III
В этой фазе к исследованию привлекаются большие группы пациентов с помощью которых исследуемое лекарство сравнивается со стандартным лечением по исходам терапии.
Как форма испытаний на людях, такие клинические испытания являются субъектом рассмотрения и одобрения этическими комитетами в соответствии с Хельсинской, Токийской и Венецианской декларациями. В процессе клинических испытаний многие новые лекарства лекарства признаются негодными к применению. В конечном итоге, остается только одно лекарство из примерно 10000 вновь полученных субстанций.
Решение одобрить новое препарат принимает национальный регулирующий орган (в России – Фармкомитет МЗ РФ). Заявители (фармацевтические компании) представляют в регулирующий орган полный комплект документации преклинических и клинических испытаний в которых полученные данные об эффективности и безопасности удовлетворяют установленным требованиям и предполагаемую форму выпуска продукта (таблетки, капсулы и т.д.)
После получения одобрения новое лекарство может продаваться под торговой маркой и, таким образом. становится доступным для назначения врачами и продажи в аптеках.
Параллельно идет разработка технологического процесса производства лекарственного средства, требований к качеству, методов анализа.
Процесс разработки лекарств и подготовки к производству лекарственных средств обычно продолжается 5 – 8 лет.
Фаза IV
По мере распространения препарата за ним продолжается наблюдение. Окончательное суждение о соотношении польза-риск нового лекарства может быть сделано только на основании долговременного опыта его применения. Таким образом, определяется терапевтическая ценность нового лекарственного препарата.
Наше мнение
Путь нового лекарства от исследовательской лаборатории до аптечного прилавка долог и требует вложения колоссальных средств. Вот почему глупо говорить о тотальном импортозамещении в фарминдустрии. Если, конечно, речь не идет о незаконном и полузаконном копировании чужих разработок или бесконечном производстве устаревших препаратов.
Как создают лекарства?
XIX век - начало XX века
Пути создания лекарств |
|
Выделение экстрактов из лекарственных растений | Поиск лечебных свойств у неорганических веществ |
Проверка |
|
На животных - на токсичность | На людях - на наличие лечебных свойств |
В аптеках множество токсичных и малоэффективных лекарств, многие средства действуют за счет эффекта плацебо. Удачные находки единичны. |
|
То, что ивовая кора может унимать жар и боль, знали еще знахари. Но официально европейские врачи ее не применяли. Они ввозили из-за границы хинин, которым и лечили лихорадку.
Так было до тех пор, пока в историю болеутоляющих и жаропонижающих средств не вмешалась политика.
Наполеон установил для Англии экономическую блокаду и закрыл материк для английских торговых судов. Из-за этого хинин перестал поступать и вспомнили об иве. И довольно быстро из нее получили салициловую кислоту.
Но увы… Эта кислота в чистом виде имела неприятный вкус, вызывала тошноту, рвоту и была причиной сильных болей в желудке.
Многие эскулапы пытались улучшить переносимость салициловой кислоты, сохранив при этом ее отменные свойства. Но удалось это лишь немецкому химику Феликсу Хоффману.
Его отец страдал мучительными болями от хронического ревматизма и почти не мог двигаться. Желая облегчить страдания отца, Хоффман-младший начал работать над улучшением салициловой кислоты.
Он обрабатывал природное вещество разными известными на тот момент способами. Ацетилсалициловая кислота оказалась самой удачной модификацией. Выпущенная затем под названием «аспирин», она стала одним из самых знаменитых медикаментов на свете. Любопытно, что механизм действия аспирина обнаружили лишь после 100 лет его применения.
Середина XX века
Пути создания лекарств |
||
Поиск лечебных свойств у неорганических и органических веществ | ||
Проверка |
||
На животных - На токсичность и наличие лечебных свойств, моделирование человеческих заболеваний у представителей фауны | На людях - На наличие лечебных свойств | На колонияхмикроорганизмов - Для выявления антимикробных свойств |
Появление антибиотиков и инсулина. В аптеках все больше эффективных лекарств, но побочные действия многих средств еще очень велики. Химическая модификация сотен и тысяч соединений приводит к открытию сульфаниламидов, мочегонных, сахароснижающих и первых гипотензивных средств. В практику входят витамины. |
||
Самые известные лекарства, дошедшие до нас
Его открыл канадский хирург Фред Бантинг. Он изучал на животных свойства экстрактов из поджелудочной железы. Каково же было его удивление, когда после введения такой вытяжки выжила собака, умиравшая от сахарного диабета. Ученый предположил, что какое-то вещество из поджелудочной железы снижает уровень сахара в крови. И через некоторое время проверил свое открытие на друге-медике, который страдал сахарным диабетом.
Новый препарат вызвал у больного друга прилив энергии и бодрости.
А анализы показали уменьшение содержания сахара в крови. С тех пор инсулин - главное средство борьбы с тяжелым сахарным диабетом.
Пенициллин
Антибиотик пенициллин был открыт в 1929 году английским микробиологом Александром Флемингом. Однажды, изучая свойства стафилококков, он забыл на лабораторном столе чашку с культурой бактерий.
Возвратившись, ученый обнаружил в чашке плесень. К его удивлению, она подавила рост микробов. Исследователя озарила догадка: плесень выделяет вещество, убивающее бактерии.
Это вещество он назвал «в честь» плесневого гриба пенициллиума, с которым работал. Испытания на животных показали, что пенициллин действительно эффективно убивает микробов. А при введении в кровь не приносит организму вреда.
Первое успешное применение пенициллина произошло в Америке. Лекарство спасло жизнь молодой женщины, матери троих детей. Температура выше 40 °С держалась у нее 11 дней, и она медленно погибала. Но чудо-лекарство привело ее в сознание уже на второй день применения. Женщина выжила и дожила до глубокой старости.
С тех пор пенициллин спас миллионы людей во всем мире. И продолжает использоваться до сих пор.
Конец ХХ века - ХХI век
Пути создания лекарств |
|||
Выделение, химическая модификация экстрактов из лекарственных растений и вытяжек из организма животных | Широкое применение компьютерного моделирования | Целенаправленный поиск соединений с лечебными свойствами, исходя из знаний биохимии, физиологии и генетики | Широкомасштабный синтез органических соединений и поиск у них лечебных свойств |
Пути проверки |
|||
На животных - на лечебные свойства, токсичность, способность вызывать мутации, уродства плода и рак | На людях - на наличие лечебных свойств. Изучение всасывания, превращений и путей выведения лекарств | На колониях микроорганизмов - для выявления антимикробных свойств | На компьютере - На соответствие молекулы лекарства-мишени в организме |
Появление тысяч эффективных и относительно безопасных лекарств. |
|||