В.Г. Кукес, Д.А. Сычёв, Г.В. Раменская, И.В. Игнатьев
Человек ежедневно подвергается воздействию множества инородных химических веществ, называемых «ксенобиотики». Ксенобиотики попадают в организм человека через лёгкие, кожу и из пищеварительного тракта в составе примесей воздуха, пищи, напитков, ЛС. Некоторые ксенобиотики не оказывают никакого воздействия на организм человека. Однако большинство ксенобиотиков могут вызывать биологические ответные реакции. Организм реагирует на ЛС так же, как и на любой другой ксенобиотик. При этом ЛС становятся объектами различных механизмов воздействия со стороны организма. Это, как правило, приводит к нейтрализации и элиминации (выведению) ЛС. Некоторые, легко растворимые в воде, ЛС элиминируются почками в неизменённом виде, другие вещества предварительно подвергаются воздействию ферментов, изменяющих их химическое строение. Таким образом, биотрансформация - общее понятие, включающее все химические изменения, происходящие с ЛС в организме. Результат биологической трансформации ЛС: с одной стороны - снижается растворимость веществ в жирах (липофильность) и повышается их растворимость в воде (гидрофильность), а с другой стороны - изменяется фармакологическая активность препарата.
Снижение липофильности и повышение гидрофильности лекарственных средств
Небольшое число ЛС способно выводиться почками в неизменён- ном виде. Чаще всего эти препараты представляют «малые молекулы» или они способны находиться в ионизированном состоянии при физиологических значениях рН. Большинство ЛС не обладают такими физико-химическими свойствами. Фармакологически активные органические молекулы чаще липофильны и остаются неионизированными при физиологических значениях рН. Эти ЛС обычно связаны с белками плазмы, плохо фильтруются в почечных клубочках и одновременно легко реабсорбируются в почечных канальцах. Биотрансформация (или система биотрансформации) направлена на повышение растворимости молекулы ЛС (повышение гидрофильности), что способствует выведению его из организма с мочой. Иными словами, липофильные ЛС превращаются в гидрофильные и, следовательно, в более легковыводимые соединения.
Изменение фармакологической активности лекарственных средств
Направления изменения фармакологической активности ЛС в результате биотрансформации.
Фармакологически активное вещество превращается в фармакологически неактивное (это характерно для большинства ЛС).
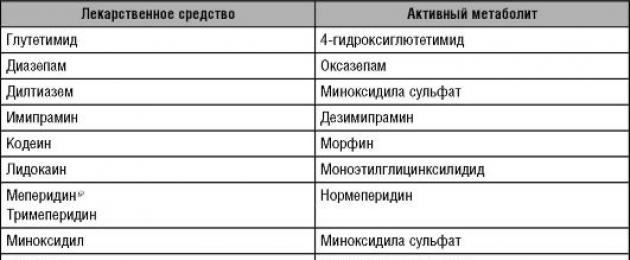
Фармакологически активное вещество на первом этапе превращается в другое фармакологически активное вещество (табл. 5-1).
Неактивное фармакологическое ЛС превращается в организме в фармакологически активное вещество; такие препараты называют «пролекарства» (табл. 5-2).
Таблица 5-1. Лекарственные средства, метаболиты которых сохраняют фармакологическую активность
Окончание таблицы 5-1
 Таблица 5-2.
Пролекарства
Таблица 5-2.
Пролекарства
 Окончание таблицы 5-2
Окончание таблицы 5-2
 * Фенацетин снят с производства из-за выраженных побочных эффектов, в частности, нефротоксичности («фенацетиновый нефрит»).
* Фенацетин снят с производства из-за выраженных побочных эффектов, в частности, нефротоксичности («фенацетиновый нефрит»).
Следует отметить, что эффективность и безопасность применения ЛС (перечислены в табл. 5-1), имеющих активные метаболиты, зависят не только от фармакокинетики собственно ЛС, но и от фармакокинетики их активных метаболитов.
5.1. ПРОЛЕКАРСТВА
Одна из целей создания пролекарств - улучшение фармакокинетических свойств; это ускоряет и увеличивает всасывание веществ. Так, были разработаны сложные эфиры ампициллина (пивампицин p , талампицин p и бикампицин p), в отличие от ампициллина практически полностью всасывающиеся при приёме внутрь (98-99%). В печени эти препараты под действием карбоксиэстераз гидролизуются до ампициллина, обладающего антибактериальной активностью.
Биологическая доступность противовирусного ЛС валацикловира составляет 54%, в печени он превращается в ацикловир. Следует отметить, что биодоступность собственно ацикловира не превышает 20%. Высокая биодоступность валацикловира обусловлена наличием в его молекуле остатка аминокислоты валина. Именно поэтому валацикловир всасывается в кишечнике путём активного транспорта с помощью транспортёра олигопептидов PEPT 1.
Ещё один пример: ингибиторы аденозинпревращающего фермента, содержащие карбоксильную группу (эналаприл, периндоприл, трандолаприл, хвинаприл, спираприл, рамиприл и др.). Так, эналаприл всасывается при приёме внутрь на 60%, гидролизуется в печени под влиянием карбоксиэстераз до активного эналаприлата. Необходимо отметить: эналаприлат при введении внутрь всасывается лишь на 10%.
Другая цель разработки пролекарств - повышение безопасности лекарственных веществ. Например, учёные создали сулиндак p - НПВС. Данный препарат изначально не блокирует синтез простагландинов. Лишь в печени сулиндак p гидролизуется с образованием активного сульфида сулиндака p (именно это вещество обладает противовоспалительной активностью). Предполагали, что сулиндак p не будет обладать ульцерогенным действием. Однако ульцерогенность НПВС обусловлена не местным, а «системным» действием, поэтому, как показали исследования, частота возникновения эрозивно-язвенных поражений органов пищеварения при приёме сулиндака p и других НПВС примерно одинакова.
Ещё одна цель создания пролекарств - повышение избирательности действия ЛС; это увеличивает эффективность и безопасность препаратов. Дофамин используют для усиления почечного кровотока при острой почечной недостаточности, однако препарат влияет на миокард и сосуды. Отмечают повышение АД, развитие тахикардии и аритмий. Присоединение к дофамину остатка глутаминовой кислоты позволило создать новый препарат - глутамил-дофа p . Глутамил-дофа p гидролизуется до дофамина только в почках под влиянием глутамилтранспептидазы и декарбоксилазы L-ароматических аминокислот и таким образом практически не оказывает нежелательного действия на центральную гемодинамику.
 Рис. 5-1.
Фазы биотрансформации лекарственных средств (Katzung В., 1998)
Рис. 5-1.
Фазы биотрансформации лекарственных средств (Katzung В., 1998)
5.2. ФАЗЫ БИОТРАНСФОРМАЦИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Процессы биотрансформации большинства ЛС происходят в печени. Однако биотрансформация ЛС может протекать и в других органах, например, в пищеварительном тракте, лёгких, почках.
В целом, все реакции биотрансформации ЛС можно отнести к одной из двух категорий, обозначаемых как фаза биотрансформации I и фаза биотрансформации II.
Реакции I фазы (несинтетические реакции)
В процессе несинтетических реакций ЛС переходят в более полярные и лучше растворимые в воде (гидрофильные) соединения, чем исходное вещество. Изменения исходных физико-химических свойств ЛС обусловлены присоединением или освобождением активных функциональных групп: например, гидроксильных (-ОН), сульфгидрильных (-SH), аминогрупп (-NH 2). Основные реакции I фазы - реакции окисления. Гидроксилирование - наиболее распространённая реакция окисления - присоединение гидроксильного радикала (-ОН). Таким образом, можно считать, что в I фазу биотрансформации происходит «взлом» молекулы ЛС (табл. 5-3). Катализаторы указанных реакций - ферменты, называемые «оксидазы со смешанной функцией». В целом, субстратная специфичность этих ферментов очень низка, поэтому они окисляют различные лекарственные вещества. К другим, менее частым реакциям I фазы, относят процессы восстановления и гидролиза.
Реакции II фазы (синтетические реакции)
Реакции II фазы биотрансформации, или синтетические реакции, представляют соединение (конъюгацию) ЛС и/или его метаболитов с эндогенными веществами, в результате образуются полярные, хорошо растворимые в воде конъюгаты, легко выводимые почками или с желчью. Для вступления в реакцию II фазы молекула должна обладать химически активным радикалом (группировкой), к которому может присоединиться конъюгирующая молекула. Если активные радикалы присутствуют в молекуле ЛС изначально, тогда реакция конъюгации протекает, минуя реакции I фазы. Иногда молекула лекарственного вещества приобретает активные радикалы в ходе реакций I фазы (табл. 5-4).
Таблица 5-3. Реакции I фазы (Katzung 1998; с дополнениями)
 Таблица 5-4.
Реакции II фазы (Katzung 1998; с дополнениями)
Таблица 5-4.
Реакции II фазы (Katzung 1998; с дополнениями)
 Следует
отметить, что препарат в процессе биотрансформации может превращаться
только за счёт реакций I фазы, либо - исключительно за счёт реакций II
фазы. Иногда часть ЛС метаболизируется путём реакций I фазы, а часть -
путём реакций II фазы. Кроме того, существует возможность
последовательного прохождения реакций I и II фазы (рис. 5-2).
Следует
отметить, что препарат в процессе биотрансформации может превращаться
только за счёт реакций I фазы, либо - исключительно за счёт реакций II
фазы. Иногда часть ЛС метаболизируется путём реакций I фазы, а часть -
путём реакций II фазы. Кроме того, существует возможность
последовательного прохождения реакций I и II фазы (рис. 5-2).
 Рис. 5-2.
Функционирование системы оксидаз со смешанной функцией
Рис. 5-2.
Функционирование системы оксидаз со смешанной функцией
Эффект первого прохождения через печень
Биотрансформация большинства ЛС осуществляется в печени. ЛС, метаболизм которых протекает в печени, подразделяют на две подгруппы: вещества с высоким печёночным клиренсом и вещества с низким печёночным клиренсом.
Для ЛС с высоким печёночным клиренсом характерна высокая степень извлечения (экстракции) из крови, что обусловлено значительной активностью (ёмкостью) метаболизирующих их ферментных систем (табл. 5-5). Поскольку такие ЛС быстро и легко метаболизируются в печени, клиренс их зависит от величины и скорости печёночного кровотока.
ЛС с низким печёночным клиренсом. Печёночный клиренс зависит не от скорости печёночного кровотока, а от активности ферментов и степени связывания ЛС с белками крови.
Таблица 5-5. Лекарственные средства с высоким печёночным клиренсом
 При
одинаковой ёмкости ферментных систем лекарственные вещества, в
значительной степени связанные с белками (дифенин, хинидин, толбутамид),
будут иметь низкий клиренс, по сравнению со слабосвязанными с белками
ЛС (теофиллин, парацетамол). Ёмкость ферментных систем - не постоянная
величина. Например, уменьшение ёмкости ферментных систем регистрируют
при увеличении дозы ЛС (вследствие насыщения ферментов); это может
привести к увеличению биологической доступности ЛС.
При
одинаковой ёмкости ферментных систем лекарственные вещества, в
значительной степени связанные с белками (дифенин, хинидин, толбутамид),
будут иметь низкий клиренс, по сравнению со слабосвязанными с белками
ЛС (теофиллин, парацетамол). Ёмкость ферментных систем - не постоянная
величина. Например, уменьшение ёмкости ферментных систем регистрируют
при увеличении дозы ЛС (вследствие насыщения ферментов); это может
привести к увеличению биологической доступности ЛС.
При приёме внутрь ЛС с высоким печёночным клиренсом, они всасываются в тонкой кишке и через систему воротной вены поступают в печень, где подвергаются активному метаболизму (на 50-80%) ещё до поступления в системное кровообращение. Этот процесс известен как пресистемная элиминация, или эффект «первого прохождения» («first-pass effect»). В результате такие ЛС имеют низкую биологическую доступность при приёме внутрь, при этом абсорбция их может составлять почти 100%. Эффект первого прохождения характерен для таких препаратов, как аминазин, ацетилсалициловая кислота, вера-
памил, гидралазин, изопреналин, имипрамин, кортизон, лабетолол, лидокаин, морфин. Метопролол, метилтестостерон, метоклопрамид, нортриптилин p , окспренолол p , органические нитраты, пропранолол, резерпин, салициламид, морацизин (этмозин) и некоторые другие препараты также подвергаются пресистемной элиминации. Следует отметить, что незначительная биотрансформация ЛС может проходить и в других органах (просвете и стенке кишечника, лёгких, плазме крови, почках и других органах).
Как показали исследования последних лет, эффект первого прохождения через печень зависит не только от процессов биотрансформации ЛС, но и от функционирования транспортёров ЛС, и, прежде всего, гликопротеина-Р и транспортёров органических анионов и катионов (см. «Роль транспортёров лекарственных средств в фармакокинетических процессах»).
5.3. ФЕРМЕНТЫ I ФАЗЫ БИОТРАНСФОРМАЦИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Микросомальная система
Многие ферменты, метаболизирующие ЛС, располагаются на мембранах эндоплазматического ретикулума (ЭПР) печени и других тканей. При изоляции мембран ЭПР путём гомогенизации и фракционирования клетки, мембраны преобразуются в везикулы, называемые «микросомы». Микросомы сохраняют большинство морфологических и функциональных характеристик интактных мембран ЭПР, включая свойство шероховатости или гладкости поверхности, соответственно шероховатого (рибосомального) и гладкого (нерибосомального) ЭПР. В то время как шероховатые микросомы в основном связаны с синтезом белка, гладкие - относительно богаты ферментами, ответственными за окислительный метаболизм лекарственных веществ. В частности, гладкие микросомы содержат ферменты, известные как оксидазы со смешанной функцией, или монооксигеназы. Активность этих ферментов требует присутствия как восстанавливающего агента - никотинамидадениндинуклеотидфосфата (НАДФ-Н), так и молекулярного кислорода. При типичной реакции расходуется (восстанавливается) одна молекула кислорода на одну молекулу субстрата, при этом один кислородный атом включается в продукт реакции, а другой образует молекулу воды.
В этом окислительно-восстановительном процессе ключевую роль играют два микросомальных фермента.
Флавопротеин НАДФ-Н-цитохром Р-450-редуктаза. Один моль этого фермента содержит по одному молю флавинмононуклеотида и флавинадениндинуклеотида. Поскольку цитохром С может служить акцептором электрона, то указанный фермент часто называют НАДФ-цитохром С-редуктазой.
Гемопротеин, или цитохром Р-450 выполняет функцию конечной оксидазы. В действительности микросомальная мембрана содержит множество форм данного гемопротеина, и эта множественность возрастает при повторном введении ксенобиотиков. Относительное изобилие цитохрома Р-450, по сравнению с редуктазой печени, делает процесс восстановления гема цитохрома Р-450 лимитирующей стадией в процессе окисления лекарственных веществ в печени.
Процесс микросомального окисления ЛС требует участия цитохрома Р-450, цитохрома Р-450-редуктазы, НАДФ-Н и молекулярного кислорода. Упрощённая схема окислительного цикла представлена на рисунке (рис. 5-3). Окисленный (Fe3+) цитохром Р-450 соединяется с лекарственным субстратом с образованием бинарного комплекса. НАДФ-Н - донор электрона для флавопротеинредуктазы, которая, в свою очередь, восстанавливает окисленный комплекс цитохром Р-450-лекарство. Второй электрон переходит от НАДФ-Н через ту же флавопротеинредуктазу, восстанавливающую молекулярный кислород и формирующую комплекс «активированный кислород»-цитохром Р-450-субстрат. Этот комплекс переносит «активированный кислород» на лекарственный субстрат с образованием окисленного продукта.
Цитохром Р-450
Цитохром Р-450, в литературе часто обозначаемый CYP, представляет группу ферментов, осуществляющих не только метаболизм ЛС и других ксенобиотиков, но и участвующих в синтезе глюкокортикоидных гормонов, желчных кислот, простаноидов (тромбоксана А2, простациклина I2), холестерина. Впервые цитохром Р-450 идентифицировали Klingenberg и Garfincell в микросомах печени крысы в 1958 году. Филогенетические исследования показали, что цитохромы Р-450 появились в живых организмах около 3,5 млрд лет назад. Цитохром Р-450 - гемопротеин: он содержит гем. Название цитохрома Р-450 связано с особыми свойствами этого гемопротеина. В восстановлен-
ной форме цитохром Р-450 связывает монооксид углерода с образованием комплекса с максимальным поглощением света при длине волны 450 нм. Это свойство объясняют тем, что в геме цитохрома Р-450 железо связано не только с атомами азота четырёх лигандов (при этом образуя порфириновое кольцо). Существуют также пятый и шестой лиганды (сверху и снизу кольца гема) - атом азота гистидина и атом серы цистеина, входящие в состав полипептидной цепи белковой части цитохрома Р-450. Наибольшее количество цитохрома Р-450 располагается в гепатоцитах. Однако цитохром Р-450 обнаруживают и в других органах: в кишечнике, почках, лёгких, надпочечниках, головном мозге, коже, плаценте и миокарде. Важнейшее свойство цитохрома Р-450 - способность метаболизировать практически все известные химические соединения. Наиболее важная реакция - гидроксилирование. Как уже указывалось, цитохромы Р-450 ещё называют монооксигеназами, так как они включают один атом кислорода в субстрат, окисляя его, а один - в воду, в отличие от диоксигеназ, которые включают оба атома кислорода в субстрат.
Цитохром Р-450 имеет множество изоформ - изоферментов. В настоящее время выделено более 1000 изоферментов цитохрома Р-450. Изоферменты цитохрома Р-450, по классификации Nebert (1987), принято разделять по близости (гомологии) нуклеотид/амино- кислотной последовательности на семейства. В свою очередь, семейства подразделяют на подсемейства. Изоферменты цитохрома Р-450 с идентичностью аминокислотного состава более 40% объединены в семейства (выделено 36 семейств, 12 из них обнаружены у млекопитающих). Изоферменты цитохрома Р-450 с идентичностью аминокислотного состава более 55% объединены в подсемейства (выделено 39 подсемейств). Семейства цитохромов Р-450 принято обозначать римскими цифрами, подсемейства - римскими цифрами и латинской буквой.
Схема обозначения отдельных изоферментов.
Первый символ (вначале) - арабская цифра, обозначающая семейство.
Второй символ - латинская буква, обозначающая подсемейство.
В конце (третий символ) указывают арабскую цифру, соответствующую изоферменту.
Например, изофермент цитохрома Р-450, обозначенный как CYP3A4, принадлежит к семейству 3, подсемейству IIIA. Изоферменты цитохрома Р-450 - представители различных семействи подсемейств-
различаются регуляторами активности (ингибиторы и индукторы) и субстратной специфичностью 1 . Например, CYP2C9 метаболизирует исключительно S-варфарин, в то время как R-варфарин метаболизируют изоферменты CYP1A2 и CYP3A4.
Однако члены отдельных семейств, подсемейств и отдельные изоферменты цитохрома Р-450 могут обладать перекрёстной субстратной специфичностью, а также иметь перекрёстные ингибиторы и индукторы. Например, ритонавир (противовирусный препарат) метаболизируют принадлежащие к различным семействам и подсемействам 7 изоферментов (CYP1A2, CYP2A6, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A4). Циметидин одновременно ингибирует 4 изофермента: CYP1A2, СYP2C9, CYP2D6 и CYP3A4. В метаболизме ЛС принимают участие изоферменты цитохрома Р-450 I, II и III семейств. CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2D6, CYP2C9, CYP209, CYP2E1, CYP3A4 - наиболее важные для метаболизма лекарственных веществ и хорошо изученные изоферменты цитохрома Р-450. Содержание различных изоферментов цитохрома Р-450 в печени человека, а также их вклад в окисление ЛС различны (табл. 5-6). Лекарственные вещества - субстраты, ингибиторы и индукторы изоферментов цитохрома Р-450 представлены в приложении 1.
Таблица 5-6. Содержание изоферментов цитохрома Р-450 в печени человека и их вклад в окисление лекарственных средств (Lewis и соавт., 1999)
 1 Некоторые изоферменты цитохрома Р-450 обладают не только субстратной специфичностью, но и стереоспецифичностью.
1 Некоторые изоферменты цитохрома Р-450 обладают не только субстратной специфичностью, но и стереоспецифичностью.
До сих пор не известны эндогенные субстраты для изоферментов семейства CYPI. Эти изоферменты метаболизируют ксенобиотики: некоторые ЛС и ПАУ - основные компоненты табачного дыма и продукты сжигания органического топлива. Отличительная особенность изоферментов семейства СYPI - их способность к индукции под действием ПАУ, в том числе, диоксина и 2,3,7,8-тетрахлорди- бензо-р-диоксина (TCDD). Поэтому семейство СYPI в литературе называют «цитохром, индуцибельный ПАУ»; «диоксин-индуцибельный цитохром» или «ТСDD-индуцибельный цитохром». В организме человека семейство СYPI представлено двумя подсемействами: IА и IB. В состав подсемейства IA входят изоферменты 1А1 и 1А2. В состав подсемейства IB входит изофермент 1В1.
Изофермент 1А1 цитохрома Р-450 (CYP1A1) обнаруживают в основном в лёгких, в меньшей степени - в лимфоцитах и плаценте. CYP1A1 не участвует в метаболизме ЛС, однако в лёгких этот изофермент активно метаболизирует ПАУ. При этом некоторые ПАУ, например, бензопирен и нитрозамины превращаются в канцерогенные соединения, способные спровоцировать развитие злокачественных новообразований, в первую очередь - рака лёгких. Этот процесс получил название «биологическая активация канцерогенов». Как и другие цитохромы семейства CYPI, CYP1A1 индуцируется ПАУ. При этом изучен механизм индукции CYP1A1 под влиянием ПАУ. Проникнув в клетку, ПАУ соединяются с Аh-рецептором (белок из класса регуляторов транскрипции); образовавшийся комплекс ПАУ-Ап-рецептор проникает в ядро при помощи другого белка - ARNT, а затем стимулирует экспрессию гена CYP1A1, связываясь со специфическим диоксин-чувствительным участком (сайтом) гена. Таким образом, у курящих людей процессы индукции CYP1A1 протекают наиболее интенсивно; это приводит к биологической активации канцерогенов. Именно этим объясняют высокий риск возникновения рака легких у курильщиков.
Изофермент 1А2 цитохрома Р-450 (CYP1A2) обнаруживают в основном в печени. В отличие от цитохрома CYP1A1, CYP1A2 метаболизирует не только ПАУ, но и ряд ЛС (теофиллин, кофеин и другие препараты). В качестве маркёрных субстратов для фенотипирования CYP1A2 используют фенацетин, кофеин и антипирин. При этом фенацетин подвергают О-деметилированию, кофеин - 3-деметилированию, а антипирин - 4-гидроксилированию. Оценка
клиренса кофеина - важный диагностический тест, позволяющий определить функциональное состояние печени. В связи с тем, что CYP1A2 - главный метаболизирующий фермент кофеина, по сути, в данном тесте определяют активность указанного изофермента. Пациенту предлагают принять внутрь кофеин, меченный радиоактивным изотопом углерода С 13 (С 13 -кофеин), затем выдыхаемый пациентом воздух в течение часа собирают в специальный резервуар и анализируют. При этом в выдыхаемом пациентом воздухе содержится радиоактивный углекислый газ (С 13 О 2 - образован радиоактивным углеродом) и обычный углекислый газ (С 12 О 2). По соотношению в выдыхаемом воздухе С 13 О 2 к С 12 О 2 (измеряют с помощью масс-спектроскопии) определяют клиренс кофеина. Существует модификация этого теста: методом высокоэффективной жидкостной хроматографии определяют концентрацию кофеина и его метаболитов в плазме крови, моче и слюне, взятых натощак. В этом случае определённый вклад в метаболизм кофеина вносят цитохромы CYP3A4 и CYP2D6. Оценка клиренса кофеина - надёж- ный тест, позволяющий оценить функциональное состояние печени при её выраженном поражении (например, при циррозе печени) и определить степень нарушений. К недостаткам теста относят его недостаточную чувствительность при умеренном поражении печени. На результат теста влияют курение (индукция CYP1A2), возраст, совместное применение ЛС, изменяющих активность изоферментов цитохрома Р-450 (ингибиторов или индукторов).
Подсемейство цитохрома Р-450 CYPIIA
Из изоферментов подсемейства CYPIIA наиболее важную роль в метаболизме ЛС играет изофермент цитохрома Р-450 2А6 (CYP2A6). Общее свойство изоферментов подсемейства CYPIIA - способность к индукции под действием фенобарбитала, поэтому подсемейство CYPIIA называют фенобарбитал-индуцибельными цитохромами.
Изофермент цитохрома Р-450 2А6 (CYP2A6) обнаруживают, в основном, в печени. CYP2A6 метаболизирует небольшое число ЛС. С помощью данного изофермента происходит превращение никотина в котинин, а также котинина в 3-гидроксикотинин; 7-гидроксили- рование кумарина; 7-гидроксилирование циклофосфана. CYP2A6 вносит определённый вклад в метаболизм ритонавира, парацетамола и вальпроевой кислоты. CYP2A6 принимает участие в биологической активации компонентов табачного дыма нитрозоаминов - канцерогенов, вызывающих рак лёгких. CYP2A6 способствует биоактивации
мощных мутагенов: 6-амино-(х)-ризена и 2-амино-3-метилмидазо- (4,5-f)-кванолина.
Подсемейство цитохрома Р450 CYPIIB
Из изоферментов подсемейства CYPIIB наиболее важную роль в метаболизме ЛС играет изофермент CYP2В6. Общее свойство изоферментов подсемейства CYPIIB - способность к индукции под действием фенобарбитала.
Изофермент цитохрома Р-450 2В6 (CYP2В6) участвует в метаболизме небольшого числа ЛС (циклофосфамид, тамоксифен, S-метадон p , бупропион р, эфавиренз). В основном CYP2В6 метаболизирует ксенобиотики. Маркёрный субстрат для CYP2В6 - антиконвульсант.
S-мефенитоин p при этом CYP2В6 подвергает S-мефенитоин p N-деметилированию (определяемый метаболит - N-деметилмефени- тоин). CYP2В6 принимает участие в метаболизме эндогенных стероидов: катализирует 16α-16β-гидроксилирование тестостерона.
Подсемейство цитохрома Р-450 CYPIIU
Из всех изоферментов подсемейства цитохрома CYPIIC наиболее важную роль в метаболизме ЛС играют изоферменты цитохрома Р-450 2С8, 2С9, 2С19. Общее свойство цитохромов подсемейства CYPIIC - 4-гидроксилазная активность по отношению к мефенитоину р (противосудорожное ЛС). Мефенитоин р - маркёрный субстрат изоферментов подсемейства CYPIIC. Именно поэтому изоферменты подсемейства CYPIIC называют ещё мефенитоин-4-гидроксилазами.
Изофермент цитохрома Р-450 2С8 (CYP2C8) принимает участие в метаболизме целого ряда лекарственных веществ (НПВС, статины и другие средства). Для многих ЛС CYP2C8 - «альтернативный» путь биотрансформации. Однако для таких препаратов, как репаглинид (гипогликемическое ЛС, принимаемое внутрь) и таксол (цитостатик), CYP2С8 - основной фермент метаболизма. CYP2С8 катализирует реакцию 6а-гидроксилирования таксола. Маркёрный субстрат CYP2С8 - паклитаксел (цитостатический препарат). В ходе взаимодействия паклитаксела с CYP2С8 происходит 6-гидроксилирование цитостатика.
Изофермент цитохрома Р-450 2С9 (CYP2C9) содержится, в основном, в печени. CYP2С9 отсутствует в фетальной печени, его обнаруживают только через месяц после рождения. Активность CYP2С9 не меняется в течение всей жизни. CYP2С9 метаболизирует различные лекарственные вещества. CYP2С9 - главный фермент метаболизма
многих НПВС, в том числе селективных ингибиторов циклоокси- геназы-2, ингибиторов ангиотензиновых рецепторов (лозартана и ирбесартана), гипогликемических препаратов (производных сульфонилмочевины), фенитоина (дифенина ♠), непрямых антикоагулянтов (варфарина 1 , аценокумарола 2), флувастатина 3 .
Следует отметить, что CYP2С9 имеет «стереоселективность» и метаболизирует в основном S-варфарин и S-аценокумарол, в то время как биотрансформация R-варфарина и R-аценокумарола происходит при помощи других изоферментов цитохрома Р-450: CYP1A2, CYP3A4. Индукторы CYP2С9 - рифампицин и барбитураты. Следует отметить, что практически все сульфаниламидные антибактериальные препараты ингибируют CYP2С9. Однако обнаружен специфический ингибитор CYP2С9 - сульфафеназол р. Существуют данные, что экстракт эхинацеи, пурпурной ингибирует CYP2С9 в исследованиях in vitro и in vivo, а гидролизованный экстракт сои (за счёт содержащихся в нём изофлавонов) ингибирует данный изофермент in vitro. Совместное применение ЛС-субстратов CYP2С9 с его ингибиторами приводит к угнетению метаболизма субстратов. В результате могут возникнуть нежелательные лекарственные реакции субстратов CYP2С9 (вплоть до интоксикации). Например, совместное применение варфарина (субстрат CYP2С9) с сульфаниламидными препаратами (ингибиторы CYP2С9) приводит к усилению антикоагулянтного эффекта варфарина. Именно поэтому при сочетании варфарина с сульфаниламидами рекомендуют выполнять строгий (по крайней мере, 1-2 раза в неделю) контроль международного нормализованного отношения. CYP2С9 обладает генетическим полиморфизмом. «Медленные» аллельные варианты CYP2C9*2 и CYP2C9*3- однонуклеотидные полиморфизмы гена CYP2C9, изученные в настоящее время наиболее полно. У носителей аллельных вариантов CYP2C9*2 и CYP2C9*3 отмечают снижение активности CYP2C9; это приводит к снижению скорости биотрансформации ЛС, метаболизирующихся данным изоферментом и к повышению их концентрации в плазме
1 Варфарин - рацематическая смесь изомеров: S-варфарина и R-вафрарина. Следует отметить, что большей антикоагулянтной активностью обладает S-варфарин.
2 Аценокумарол - рацематическая смесь изомеров: S-аценокумарола и R-ацено- кумарола. Однако, в отличие от варфарина, эти два изомера обладают одинаковой антикоагулянтной активностью.
3 Флувастатин - единственное ЛС из группы гиполипидемических препаратов ингибиторов ГМГ-КоА-редуктазы, метаболизм которого происходит при участии CYP2C9, а не CYP3A4. При этом CYP2C9 метаболизирует оба изомера флувастатина: активный (+)-3R,5S-энантиомер и неактивный (-)-3S,5R-энантиомер.
крови. Поэтому гетерозиготы (CYP2C9*1/*2, CYP2C9*1/*3) и гомозиготы (CYP2C9*2/*2, CYP2C9*3/*3, CYP2C9*2/*3) - «медленные» метаболизаторы по CYP2C9. Так, именно у этой категории пациентов (носителей перечисленных аллельных вариантов гена CYP2C9) наиболее часто отмечают нежелательные лекарственные реакции при применении ЛС, метаболизм которых происходит под влиянием CYP2C9 (непрямые антикоагулянты, НПВС, применяемые внутрь гипогликемические ЛС - производные сульфонилмочевины).
Изофермент цитохрома Р-450 2С18 (CYP2C18) содержится в основном в печени. CYP2Cl8 отсутствует в фетальной печени, его обнаруживают только через месяц после рождения. Активность CYP2Cl8 не изменяется в течение всей жизни. CYP2Cl8 вносит определённый вклад в метаболизм таких ЛС, как напроксен, омепразол, пироксикам, пропранолол, изотретиноин (ретиноевая кислота) и варфарин.
Изофермент цитохрома Р-450 2С19 (CYP2C19) - основной фермент метаболизма ингибиторов протонного насоса. При этом метаболизм отдельных ЛС из группы ингибиторов протонного насоса имеет свои особенности. Так, у омепразола обнаружили два пути метаболизма.
Под действием CYP2C19 омепразол превращается в гидроксиомепразол. Под действием CYP3A4 гидроксиомепразол переходит в омепразол гидроксисульфон.
Под действием CYP3A4 омепразол превращается в сульфид омепразола и сульфон омепразола. Под действием CYP2C19 сульфид омепразола и сульфон омепразола переходят в омепразол гидроксисульфон.
Таким образом, вне зависимости от пути биологической трансформации, конечный метаболит омепразола - омепразол гидроксисульфон. Однако следует отметить, что указанные пути метаболизма характерны, прежде всего, для R-изомера омепразола (S-изомер в значительно меньшей степени подвергается биотрансформации). Понимание этого феномена позволило создать эзопразол р - препарат, представляющий S-изомер омепразола (ингибиторы и индукторы CYP2C19, а также генетический полиморфизм этого изофермента в меньшей степени влияют на фармакокинетику эзопразола р).
Метаболизм лансопразола идентичен метаболизму омепразола. Рабепразол метаболизируется при участии CYP2C19 и CYP3A4 до диметилрабепразола и рабепразол сульфона соответственно.
CYP2C19 участвует в метаболизме тамоксифена, фенитоина, тиклопидина, таких психотропных ЛС, как трициклические антидепрессанты, диазепам, некоторые барбитураты.
Для CYP2C19 характерен генетический полиморфизм. Медленные метаболизаторы по CYP2Cl9 - носители «медленных» аллельных вариантов. Применение у медленных метаболизаторов по CYP2CL9 препаратов - субстратов этого изофермента приводит к более частому возникновению нежелательных лекарственных реакций, особенно при использовании препаратов с узкой терапевтической широтой: трициклических антидепрессантов, диазепама, некоторых барбитуратов (мефобарбитала, гексобарбитала). Однако наибольшее количество исследований посвящено влиянию полиморфизма гена CYP2C19 на фармакокинетику и фармакодинамику блокаторов ингибиторов протонного насоса. Как показали фармакокинетические исследования, проведённые при участии здоровых добровольцев, площадь под фармакокинетической кривой, значения максимальной концентрации омепразола, лансопразола и рабепразола достоверно выше у гетерозигот и, особенно, у гомозигот по «медленным» аллельным вариантам гена CYP2C19. Кроме того, более выраженное подавление желудочной секреции при применении омепразола, лансорпразола, рабепразола наблюдали у пациентов (гетерозиготы и гомозиготы по «медленным» аллельным вариантам CYP2C19), страдающих язвенной болезнью и рефлюкс-эзофагитом. Однако частота нежелательных лекарственных реакций ингибиторов протонного насоса не зависит от генотипа по CYP2C19. Существующие данные позволяют предположить, что для достижения «целевого» подавления желудочной секреции у гетерозигот и гомозигот по «медленным» аллельным вариантам гена CYP2C19 необходимы меньшие дозы ингибиторов протонного насоса.
Подсемейство цитохрома Р-450 CYPIID
В состав подсемейства цитохрома Р-450 CYPIID входит единственный изофермент - 2D6 (CYP2D6).
Изофермент цитохрома Р-450 2D6 (CYP2D6) обнаруживают в основном в печени. CYP2D6 метаболизирует около 20% всех известных ЛС, в том числе нейролептики, антидепрессанты, транквилизаторы, β-адреноблокаторы. Доказано: CYP2D6 - главный фермент биотрансформации и трициклического антидепрессанта амитриптилина. Однако, как показали исследования, незначительная часть амитриптилина метаболизируется и другими изоферментами цитохрома Р-450 (CYP2C19, CYP2C9, CYP3A4) до неактивных метаболитов. Дебризохин р, декстрометорфан и спартеин - маркёрные субстраты, используемые для фенотипирования изофермента 2D6. CYP2D6, в отличие от других изоферментов цитохрома Р-450, не имеет индукторов.
Ген CYP2D6 обладает полиморфизмом. Еще в 1977 году Iddle и Mahgoub обратили внимание на различие гипотензивного эффекта у больных артериальной гипертензией, применявших дебризохин р (препарат из группы α-адреноблокаторов). Тогда же сформулировали предположение о различии скорости метаболизма (гидроксилирования) дебризохина р у разных индивидуумов. У «медленных» метаболизаторов дебризохина р зарегистрировали наибольшую выраженность гипотензивного эффекта данного препарата. Позднее доказали, что у «медленных» метаболизаторов дебризохина р замедлен метаболизм и некоторых других ЛС, в том числе фенацетина, нортриптилина р, фенформина р, спартеина, энкаинида р, пропранолола, гуаноксана р и амитриптилина. Как показали дальнейшие исследования, «медленные» метаболизаторы по CYP2D6 - носители (как гомозиготы, так и гетерозиготы) функционально дефектных аллельных вариантов гена CYP2D6. Результат этих вариантов - отсутствие синтеза CYP2D6 (аллельный вариант CYP2D6x5), синтез неактивного белка (аллельные варианты CYP2D6x3, CYP2D6x4, CYP2D6x6, CYP2D6x7, CYP2D6x8, CYP2D6x11, CYP2D6x12, CYP2D6x14, CYP2D6x15, CYP2D6x19, CYP2D6x20), синтез дефектного белка со сниженной активностью (варианты CYP2D6x9, CYP2D6x10, CYP2D6x17,
CYP2D6x18, CYP2D6x36). С каждым годом растёт количество найденных аллельных вариантов гена CYP2D6 (их носительство приводит к изменению активности CYP2D6). Однако ещё Saxena (1994) указывал, что 95% всех «медленных» метаболизаторов по CYP2D6 - носители вариантов CYP2D6x3, CYP2D6x4, CYP2D6x5, остальные варианты обнаруживают гораздо реже. По данным Rau и соавт. (2004), частота аллельного варианта CYP2D6x4 среди пациентов, у которых наблюдали нежелательные лекарственные реакции на фоне приёма трициклических антидепрессантов (артериальная гипотензия, седативный эффект, тремор, кардиотоксичность), почти в 3 раза (20%) превышает таковую у пациентов, при лечении которых указанными препаратами осложнений не регистрировали (7%). Аналогичное влияние генетического полиморфизма CYP2D6 обнаружили и на фармакокинетику и фармакодинамику нейролептиков, в результате продемонстрировали наличие ассоциаций между носительством некоторых аллельных вариантов гена CYP2D6 и развитием индуцированных нейролептиками экстрапирамидных нарушений.
Однако носительство «медленных» аллельных вариантов гена CYP2D6 может сопровождаться не только увеличением риска развития нежелательных лекарственных реакций при применении препа-
ратов, метаболизирующихся данным изоферментом. Если ЛС - пролекарство, а активный метаболит образуется именно под действием CYP2D6, то у носителей «медленных» аллельных вариантов отмечают низкую эффективность препарата. Так, у носителей «медленных» аллельных вариантов гена CYP2D6 регистрируют менее выраженный анальгезирующий эффект кодеина. Этот феномен объясняют снижением О-деметилирования кодеина (в ходе указанного процесса образуется морфин). Обезболивающее действие трамадола также обусловлено активным метаболитом О-деметилтрамадолом (образуется под действием CYP2D6). У носителей «медленных» аллелельных вариантов гена CYP2D6 отмечают значительное уменьшение синтеза О-деметилтрамадола; это может привести к недостаточному анальгезирующему эффекту (аналогично процессам, возникающим при использовании кодеина). Так, Stamer и соавт. (2003), изучив анальгезирующий эффект трамадола у 300 пациентов, перенёсших операции на брюшной полости, обнаружили, что гомозиготы по «медленным» аллельным вариантам гена CYP2D6 не «отвечали» на терапию трамадолом в 2 раза чаще, чем пациенты, не несущие данных аллелей (46,7% против 21,6% соответственно, р=0,005).
В настоящее время выполнили множество исследований, посвя- щённых влиянию генетического полиморфизма CYP2D6 на фармакокинетику и фармакодинамику β-адреноблокаторов. Результаты этих исследований имеют клиническое значение для индивидуализации фармакотерапии данной группой ЛС.
Подсемейство цитохрома Р-450 CYPIIB
Из изоферментов подсемейства цитохрома IIE наиболее важную роль в метаболизме ЛС играет изофермент цитохрома Р-450 2Е1. Общее свойство изоферментов подсемейства CYPIIE - способность к индукции под влиянием этанола. Именно поэтому второе название подсемейства CYPIIE - этанол-индуцибельные цитохромы.
Изофермент цитохрома Р-450 2Е1 (CYP2E1) содержится в печени взрослых. CYP2E1 составляет около 7% всех изоферментов цитохрома Р-450. Субстраты CYP2E1 - малое количество ЛС, а также некоторые другие ксенобиотики: этанол, нитрозоамины, «небольшие» ароматические углеводороды типа бензола и анилина, алифатические хлоруглеводороды. CYP2E1 катализирует превращение дапсона в гидроксиламиндапсон, n1-деметилирование и N7-деметилирование кофеина, дегалогенизацию хлорфторуглеводородов и средств для ингаляционного наркоза (галотан) и некоторые другие реакции.
CYP2E1 вместе с CYP1A2 катализируют важную реакцию превращения парацетамола (ацетаминофена) в N-ацетилбензохинонимин, обладающий мощным гепатотоксическим действием. Существуют данные об участии цитохрома CYP2E1 ватерогенезе. Например, известно, что CYP2E1 - наиболее важный изофермент цитохрома Р-450, окисляющий холестерин липопротеидов низкой плотности (ЛНП). В процессе окисления ЛНП также принимают участие цитохромы и другие изоферменты цитохрома Р-450, а также 15-липооксигеназа и НАДФ-Н-оксидазы. Продукты окисления: 7а-гидроксихолестерол, 7β -гидроксихолестерол, 5β -6β -эпоксихолестерол, 5 α-6β -эпоксихолестерол, 7-кетохолестерол, 26-гидроксихолестерол. Процесс окисления ЛНП происходит в эндотелиоцитах, гладкой мускулатуре кровеносных сосудов, макрофагах. Окисленные ЛНП стимулируют формирование пенистых клеток и таким образом способствуют образованию атеросклеротических бляшек.
Подсемейство цитохрома Р-450 CYPIIIA
Подсемейство цитохрома Р-450 CYPIIIA включает четыре изофермента: 3А3, 3А4, 3А5 и 3А7. Цитохромы подсемейства IIIA составляют 30% всех изоферментов цитохрома Р-450 в печени и 70% всех изоферментов стенки пищеварительного тракта. При этом в печени преимущественно локализован изофермент 3А4 (CYP3A4), в стенках желудка и кишечника - изоферменты 3А3 (CYP3A3) и 3А5 (CYP3A5). Изофермент 3А7 (CYP3A7) обнаруживают только в печени плода. Из изоферментов подсемейства IIIA наиболее важную роль в метаболизме ЛС играет CYP3A4.
Изофермент цитохрома Р-450 3А4 (CYP3A4) метаболизирует около 60% всех известных ЛС, в том числе блокаторы медленных кальциевых каналов, макролидные антибиотики, некоторые антиаритмики, статины (ловастатин, симвастатин, аторвастатин), клопидогрел 1 и другие препараты.
CYP3A4 катализирует реакцию 6β-гидроксилирования эндогенных стероидов, в том числе тестостерона, прогестерона, кортизола p . Маркёрные субстраты для определения активности CYP3A4 - дапсон, эритромицин, нифедипин, лидокаин, тестостерон и кортизол p .
Метаболизм лидокаина протекает в гепатоцитах, где через оксидативное N-деэтилирование CYP3A4 образуется моноэтилглицинксилидид (MEGX).
1 Клопидогрел - пролекарство, под действием CYP3A4 он превращается в активный метаболит, обладающий антиагрегантным действием.
Определение активности CYP3A4 по MEGX (метаболит лидокаина) - наиболее чувствительный и специфичный тест, позволяющий оценить функциональное состояние печени при острых и хронических её заболеваниях, а также при синдроме системного воспалительного ответа (сепсисе). При циррозе печени концентрация MEGX коррелирует с прогнозом заболевания.
В литературе существуют данные о внутривидовой вариабельности метаболизма ЛС под действием CYP3A4. Однако молекулярные подтверждения генетического полиморфизма CYP3A4 появились только в последнее время. Так, A. Lemoin и соавт. (1996) описали случай интоксикации такролимусом (субстрат CYP3A4) у больного после пересадки печени (в клетках печени активность CYP3A4 обнаружить не удалось). Только после обработки клеток пересаженной печени глюкокортикоидами (индукторы CYP3A4) можно определить активность CYP3A4. Существует предположение, что нарушение экспрессии факторов транскрипции гена, кодирующего CYP3A4, - причина вариабельности метаболизма данного цитохрома.
Изофермент цитохрома Р-450 3А5 (CYP3A5), по последним данным, может играть существенную роль в метаболизме некоторых лекарственных веществ. Следует отметить, что CYP3A5 экспрессируется в печени 10-30% взрослых людей. У этих индивидуумов вклад CYP3A5 в активность всех изоферментов подсемейства IIIA составляет от 33 (у европейцев) до 60% (у афроамериканцев). Как показали исследования, под влиянием CYP3A5 происходят процессы биотрансформации тех ЛС, которые традиционно рассматривают как субстраты CYP3A4. Следует отметить, что индукторы и ингибиторы CYP3A4 обладают аналогичным действием и в отношении CYP3A5. Активность CYP3A5 у различных индивидуумов варьирует более чем в 30 раз. Впервые различия активности CYP3A5 описали Paulussen и соавт. (2000): они наблюдали in vitro существенные различия скорости метаболизма мидазолама под влиянием CYP3A5.
Дигидропиримидин дегидрогеназа
Физиологическая функция дигидропиримидин дегидрогеназы (ДПДГ) - восстановление урацила и тимидина - первая реакция трёхэтапного метаболизма этих соединений до β-аланина. Кроме того, ДПДГ - основной фермент, метаболизирующий 5-фторура- цил. Указанный препарат применяют в составе комбинированной химиотерапии рака молочной железы, яичников, пищевода, желудка, толстой и прямой кишки, печени, шейки матки, вульвы. Также
5-фторурацил используют при лечении рака мочевого пузыря, простаты, опухолей головы, шеи, слюнных желёз, надпочечников, поджелудочной железы. В настоящее время известна аминокислотная последовательность и количество аминокислотных остатков (их всего 1025), входящих в состав ДПДГ; молекулярная масса фермента составляет 111 кД. Идентифицировали ген ДПДГ, локализованный в хромосоме 1 (локус 1р22). Цитоплазма клеток различных тканей и органов содержит ДПДГ, особенно большое количество фермента обнаруживают в клетках печени, в моноцитах, лимфоцитах, гранулоцитах, тромбоцитах. Однако в эритроцитах активность ДПДГ не отмечена (Van Kuilenburg и соавт., 1999). С середины 80-х годов появились сообщения о серьёзных осложнениях, возникающих при применении 5-фторурацила (причина осложнений - наследственно обусловленная низкая активность ДПДГ). Как показали Diasio и соавт. (1988), низкая активность ДПДГ наследуется по аутосомнорецессивному типу. Таким образом, ДПДГ - фермент, обладающий генетическим полиморфизмом. В будущем, по-видимому, произой- дёт внедрение методов фенотипирования и генотипирования ДПДГ в онкологическую практику для обеспечения безопасности химиотерапии 5-фторурацилом.
5.4. ФЕРМЕНТЫ II ФАЗЫ БИОТРАНСФОРМАЦИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Глюкуронилтрансферазы
Глюкуронирование - наиболее важная реакция II фазы метаболизма лекарственных веществ. Глюкуронирование представляет присоединение (конъюгацию) к субстрату уридиндифосфат-глюкуроновой кислоты (УДФ-глюкуроновой кислоты). Эта реакция катализируется надсемейством ферментов, называемых «УДФ-глюкуронилтрансферазы» и обозначаемых как UGT. Надсемейство УДФ-глюкуронилтрансфераз включает два семейства и более двадцати изоферментов, локализованных в эндоплазматической системе клеток. Они катализируют глюкуронирование большого количества ксенобиотиков, включая ЛС и их метаболиты, пестициды и канцерогены. К соединениям, подвергающимся глюкуронированию, относят простые и сложные эфиры; соединения, содержащие карбоксильные, карбомоильные, тиольные и карбонильные группы, а также нитрогруппы. Глюкуронирование
приводит к увеличению полярности химических соединений, что облегчает их растворимость в воде и элиминацию. УДФ-глюкуронилтрансферазы обнаруживают у всех позвоночных животных: от рыб до человека. В организме новорождённых регистрируют низкую активность УДФ-глюкуронилтрансфераз, однако через 1-3 мес жизни активность данных ферментов можно сравнить с таковой у взрослых. УДФ-глюкуронилтрансферазы содержатся в печени, кишечнике, лёг- ких, головном мозге, обонятельном эпителии, почках, но печень - главный орган, в котором происходит глюкуронирование. Степень экспрессии различных изоферментов УДФ-глюкуронилтрансферазы в органах неодинакова. Так, изофермент УДФ-глюкуронилтрансферазы UGT1A1, катализирующий реакцию глюкуронирования билирубина, экспрессируется главным образом в печени, но не в почках. Изоферменты УДФ-глюкуронилтрансферазы UGT1A6 и UGT1A9, ответственные за глюкуронирование фенола, экспрессируются и в печени, и в почках одинаково. Как указывалось выше, по идентичности аминокислотного состава надсемейство УДФ-глюкуронилтрансфераз подразделяют на два семейства: UGT1 и UGT2. Изоферменты, семейства UGT1 сходны по аминокислотному составу на 62-80%, а изоферменты семейства UGT2 - на 57-93%. Изоферменты, входящие в состав семейств УДФ-глюкуронилтрансферазы человека, а также локализация генов и маркёрные субстраты изоферментов для фенотипирования представлены в таблице (табл. 5-7).
Физиологическая функция УДФ-глюкуронилтрансфераз - глюкуронирование эндогенных соединений. Продукт катаболизма гема - билирубин - наиболее хорошо изученный эндогенный субстрат УДФ-глюкуронилтрансферазы. Глюкуронирование билирубина предотвращает накопление токсичного свободного билирубина. При этом билирубин выделяется с желчью в виде моноглюкуронидов и диглюкуронидов. Другая физиологическая функция УДФ-глюкуронилтрансферазы - участие в метаболизме гормонов. Так, тироксин и трийодтиронин подвергаются глюкуронированию в печени и выводятся в виде глюкуронидов с желчью. УДФ-глюкуронилтрансферазы также участвуют в метаболизме стероидных гормонов, желчных кислот, ретиноидов, однако эти реакции в настоящее время изучены недостаточно.
Глюкуронированию подвергаются ЛС разных классов, многие из них имеют узкую терапевтическую широту, например, морфин и хлорамфеникол (табл. 5-8).
Таблица 5-7. Состав семейств УДФ-глюкуронилтрансферазы человека, локализация генов и маркёрные субстраты изоферментов
 Таблица 5-8.
Лекарственные
средства, метаболиты и ксенобиотики, подвергающиеся глюкоуронированию
различными изоферментами УДФ-глюкуронилтрансферазы
Таблица 5-8.
Лекарственные
средства, метаболиты и ксенобиотики, подвергающиеся глюкоуронированию
различными изоферментами УДФ-глюкуронилтрансферазы
 Окончание таблицы 5-8
Окончание таблицы 5-8
 Лекарственные средства (представители разных химических групп), подвергающиеся глюкуронированию
Лекарственные средства (представители разных химических групп), подвергающиеся глюкуронированию
Фенолы: пропофол, ацетаминофен, налоксон.
Спирты: хлорамфеникол, кодеин, оксазепам.
Алифатические амины: циклопироксоламин p , ламотриджин, амитриптилин.
Карбоновые кислоты: ферпазон p , фенилбутазон, сульфинпиразон.
Карбоксильные кислоты: напроксен, зомепирал p , кетопрофен. Таким образом, глюкуронированию подвергаются соединения,
содержащие разные функциональные группы, выполняющие функции акцепторов для УДФ-глюкуроновой кислоты. Как указывалось выше, в результате глюкуронирования образуются полярные неактивные метаболиты, легко выводящиеся из организма. Однако существует пример, когда в результате глюкуронирования образуется активный метаболит. Глюкуронирование морфина приводит к образованию морфин-6-глюкуронида, обладающего значительным анальгезирующим эффектом и реже, чем морфин, вызывающего тошноту и рвоту. Также глюкуронирование может способствовать биологической активации канцерогенов. К канцерогенным глюкуронидам относят N-глюкуронид 4-аминобифенила, N-глюкуронид N-ацетил- бензидина,О-глюкуронид-4-((гидрокисметил)-нитрозоамино)-1-(3-пи- ридил)-1-бутанона.
Давно известно о существовании наследственных нарушений глюкуронирования билирубина. К ним относят синдром Жильбера и синдром Криглера-Найяра. Синдром Жильбера - наследственное заболевание, наследуемое по аутосомно-рецессивному типу. Распространённость синдрома Жильбера среди населения составляет 1-5%. Причина развития данного заболевания - точечные мутации (как правило, замены в нуклеотидной последовательности) в гене UGT1. При этом образуется УДФ-глюкуронилтрансфераза, характеризующаяся малой активностью (25-30% от нормального уровня). Изменение глюкуронирования лекарственных веществ у больных с синдромом Жильбера изучено мало. Существуют данные о снижении клиренса толбутамида, парацетамола (ацетаминофена ♠) и рифампина p у больных с синдромом Жильбера. Изучали частоту побочных эффектов нового цитостатического препарата иринотекана у пациентов, страдающих одновременно колоректальным раком и синдромом Жильбера и у больных колоректальным раком. Иринотекан (СТР-11) - новый высокоэффективный препарат, обладающий цитостатическим действием, ингибирующий топоизомеразу I и применяемый при колоректальном раке при наличии резистентности к фторурацилу. Иринотекан в печени под действием карбоксиэстераз превращает-
ся в активный метаболит 7-этил-10-гидроксикамптотекин (SN-38). Главный путь метаболизма SN-38 - глюкуронирование с помощью UGT1A1. В ходе исследований побочные эффекты иринотекана (в частности, диарею) достоверно чаще регистрировали у больных, имеющих синдром Жильбера. Учёные доказали: носительство аллельных вариантов UGT1A1x1B, UGT1A1x26, UGT1A1x60 ассоциируется с более частым развитием гипербилирубинемии при применении иринотекана, при этом регистрировали низкие значения площади под фармакокинетической кривой глюкуронида SN-38. В настоящее время Американским управлением по контролю над пищевыми продуктами и медикаментами (Food and drug administration - FDA) одобрено определение аллельных вариантов гена UGT1A1 для выбора режима дозирования иринотекана. Существуют данные о влиянии носительства аллельных вариантов генов, кодирующих и другие изоформы UGT, на фармакокинетику и фармакодинамику различных ЛС.
Ацетилтрансферазы
Ацетилирование эволюционно представляет один из самых ранних механизмов адаптации. Реакция ацетилирования необходима для синтеза жирных кислот, стероидов, функционирования цикла Кребса. Важная функция ацетилирования - метаболизм (биотрансформация) ксенобиотиков: ЛС, бытовых и промышленных ядов. На процессы ацетилирования влияет N-ацетилтрансфераза, а также кофермент А. Контроль интенсивности ацетилирования в организме человека происходит при участии β 2 -адренорецепторов и зависит от метаболических резервов (пантотеновой кислоты, пиридоксина, тиамина, липоевой кислоты *) и генотипа. Кроме того, интенсивность ацетилирования зависит от функционального состояния печени и других органов, содержащих N-ацетилтрансферазу (хотя ацетилирование, как и другие реакции II фазы, мало изменяется при заболеваниях печени). Между тем ацетилирование ЛС и других ксенобиотиков происходит преимущественно в печени. Выделено два изофермента N-ацетилтрансферазы: N-ацетилтрансфераза 1 (NAT1) и N-ацетилтрансфераза 2 (NAT2). NAT1 ацетилирует небольшое количество ариламинов и не обладает генетическим полиморфизмом. Таким образом, основной фермент ацетилирования - NAT2 . Ген NAT2 расположен в хромосоме 8 (локусы 8р23.1, 8р23.2 и 8р23.3). NAT2 ацетилирует различные ЛС, в том числе изониазид и сульфаниламиды (табл. 5-9).
Таблица 5-9. Лекарственные средства, подвергающиеся ацетилированию
 Наиболее
важным свойством NAT2 считают генетический полиморфизм. Впервые
полиморфизм ацетилирования описал в 1960-е годы Evans; он выделил
медленные и быстрые ацетиляторы изониазида. Также отметили, что у
«медленных» ацетиляторов, в связи с накоплением (кумуляцией) изониазида,
чаще возникают полиневриты. Так, у «медленных» ацетиляторов период
полувыведения изониазида составляет 3 ч, в то время как у «быстрых»
ацетиляторов - 1,5 ч. Развитие полиневритов обусловлено влиянием
изониазида: препарат тормозит переход пиридоксина (витамина В 6)
в активный кофермент дипиридоксинфосфат, необходимый для синтеза
миелина. Предполагали, что у «быстрых» ацетиляторов применение
изониазида с большей вероятностью приведёт к развитию гепатотоксического
эффекта из-за более интенсивного образования ацетилгидразина, однако
практического подтверждения это предположение не получило.
Индивидуальная скорость ацетилирования существенно не влияет на режим
дозирования препарата при ежедневном приёме, но может уменьшать
эффективность терапии при периодическом использовании изониазида.
Проанализировав результаты лечения изониазидом 744 больных туберкулёзом,
выяснили, что у «медленных» ацетиляторов закрытие полостей в лёгких
происходит быстрее. Как показало исследование, проведённое Sunahara в
1963 году, «медленные» ацетиляторы - гомозиготы по «медленной» аллели
NAT2, а «быстрые» метаболизаторы - гомозиготы либо гетерозиготы по
«быстрой» аллели NAT2. В 1964 году Evans опубликовал данные о том, что
полиморфизм ацетилирования характерен не только для изониазида, но и для
гидралазина и сульфаниламидов. Затем наличие полиморфизма ацетили-
Наиболее
важным свойством NAT2 считают генетический полиморфизм. Впервые
полиморфизм ацетилирования описал в 1960-е годы Evans; он выделил
медленные и быстрые ацетиляторы изониазида. Также отметили, что у
«медленных» ацетиляторов, в связи с накоплением (кумуляцией) изониазида,
чаще возникают полиневриты. Так, у «медленных» ацетиляторов период
полувыведения изониазида составляет 3 ч, в то время как у «быстрых»
ацетиляторов - 1,5 ч. Развитие полиневритов обусловлено влиянием
изониазида: препарат тормозит переход пиридоксина (витамина В 6)
в активный кофермент дипиридоксинфосфат, необходимый для синтеза
миелина. Предполагали, что у «быстрых» ацетиляторов применение
изониазида с большей вероятностью приведёт к развитию гепатотоксического
эффекта из-за более интенсивного образования ацетилгидразина, однако
практического подтверждения это предположение не получило.
Индивидуальная скорость ацетилирования существенно не влияет на режим
дозирования препарата при ежедневном приёме, но может уменьшать
эффективность терапии при периодическом использовании изониазида.
Проанализировав результаты лечения изониазидом 744 больных туберкулёзом,
выяснили, что у «медленных» ацетиляторов закрытие полостей в лёгких
происходит быстрее. Как показало исследование, проведённое Sunahara в
1963 году, «медленные» ацетиляторы - гомозиготы по «медленной» аллели
NAT2, а «быстрые» метаболизаторы - гомозиготы либо гетерозиготы по
«быстрой» аллели NAT2. В 1964 году Evans опубликовал данные о том, что
полиморфизм ацетилирования характерен не только для изониазида, но и для
гидралазина и сульфаниламидов. Затем наличие полиморфизма ацетили-
рования доказали и для других лекарственных средств. Применение прокаинамида и гидралазина у «медленных» ацетиляторов гораздо чаще вызывает поражение печени (гепатотоксичность), таким образом, и для этих препаратов характерен полиморфизм ацетилирования. Однако в случае с дапсоном (также подвергается ацетилированию) не удалось обнаружить различий в частоте возникновения волчаночноподобного синдрома при применении данного препарата «медленными» и «быстрыми» ацетиляторами. Распространённость «медленных» ацетиляторов варьирует: от 10-15% среди японцев и китайцев до 50% среди представителей европеоидной расы. Только в конце 80-х годов начали идентифицировать аллельные варианты гена NAT2, носительство которых обусловливает медленное ацетилирование. В настоящее время известно около 20 мутантных аллелей гена NAT2. Все указанные аллельные варианты наследуются по аутосомно-рецессивному типу.
Тип ацетилирования определяют, используя методы фенотипирования и генотипирования NAT2. В качестве маркёрных субстратов ацетилирования используют дапсон, изониазид и сульфадимин (сульфадимезин *). Отношение концентрации моноацетилдапсона к концентрации дапсона менее 0,35 в плазме крови через 6 ч после введения препарата характерно для «медленных» ацетиляторов, а более 0,35 - для «быстрых» ацетиляторов. Если в качестве маркерного субстрата используют сульфадимин, то наличие менее 25% сульфадимина в плазме крови (анализ выполняют через 6 ч) и менее 70% в моче (собранной через 5-6 ч после введения препарата) свидетельствует о фенотипе «медленного» ацетилирования.
Тиопурин S-метилтрансфераза
Тиопурин S-метилтрансфераза (ТРМТ) - фермент, катализирующий реакцию S-метилирования производных тиопурина - основной путь метаболизма цитостатических веществ из группы антагонистов пурина: 6-меркаптопурина, 6-тиогуанина, азатиоприна. 6-мер- каптопурин используют в составе комбинированной химиотерапии миелобластного и лимфобластного лейкоза, хронического миелолейкоза, лимфосаркомы, саркомы мягких тканей. При острых лейкозах применяют, как правило, 6-тиогуанин. В настоящее время известна аминокислотная последовательность и количество аминокислотных остатков, входящих в состав ТРМТ, - 245. Молекулярная масса ТРМТ составляет 28 кДа. Также идентифицировали ген ТРМТ, локализованный в хромосоме 6 (локус 6q22.3). ТРМТ располагается в цитоплазме кроветворных клеток.
В 1980 году Weinshiboum изучал активность ТРМТ у 298 здоровых добровольцев и обнаружил значительные различия активности ТРМТ у людей: 88,6% обследованных имели высокую активность ТРМТ, 11,1% - промежуточную. Низкую активность ТРМТ (или полное отсутствие активности фермента) зарегистрировали у 0,3% обследованных добровольцев. Так впервые описали генетический полиморфизм ТРМТ. Как показали более поздние исследования, для людей с низкой активностью ТРМТ характерна повышенная чувствительность к 6-меркаптопурину, 6-тиогуанину и азатиоприну; при этом развиваются опасные для жизни гематотоксические (лейкопения, тромбоцитопения, анемия) и гепатотоксические осложнения. В условиях низкой активности ТРМТ, метаболизм 6-меркаптопурина идёт по альтернативному пути - до высокотоксичного соединения 6-тио- гуанина нуклеотида. Lennard и соавт. (1990) изучали концентрацию 6-тиогуанина нуклеотида в плазме крови и активность ТРМТ в эритроцитах 95 детей, получавших 6-меркаптопурин по поводу острого лимфобластного лейкоза. Авторы выяснили: чем меньше активность ТРМТ, тем выше концентрации 6-TGN в плазме крови и тем более выражены побочные эффекты 6-меркаптопурина. В настоящее время доказано, что низкая активность ТРМТ наследуется по аутосомнорецессивному типу, причём у гомозигот регистрируют низкую активность ТРМТ, а у гетерозигот - промежуточную. Генетические исследования последних лет, выполненные методом полимеразной цепной реакции, позволили обнаружить мутации гена ТРМТ, определяющие низкую активность данного фермента. Безопасные дозы 6-меркапто- пурина: при высокой активности ТРМТ (нормальный генотип) назначают по 500 мг/(м 2 ×сутки), при промежуточной активности ТРМТ (гетерозиготы) - по 400 мг/(м 2 ×сутки), при медленной активности ТРМТ (гомозиготы) - по 50 мг/(м 2 ×сутки).
Сульфотрансферазы
Сульфатирование - реакция присоединения (конъюгации) к субстрату остатка серной кислоты, при этом образуются сложные эфиры серной кислоты или сульфоматы. Сульфатированию в организме человека подвергаются экзогенные соединения (в основном фенолы) и эндогенные соединения (гормоны щитовидной железы, катехоламины, некоторые стероидные гормоны). В качестве кофермента реакции сульфатирования выступает 3"-фосфоаденилсульфат. Затем происходит превращение 3"-фосфоаденилсульфата в аденозин- 3",5"-бифосфонат. Реакция сульфатирования катализируется над-
семейством ферментов, называемых «сульфотрансферазы» (SULT). Сульфотрансферазы локализуются в цитозоле. В организме человека обнаружили три семейства. В настоящее время идентифицировали около 40 изоферментов сульфотрансферазы. Изоферменты сульфотрансферазы в организме человека кодируются, по крайней мере, 10 генами. Наибольшая роль в сульфатировании лекарственных веществ и их метаболитов принадлежит изоферментам сульфотрансферазы семейства 1 (SULT1). SULT1A1 и SULT1A3 - самые важные изоферменты данного семейства. Изоферменты SULT1 локализованы главным образом в печени, а также толстой и тонкой кишке, лёгких, головном мозге, селезёнке, плаценте, лейкоцитах. Изоферменты SULT1 имеют молекулярную массу около 34 кДа и состоят из 295 аминокислотных остатков, ген изоферментов SULT1 локализован в 16 хромосоме (локус 16р11.2). SULT1A1 (термостабильная сульфотрансфераза) катализирует сульфатирование «простых фенолов», в том числе лекарственных веществ фенольной структуры (миноксидил р, ацетаминофен, морфин, салициламид, изопреналин и некоторые другие). Следует отметить, что сульфатирование миноксидила р приводит к образованию его активного метаболита - миноксидила сульфата. SULT1A1 сульфатирует метаболиты лидокаина: 4-гидрокси-2,6-ксилидин(4-гидроксил) и ропивакаина: 3-гид- роксиропивакаин, 4-гидроксиропивакаин, 2-гидроксиметилропива- каин. Кроме того, SULT1A1 сульфатирует 17β-эстрадиол. Маркёрный субстрат SULT1A1 - 4-нитрофенол. SULT1A3 (термолабильная сульфотрансфераза) катализирует реакции сульфатирования фенольных моноаминов: дофамина, норадреналина, серотонина. Маркёрный субстрат SULT1A3 - дофамин. Изоферменты сульфотрансферазы семейства 2 (SULT2) обеспечивают сульфатирование дигидроэпиандростерона, эпиандростерона, андростерона. Изоферменты SULT2 участвуют в биологической активации канцерогенов, например, ПАУ (5-гидроксиметилхризен, 7,12-дигидроксиметилбенз[а]антрацен), N-гидрокси-2-ацетиламинофлуорен. Изоферменты сульфотрансферазы семейства 3 (SULT3) катализируют N-сульфатирование ациклических ариламинов.
Эпоксидгидролаза
Водная конъюгация играет важную роль в детоксикации и биологической активации большого количества ксенобиотиков, таких, как арены, алифатические эпоксиды, ПАУ, афлотоксин В1. Реакции водной конъюгации катализирует особый фермент - эпоксидгидролаза
(ЕРНХ). Наибольшее количество данного фермента обнаружено в печени. Учёные выделили две изоформы эпоксидгидролазы: ЕРНХ1 и ЕРНХ2. ЕРНХ2 состоит из 534 аминокислотных остатков, имеет молекулярную массу 62 кДа; ген ЕРНХ2 располагается в хромосоме 8 (локус 8р21-р12). ЕРНХ2 локализуется в цитоплазме и пероксисомах; данная изоформа эпоксидгидролазы играет небольшую роль в метаболизме ксенобиотиков. Большую часть реакций водной конъюгации катализирует ЕРНХ1. ЕРНХ1 состоит из 455 аминокислотных остатков, имеет молекулярную массу 52 кДа. Ген ЕРНХ1 располагается в хромосоме 1 (локус 1q42.1). Велико значение ЕРНХ1 в водной конъюгации токсических метаболитов лекарственных веществ. Противосудорожное средство фенитоин окисляется цитохромом Р-450 до двух метаболитов: парагидроксилатеда и дигидродиола. Указанные метаболиты - активные электрофильные соединения, способные ковалентно связываться с макромолекулами клеток; это приводит к гибели клетки, формированию мутаций, озлокачествлению, дефектам митоза. Кроме того, парагидроксилатед и дигидродиол, действуя как гаптены, могут вызывать и иммунологические реакции. Гиперплазия дёсен, а также тератогенные эффекты - токсические реакции фенитоина зарегистрированы у животных. Доказано, что эти эффекты обусловлены действием метаболитов фенитоина: парагидроксилатеда и дигидродиола. Как показали Buecher и соавт. (1990), низкая активность ЕРНХ1 (меньше 30% от нормы) в амниоцитах - серьёзный фактор риска развития врождённых аномалий плода у женщин, принимающих во время беременности фенитоин. Доказано также, что основная причина снижения активности ЕРНХ1 - точечная мутация в экзоне 3 гена ЕРНХ1; в результате синтезируется дефектный фермент (тирозин в 113 положении заменён на гистидин). Мутация наследуется по аутосомнорецессивному типу. Снижение активности ЕРНХ1 наблюдают только у гомозигот по этой мутантной аллели. Данные о распространённости гомозигот и гетерозигот по этой мутации отсутствуют.
Глутатионтрансферазы
Конъюгации с глутатионом подвергаются ксенобиотики с различной химической структурой: эпоксиды, ареноксиды, гидроксиламины (некоторые из них обладают канцерогенным действием). Среди лекарственных веществ конъюгации с глутатионом подвергаются этакриновая кислота (урегит ♠) и гепатотоксичный метаболит парацетамола (ацетаминофена ♠) - N-ацетилбензохинонимин, превраща-
ющийся при этом в нетоксичное соединение. В результате реакции конъюгации с глутатионом образуются цистеиновые конъюгаты, называемые «тиоэстеры». Конъюгацию с глутатионом катализируют ферменты глутатион SH-S-трансферазы (GST). Эта группа ферментов локализована в цитозоле, хотя описана и микросомальная GST (однако её роль в метаболизме ксенобиотиков изучена мало). Активность GST в эритроцитах человека у различных индивидуумов различается в 6 раз, однако зависимость активности фермента от пола при этом отсутствует). Тем не менее, как показали исследования, существует чёткая корреляция активности GST у детей и их родителей. По идентичности аминокислотного состава у млекопитающих выделяют 6 классов GST: α- (альфа-), μ- (мю-), κ- (каппа-), θ- (тета-), π- (пи-) и σ- (сигма-) GST. В организме человека в основном экспрессируются GST классов μ (GSTM), θ (GSTT и π (GSTР). Среди них наибольшее значение в метаболизме ксенобиотиков имеют GST класса μ, обозначаемые как GSTM. В настоящее время выделено 5 изоферментов GSTM: GSTM1, GSTM2, GSTM3, GSTM4 и GSTM5. Ген GSTM локализован в хромосоме 1 (локус 1р13.3). GSTM1 экспрессируется в печени, почках, надпочечниках, желудке; слабая экспрессия данного изофермента найдена в скелетных мышцах, миокарде. GSTM1 не экспрессируется в плодной печени, фибробластах, эритроцитах, лимфоцитах и тромбоцитах. GSTM2 («мышечная» GSTM) экспрессируется во всех вышеперечисленных тканях (особенно в мышечной), кроме фибробластов, эритроцитов, лимфоцитов, тромбоцитов и фетальной печени. Экспрессия GSTM3 («мозговая» GSTM) осуществляется во всех тканях организма, особенно в ЦНС. Важная роль в инактивации канцерогенов принадлежит GSTM1. Косвенным подтверждением этого считают достоверное увеличение частоты злокачественных заболеваний среди носителей нулевых аллелей гена GSTM1, у которых отсутствует экспрессия GSTM1. Harada и соавт. (1987), изучив образцы печени, изъятые у 168 трупов, обнаружили, что нулевая аллель гена GSTM1 достоверно чаще встречается у больных с гепатокарциномой. Board и соавт. (1987) впервые выдвинули гипотезу: в организме носителей нулевых аллелей GSTM1 не происходит инактивация некоторых электрофильных канцерогенов. По данным Board и соавт. (1990), распро- странённость нулевой аллели GSTM1 среди европейского населения составляет 40-45%, в то время как у представителей негроидной расы - 60%. Существуют данные о более высокой частоте рака лёгких у носителей нулевой аллели GSTM1. Как показали Zhong и соавт. (1993),
70% больных раком ободочной кишки - носители нулевой аллели GSTM1. Другой изофермент GST, принадлежащий к классу π, - GSTР1 (локализуется главным образом в печени и структурах гематоэнцефалического барьера) участвует в инактивации пестицидов и гербицидов, широко используемых в сельском хозяйстве.
5.5. ФАКТОРЫ, ВЛИЯЮЩИЕ НА БИОТРАНСФОРМАЦИЮ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Генетические факторы, влияющие на систему биотрансформации и транспортёры лекарственных средств
Генетические факторы, представляющие однонуклеотидные полиморфизмы генов, кодирующих ферменты биотрансформации и транс- портёры ЛС, могут в значительной степени влиять на фармакокинетику ЛС. Межиндивидуальные различия в скорости метаболизма ЛС, которые можно оценить по отношению концентрации ЛС-субстрата к концентрации его метаболита в плазме крови или в моче (метаболическое отношение), позволяют выделить группы индивидуумов, различающиеся по активности того или иного изофермента метаболизма.
«Экстенсивные» метаболизаторы (extensive metabolism, ЕМ) - лица с «нормальной» скоростью метаболизма определённых ЛС, как правило, гомозиготы по «дикой» аллели гена соответствующего фермента. К группе «экстенсивных» метаболизаторов принадлежит большинство населения.
«Медленные» метаболизаторы (poor metabolism, РМ) - лица со сниженной скоростью метаболизма определённых ЛС, как правило, гомозиготы (при аутосомно-рецессивном типе наследования) или гетерозиготы (при аутосомно-доминантном типе наследования) по «медленной» аллели гена соответствующего фермента. У этих индивидуумов происходит синтез «дефектного» фермента, либо вообще отсутствует синтез фермента метаболизма. В результате происходит снижение ферментативной активности. Нередко обнаруживают полное отсутствие ферментативной активности. У этой категории лиц регистрируют высокие показатели отношения концентрации ЛС к концентрации его метаболита. Следовательно, у «медленных» метаболизаторов ЛС накапливается в организме в высоких концентрациях; это приводит к разви-
Тию выраженных нежелательных лекарственных реакций, вплоть до интоксикации. Именно поэтому таким пациентам (медленным метаболизаторам) необходимо выполнять тщательный подбор дозы ЛС. «Медленным» метаболизаторам назначают меньшие дозы ЛС, чем «активным». «Сверхактивные», или «быстрые» метаболизаторы (ultraextensive metabolism, UM) - лица с повышенной скоростью метаболизма определённых ЛС, как правило, гомозиготы (при аутосомнорецессивном типе наследования) или гетерозиготы (при аутосомно-доминантном типе наследования) по «быстрой» аллели гена соответствующего фермента или, что наблюдают чаще, несущие копии функциональных аллелей. У этой категории лиц регистрируют низкие значения отношения концентрации ЛС к концентрации его метаболита. В результате концентрация ЛС в плазме крови недостаточна для достижения терапевтического эффекта. Таким пациентам («сверхактивным» метаболизаторам) назначают более высокие дозы ЛС, чем «активным» метаболизаторам. Если присутствует генетический полиморфизм того или иного фермента биотрансформации, то распределение индивидуумов по скорости метаболизма ЛС-субстратов данного фермента приобретает бимодальный (если существует 2 типа метаболизаторов) или тримодальный (если существует 3 типа метаболизаторов) характер.
Полиморфизм характерен и для генов, кодирующих транспортёры ЛС, при этом фармакокинетика ЛС может изменяться в зависимости от функции данного транспортёра. Клиническое значение наиболее значимых ферментов биотрансформации и транспортёров рассмотрено ниже.
Индукция и ингибирование системы биотрансформации и транспортёров
Под индукцией фермента биотрансформации или транспортёра понимают абсолютное увеличение его количества и (или) активности вследствие воздействия определённого химического агента, в частности, ЛС. В случае с ферментами биотрансформации это сопровождается гипертрофией ЭПР. Индукции могут подвергаться как ферменты I фазы (изоферменты цитохрома Р-450) и II фазы биотрансформации (УДФ-глюкуронилтрансфераза и др.), так и транспортёры ЛС (гликопротеин-Р, транспортёры органических анионов и катионов). ЛС, индуцирующие ферменты биотрансформации и транспортёры, не обладают очевидным структурным сходством, однако для них харак-
терны некоторые общие признаки. Такие вещества растворимы в жирах (липофильны); служат субстратами ферментов (которые они индуцируют) и имеют, чаще всего, длительный период полувыведения. Индукция ферментов биотрансформации ведёт к ускорению биотрансформации и, как правило, к снижению фармакологической активности, а следовательно, и к эффективности совместно применяемых с индуктором ЛС. Индукция транспортёров ЛС может приводить к различным изменениям концентрации ЛС в плазме крови, в зависимости от функций данного транспортёра. Различные субстраты способны индуцировать ферменты биотрансформации ЛС и транспортёры ЛС с неодинаковыми молекулярной массой, субстратной специфичностью, иммунохимическими и спектральными характеристиками. Кроме того, существуют значительные межиндивидуальные различия в интенсивности индукции ферментов биотрансформации и транспортёров ЛС. Один и тот же индуктор может повышать активность фермента или транспортёра у различных индивидуумов в 15-100 раз.
Основные типы индукции
«Фенобарбиталовый» тип индукции - непосредственное воздействие молекулы-индуктора на регуляторную область гена; это приводит к индукции фермента биотрансформации или транс- портёра ЛС. Такой механизм наиболее характерен для аутоиндукции. Под аутоиндукцией понимают увеличение активности фермента, метаболизирующего ксенобиотик, под действием самого ксенобиотика. Аутоиндукцию рассматривают как адаптивный механизм, выработанный в процессе эволюции для инактивации ксенобиотиков, в том числе растительного происхождения. Так, аутоиндукцией по отношению к цитохромам подсемейства IIВ обладает фитонцид чеснока - диалил сульфид. Барбитураты (индукторы изоферментов цитохрома Р-450 3А4, 2С9, подсемейства IIВ) - типичные аутоиндукторы (среди лекарственных веществ). Именно поэтому данный тип индукции получил название «фенобарбиталовый».
«Рифампицин-дексаметазоновый» тип - индукция изоферментов цитохрома Р-450 1А1, 3А4, 2В6 и гликопротеина-Р опосредована взаимодействием молекулы индуктора со специфическими рецепторами, их относят к классу белков-регуляторов транскрипции: прегнан-Х-рецептор (PXR), Ah-рецептор, CAR-рецеп- тор. Соединяясь с этими рецепторами, ЛС-индукторы образуют комплекс, который, проникая в ядро клетки, воздействует на
Регуляторную область гена. В результате происходит индукция фермента биотрансформации ЛС, или транспортёра. По этому механизму рифампины, глюкокортикоиды, препараты зверобоя и некоторые другие вещества индуцируют изоферменты цитохрома Р-450 и гликопротеин-Р. «Этаноловый» тип - стабилизация молекулы фермента биотрансформации ЛС вследствие образования комплекса с некоторыми ксенобиотиками (этанол, ацетон). Например, этанол индуцирует изофермент 2Е1 цитохрома Р-450 на всех этапах его образования: от транскрипции до трансляции. Полагают, что стабилизирующий эффект этанола связан с его способностью активировать систему фосфорилирования в гепатоцитах через ЦАМФ. По данному механизму изониазид индуцирует изофермент 2Е1 цитохрома Р-450. С «этаноловым» механизмом связывают процесс индукции изофермента 2Е1 цитохрома Р-450 при голодании и сахарном диабете, в данном случае в качестве индукторов изофермента 2Е1 цитохрома Р-450 выступают кетоновые тела. Индукция ведёт к ускорению биотрансформации ЛС-субстратов соответствующих ферментов, и, как правило, к снижению их фармакологической активности. Среди индукторов наиболее часто применяют в клинической практике рифампицин (индуктор изоферментов 1А2, 2С9, 2С19, 3A4, 3А5, 3А6, 3А7 цитохрома Р-450; гликопротеин-Р) и барбитураты (индукторы изоферментов 1A2, 2В6, 2C8, 2С9, 2С19, 3A4, 3А5, 3А6, 3А7 цитохрома Р-450). Для развития индуцирующего эффекта барбитуратов требуется несколько недель. В отличие от барбитуратов, рифампицин, как индуктор, действует быстро. Эффект рифампицина можно обнаружить уже через 2-4 дня. Максимальный эффект препарата регистрируют через 6-10 дней. Индукция ферментов, или транспортёров ЛС, вызванная рифампицином и барбитуратами, иногда приводит к снижению фармакологической эффективности непрямых антикоагулянтов (варфарина, аценокумарола), циклоспорина, глюкокортикоидов, кетоконазола, теофиллина, хинидина, дигоксина, фексофенадина и верапамила (это требует коррекции режима дозирования данных ЛС т.е. увеличения дозы). Следует подчеркнуть, что при отмене индуктора ферментов биотрансформации ЛС дозу сочетаемого ЛС следует снижать, так как происходит увеличение его концентрации в плазме крови. Примером такого взаимодействия можно считать комбинацию антикоагулянтов непрямого действия и фенобарбитала. Как показали исследования, в 14% случаев кровотечения при лечении
непрямыми антикоагулянтами развиваются вследствие отмены ЛС, индуцирующих ферменты биотрансформации.
Некоторые соединения могут ингибировать активность ферментов биотрансформации и транспортёров ЛС. Причём при снижении активности ферментов, метаболизирующих ЛС, возможно развитие побочных эффектов, связанных с длительной циркуляцией этих соединений в организме. Ингибирование транспортёров ЛС может приводить к различным изменениям концентрации ЛС в плазме крови в зависимости от функций данного транспортёра. Некоторые лекарственные вещества способны ингибировать как ферменты I фазы биотрансформации (изоферменты цитохрома Р-450) и II фазы биотрансформации (N-ацетилтрансфераза и др.), так и транспортёры ЛС.
Основные механизмы ингибирования
Связывание с регуляторной областью гена фермента биотрансформации или транспортёра ЛС. По данному механизму происходит ингибирование ферментов биотрансформации ЛС под действием большого количества препарата (циметидин, флуоксетин, омепразол, фторхинолоны, макролиды, сульфаниламиды и т.д.).
Некоторые препараты, обладающие высоким аффинитетом (сродством) к определённым изоферферментам цитохрома Р-450 (верапамил, нифедипин, исрадипин, хинидин), ингибируют биотрансформацию ЛС с более низким аффинитетом к этим изоферментам. Подобный механизм называют конкурентным метаболическим взаимодействием.
Прямая инактивация изоферментов цитохрома Р-450 (гастоден р). Угнетение взаимодействия цитохрома Р-450 с НАДФ-Н-цитохром Р-450 редуктазой (фумарокумарины сока грейпфрута и лайма).
Снижение активности ферментов биотрансформации ЛС под действием соответствующих ингибиторов ведёт к повышению концентрации в плазме крови этих ЛС (субстратов для ферментов). При этом происходит удлинение периода полувыведения лекарственных веществ. Всё это служит причиной развития побочных эффектов. Некоторые ингибиторы влияют на несколько изоферментов биотрансформации одновременно. Для угнетения нескольких изоформ ферментов могут потребоваться большие концентрации ингибитора. Так, флуконазол (противогрибковый препарат) в дозе 100 мг в сутки угнетает активность изофермента 2С9 цитохрома Р-450. При повышении дозы данного ЛС до 400 мг отмечают также угнетение
активности изофермента 3А4. Кроме того, чем выше доза ингибитора, тем быстрее развивается (и тем выше) его эффект. Ингибирование вообще развивается быстрее, чем индукция, обычно его можно зарегистрировать уже через 24 ч с момента назначения ингибиторов. На скорость ингибирования активности фермента влияет также путь введения ЛС-ингибитора: если ингибитор вводят внутривенно, то процесс взаимодействия произойдёт быстрее.
Ингибиторами и индукторами ферментов биотрансформации и транспортёров ЛС могут служить не только ЛС, но и фруктовые соки (табл. 5-10), и фитопрепараты (приложение 2) - всё это имеет клиническое значение при применении ЛС, выполняющих функции субстратов для данных ферментов и транспортёров.
Таблица 5-10. Влияние фруктовых соков на активность системы биотрансформации и транспортёров лекарственных средств
 5.6. ЭКСТРАГЕПАТИЧЕСКАЯ БИОТРАНСФОРМАЦИЯ
5.6. ЭКСТРАГЕПАТИЧЕСКАЯ БИОТРАНСФОРМАЦИЯ
Роль кишечника в биотрансформации лекарственных средств
Кишечник считают вторым по значимости органом (после печени), выполняющим биотрансформацию ЛС. В стенке кишечника осуществляются как реакции I фазы, так и реакции II фазы биотрансформации. Биотрансформация ЛС в стенке кишечника имеет большое значение в эффекте первого прохождения (пресистемной биотрансформации). Уже доказана существенная роль биотрансформации в стенке кишечника в эффекте первого прохождения таких ЛС, как циклоспорин А, нифедипин, мидазолам, верапамил.
Ферменты I фазы биотрансформации лекарственных средств в стенке кишечника
Среди ферментов I фазы биотрансформации ЛС, в стенке кишечника в основном локализованы изоферменты цитохрома Р-450. Среднее содержание изоферментов цитохрома Р-450 в стенке кишечника человека составляет 20 пмоль/мг микросомального белка (в печени - 300 пмоль/мг микросомального белка). Установлена чёткая закономерность: содержание изоферментов цитохрома Р-450 уменьшается от проксимальных отделов кишечника к дистальным (табл. 5-11). Кроме того, содержание изоферментов цитохрома Р-450 максимально на вершине ворсинок кишечника и минимально - в криптах. Преобладающийвкишечникеизоферментцитохрома Р-450 - CYP3А4 составляет 70% от всех изоферментов цитохрома Р-450 кишечника. По данным разных авторов, содержание CYP3А4 в стенке кишечника варьирует, что объясняют межиндивидульными различиями цитохрома Р-450. Также имеют значение и способы очистки энтероцитов.
Таблица 5-11. Содержание изофермента 3А4 цитохрома Р-450 в стенке кишечника и печени человека
 В
стенке кишечника идентифицированы также другие изоферменты: CYP2C9 и
CYP2D6. Однако, по сравнению с печенью, содержание указанных ферментов в
стенке кишечника незначительно (в 100-200 раз меньше). Проведённые
исследования продемонстрировали незначительную, по сравнению с печенью,
метаболическую активность изоферментов цитохрома Р-450 стенки кишечника
(табл. 5-12). Как показали исследования, посвященные изучению индукции
изоферментов цитохрома Р-450 стенки кишечника, индуцибельность
изоферментов стенки кишечника ниже, чем у изоферментов цитохрома Р-450
печени.
В
стенке кишечника идентифицированы также другие изоферменты: CYP2C9 и
CYP2D6. Однако, по сравнению с печенью, содержание указанных ферментов в
стенке кишечника незначительно (в 100-200 раз меньше). Проведённые
исследования продемонстрировали незначительную, по сравнению с печенью,
метаболическую активность изоферментов цитохрома Р-450 стенки кишечника
(табл. 5-12). Как показали исследования, посвященные изучению индукции
изоферментов цитохрома Р-450 стенки кишечника, индуцибельность
изоферментов стенки кишечника ниже, чем у изоферментов цитохрома Р-450
печени.
Таблица 5-12. Метаболическая активность изоферментов цитохромов Р-450 стенки кишечника и печени
 Ферменты II фазы биотрансформации лекарственных средств в стенке кишечника
Ферменты II фазы биотрансформации лекарственных средств в стенке кишечника
УДФ-глюкуронилтрансфераза и сульфотрансфераза - наиболее хорошо изученные ферменты II фазы биотрансформации ЛС, расположенные в стенке кишечника. Распределение этих ферментов в кишечнике аналогично изоферментам цитохрома Р-450. Cappiello и соавт. (1991) изучали активность УДФ-глюкуронилтрансферазы в стенке кишечника и печени человека по метаболическому клиренсу 1-нафтола, морфина и этинилэстрадиола (табл. 5-13). Как показали исследования, метаболическая активность УДФ-глюкуронилтрансферазы стенки кишечника ниже УДФ-глюкуронилтрансферазы печени. Подобная закономерность характерна и для глюкуронирования билирубина.
Таблица 5-13. Метаболическая активность УДФ-глюкуронилтрансферазы в стенке кишечника и в печени
 Cappiello
и соавт. (1987) изучали также активность сульфотрансферазы стенки
кишечника и печени по метаболическому клиренсу 2-нафтола. Полученные
данные свидетельствуют о наличии различий показателей метаболического
клиренса (причём клиренс 2-нафтола в стенке кишечника ниже, чем в
печени). В подвздошной кишке величина данного показателя составляет 0,64
нмоль/(минхмг), в сигмовидной кишке - 0,4 нмоль/(минхмг), в печени -
1,82 нмоль/(минхмг). Однако существуют препараты, сульфатирование
которых происходит в основном в стенке кишечника. К ним относят,
например, β 2 -адреномиметики: тербуталин и изопреналин (табл. 5-14).
Cappiello
и соавт. (1987) изучали также активность сульфотрансферазы стенки
кишечника и печени по метаболическому клиренсу 2-нафтола. Полученные
данные свидетельствуют о наличии различий показателей метаболического
клиренса (причём клиренс 2-нафтола в стенке кишечника ниже, чем в
печени). В подвздошной кишке величина данного показателя составляет 0,64
нмоль/(минхмг), в сигмовидной кишке - 0,4 нмоль/(минхмг), в печени -
1,82 нмоль/(минхмг). Однако существуют препараты, сульфатирование
которых происходит в основном в стенке кишечника. К ним относят,
например, β 2 -адреномиметики: тербуталин и изопреналин (табл. 5-14).
Таким образом, несмотря на определённый вклад в биотрансформацию лекарственных веществ, стенка кишечника по своей метаболической способности значительно уступает печени.
Таблица 5-14. Метаболический клиренс тербуталина и изопреналина в стенке кишечника и печени
 Роль лёгких в биотрансформации лекарственных средств
Роль лёгких в биотрансформации лекарственных средств
В лёгких человека присутствуют как ферменты I фазы биотрансформации (изоферменты цитохрома Р-450), так и ферменты II фазы
(эпоксидгидролаза, УДФ-глюкуронилтрансфераза и др.). В лёгочной ткани человека удалось идентифицировать различные изоферменты цитохрома Р-450: CYP1A1, CYP1B1, CYP2А, CYP2A10, CYP2A11, CYP2В, CYP2E1, CYP2F1, CYP2F3. Общее содержание цитохрома Р-450 в лёгких человека составляет 0,01 нмоль/мг микросомального белка (это в 10 раз меньше, чем в печени). Существуют изоферменты цитохрома Р-450, которые экспрессируются преимущественно в лёг- ких. К ним относят CYP1A1 (найден у человека), CYP2В (у мыши), CYP4В1 (у крысы) и CYP4В2 (у крупного рогатого скота). Эти изоферменты имеют большое значение в биологической активации ряда канцерогенов и пульмонотоксичных соединений. Информация об участии CYP1A1 в биологической активации ПАУ изложена выше. У мышей окисление бутилированного гидрокситолуена изоферментом CYP2В приводит к образованию пневмотоксичного электрофильного метаболита. Изоферменты CYP4В1 крыс и CYP4В2 крупного рогатого скота способствуют биологической активации 4-ипоменола (4-ипоме- нол - сильнодействующий пневмотоксичный фуранотерпеноид грибка сырого картофеля). Именно 4-импоменол стал причиной массового падежа крупного рогатого скота в 70-е годы в США и Англии. При этом 4-ипоменол, окисленный изоферментом CYP4В2, вызывал интерстициальную пневмонию, приводившую к летальному исходу.
Таким образом, экспрессия в лёгких специфичных изоферментов объясняет избирательную пульмонотоксичность некоторых ксенобиотиков. Несмотря на наличие в лёгких и других отделах дыхательных путей ферментов, их роль в биотрансформации лекарственных веществ ничтожна. В таблице приведены ферменты биотрансформации ЛС, обнаруженные в дыхательных путях человека (табл. 5-15). Определение локализации ферментов биотрансформации в дыхательных путях затруднено из-за использования в исследованиях гомогенизата лёгких.
Таблица 5-15. Ферменты биотрансформации, обнаруженные в дыхательных путях человека
 Роль почек в биотрансформации лекарственных средств
Роль почек в биотрансформации лекарственных средств
Исследования, выполненные в течение последних 20 лет, показали, что почки принимают участие в метаболизме ксенобиотиков и лекарственных веществ. При этом, как правило, происходит снижение биологической и фармакологической активности, однако в некоторых случаях возможен и процесс биологической активации (в частности, биоактивации канцерогенов).
В почках обнаружены как ферменты I фазы биотрансформации, так и ферменты II фазы. Причём ферменты биотрансформации локализованы и в корковом, и в мозговом веществе почек (табл. 5-16). Однако, как показали исследования, большее количество изоферментов цитохрома Р-450 содержит именно корковый слой почек, а не мозговой. Максимальное содержание изоферментов цитохрома Р-450 обнаружили в проксимальных почечных канальцах. Так, почки содержат изофермент CYP1A1, ранее считавшийся специфичным для лёгких, и CYP1A2. Причём указанные изоферменты в почках подвергаются индукции ПАУ (например, β-нафтовлавоном, 2-ацетиламино- флурином) так же, как и в печени. В почках обнаружили активность CYP2B1, в частности, описали окисление парацетамола (ацетаминофена ♠) в почках под действием этого изофермента. Позднее продемонстрировали, что именно образование токсичного метаболита N-ацетибензахинонимина в почках под действием CYP2E1 (по аналогии с печенью) - основная причина нефротоксического действия данного препарата. При совместном применении парацетамола с индукторами CYP2E1 (этанолом, тестостероном и т.д.) риск поражения почек возрастает в несколько раз. Активность CYP3A4 в почках регистрируют не всегда (только в80% случаев). Следует отметить: вклад изоферментов цитохрома Р-450 почек в биотрансформацию лекарственных веществ скромен и, видимо, в большинстве случаев не имеет клинического значения. Однако для некоторых ЛС биохимическое преобразование в почках - основной путь биотрансформации. Как показали исследования, тропизетрон р (противорвотное ЛС), главным образом, окисляется в почках под действием изоферментов CYP1A2 и CYP2E1.
Среди ферментов II фазы биотрансформации в почках наиболее часто определяют УДФ-глюкуронилтрансферазу и β-лиазу. Следует отметить, что активность β-лиазы в почках выше, чем в печени. Обнаружение этой особенности позволило разработать некоторые «пролекарства», при активации которых образуются активные мета-
болиты, селективно действующие на почки. Так, создали цитостатический препарат для лечения хронического гломерулонефрита - S-(6-пуринил)-L-цистеин. Это соединение - изначально неактивное, в почках под действием β-лиазы превращается в активный 6-мер- каптопурин. Таким образом, 6-меркуптопурин производит эффект исключительно в почках; это значительно снижает частоту и выраженность нежелательных лекарственных реакций.
Глюкуронированию в почках подвергаются такие ЛС, как парацетамол (ацетаминофен ♠), зидовудин (азидотимидин ♠), морфин, сульфаметазон р, фуросемид (лазикс ♠) и хлорамфеникол (левомицетин ♠).
Таблица 5-16. Распределение ферментов биотрансформации лекарственных средств в почках (Lohr и соавт., 1998)
 * - содержание фермента достоверно выше.
* - содержание фермента достоверно выше.
Литература
Кукес В.Г. Метаболизм лекарственных средств: клинико-фармакологические аспекты. - М.: Реафарм, 2004. - С. 113-120.
Середенин С.Б. Лекции по фармакогенетике. - М.: МИА, 2004. -
Diasio R.B., Beavers T.L., Carpenter J.T. Familial deficiency of dihydropyrimidine dehydrogenase: biochemical basis for familial pyrimidinemia and severe 5-fluorouracil-induced toxicity // J. Clin. Invest. - 1988. - Vol. 81. -
Lemoine A., Daniel A., Dennison A., Kiffel L. et al. FK 506 renal toxicity and lack of detectable cytochrome P-450 3A in the liver graft of a patient undergoing liver transplantation // Hepatology. - 1994. - Vol. 20. - P. 1472-1477.
Lewis D.F.V., Dickins M., Eddershaw P.J. et al. Cytochrome-P450 Substrate Specificities, Substrate structural Templates and Enzyme Active Site Geometries // Drug Metabol. Drug Interact. - 1999. - Vol. 15. - P. 1-51.
Как уже говорилось, длительное применение фенобарбитала приводит к изменению пигментного метаболизма печени. Многие другие лекарственные препараты, лекарственные вещества, и продукты могут повышать активность цитохрома Р-450 и соответственно, изменять время полужизни лекарства - объекта. Примеры факторов, могущих вызывать клинически значимые взаимодействия: курение сигарет, хронический алкоголизм, прием рифампицина и некоторых противосудорожных лекарственных средств (барбитуратов, фенитоина, карбамазепина). Быстрота развития и обратимость индукции ферментов зависит от индуктора и скорости синтеза новых ферментов. Этот адаптационный процесс относительно медленный и может занимать от нескольких дней до нескольких месяцев. Он также может ускорять метаболизм самого индуктора - это ауто-индукция.
Два препарата - индуктора широко применяются в практике отделения интенсивной терапии - это рифампицин и фенобарбитал. В отличие от фенобарбитала, развитие действия которого как индуктора требует по крайней мере, нескольких недель, рифампицин как индуктор действует быстро и такое его действие может быть обнаружено уже через 2-4 дня и достигать своего максимума через 6-10 дней. Индукция ферментов, вызванная рифампицином, может приводить к более выраженным взаимодействиям с варфарином, циклоспорином, глюкокортикоидами, кетоконазолм, теофиллином, хинидином, дигитоксином и верапамилом, что требует пристального наблюдения за пациентом и частую коррекцию доз препарата - объекта. Цитохром может также индуцироваться противосудорожными препаратами, рифампицином, глюкокортикоидами и некоторыми антибиотиками из группы макролидов. Это также может приводить к появлению лекарственных взаимодействий.
ИНГИБИРОВАНИЕ МИКРОСОМАЛЬНЫХ ФЕРМЕНТОВ ПЕЧЕНИ
Ингибирование ферментов группы цитохромов - это самый частый механизм, ответственный за возникновение лекарственных взаимодействий в практике отделений интенсивной терапии. Если вещество угнетает цитохром, то оно изменяет и метаболизм препарата – объекта. Этот эффект заключается в удлинении времени полужизни лекарства-объекта и соответственно, повышать его концентрацию. Некоторые ингибиторы влияют сразу на несколько изоформ ферментов, это например макролидный антибиотик эритромицин. Для угнетения сразу нескольких изоформ ферментов могут потребоваться большие концентрации ингибитора. Флюконазол угнетает активность цитохрома 2-9 в дозе 100 мг в день, но если дозу повысить до 400 мг, то будет угнетаться активность цитохрома 3-4. Че6м выше доза ингибитора, тем быстрее наступает его действие и тем больше оно выражено. Ингибирование вообще развивается быстрее, чем индукция, обычно его можно зарегистрировать уже через 24 часа от момента назначения ингибиторов. Время развития максимального угнетения активности ферментов зависит как от самого ингибитора, так и от лекарства - объекта. Поскольку изоформы фермента отличаются по генам, воздействию окружающей Среды, возраста человека, имеющихся заболеваний при воздействии одного и того же ингибитора степень угнетения активности фермента у разных пациентов может варьировать. Примерно 5% всех жителей США имеют генетический дефицит изоформы цитохрома 2-6, который участвует в метаболизме бета - блокаторов, нейролептиков и антидепрессантов. У этих пациентов не бывает ингибирования этой формы фермента хинидином, что наблюдается у всей остальной популяции. Ингибирование изоформы 3А встречается часто и вызывается большим количеством препаратов, часто применяющихся в практике отделения интенсивной терапии. Это могут быть: кетоконазол, флюконазол, циклоспорин, ритонавир, дилтиазем, нифедипин, никардипин, флуоксетин, хинидин, верапамил и эритромицин. Это быстро обратимые ингибиторы. Путь введения лекарственного препарата влияет на скорость развития и выраженность угнетения активности фермента. Например, если препарат вводится внутривенно, то взаимодействие разовьется быстрее.
ИЗМЕНЕНИЯ ВЫДЕЛЕНИЯ
Высокополярные вещества или растворимые в воде метаболиты жирорастворимых веществ выделяются почками, однако нельзя забывать, что в меньшей степени они выделяются печенью, с потом и грудным молоком. Водорастворимые вещества, находящиеся в крови, могут выделяться с мочой путем пассивной клубочковой фильтрации, активной канальцевой секреции или путем блокады активной, или чаще пассивной канальцевой реабсорбции.
Препараты, снижающие скорость клубочковой фильтрации (СКФ) обычно снижают фильтрационное давление либо вследствие уменьшения внутрисосудистого объема, либо снижения артериального давления, либо сосудистого тонуса почечных артерий. Снижение СКФ препаратом – объектом, например, фуросемидом, может, в свою очередь, ограничить пассивную фильтрацию лекарства – мишени, например, аминогликозидов, что приводит к повышению их концентрации в крови. В это же самое время нефротоксичные препараты, такие, как те же аминогликозиды, могут уменьшать количество функционирующих нефронов и снижать СКФ, что приводит к накоплению в организме других препаратов, таких, как дигоксин, которые выводятся практически только почками. Хотя это – непрямое взаимодействие, оно имеет огромное значение для пациентов ОИТ, и его можно избежать путем тщательного подбора доз препаратов.
Многие растворимые в воде органические кислоты активно секретируются в первую очередь в проксимальной части канальца. Активный энергозависимый транспорт органических анионов и катионов – это уникальная система. Ингибирование этих специфических систем лекарственными препаратами могут привести к накоплению препарата – мишени. Конкуренция за транспортные системы эндогенными (например, мочевая кислота) и экзогенными веществами (пенициллинами, пробенецидом, нестероидными противовспалительными препаратами, метотрексатом, сульфаниламидами и цефалоспоринами) может привести к развитию клинически значимых лекарственных взаимодействий. Примером такого взаимодействия можно проследить на примере хинидина и дигоксина. Как уже говорилось ранее, изменения метаболизма дигоксина в органах и тканях могут возникать при одновременном назначении этих двух препаратов. Происходит относительное изменение объема распределения препарата и одновременно взаимодействие другого рода – конкуренция за транспортные системы в почках. Снижение выведения дигоксина почками и одновременное изменение метаболизма препарата могут привести к удвоению концентрации препарата в крови. Этот тип лекарственного взаимодействия в прошлом использовался в терапевтических целях. Препарат пробенецид использовался для повышения концентрации в организме пенициллина. Реабсорбция отфильтрованных и выделенных лекарственных препаратов происходит в дистальной части канальца и в собирательных трубочках. На этот процесс влияют изменения концентрации препаратов, объемная скорость диуреза, и рН мочи по сравнению с таковым для сыворотки крови. При изменении рН мочи в дистальной части канальцев изменяется транспорт органических оснований и кислот. Эти ионизированные вещества не проходят через мембрану канальцев почек напрямую, что увеличивает скорость их экскреции. Важный и клинически значимый пример таких взаимодействий – это использование бикарбоната натрия для ощелачивания мочи и ускорения выведения аспирина или салицилатов при отравлении этими веществами. Поскольку рН изменяется в логарифмической зависимости, при возрастании этого показателя на одну единицу приводит к ускорению почечной экскреции в десять раз. Урикозурический эффект пробенецида связан с блокированием препаратом активной реабсорбции эндогенной мочевой кислоты из проксимальной части почечных канальцев.
Аспирин также угнетает реабсорбцию мочевой кислоты, однако если его применять совместно с пробенецидом, то аспирин ликвидирует урикозурический эффект последнего. Непрямые лекарственные взаимодействия могут влиять как на механизмы экскреции, так и реабсорбции. Литий реабсорбируется в почках вместе с натрием, по одному и тому же механизму. При уменьшении внутрисосудистого объема, например, при использовании тиазидовых диуретиков, компенсаторно увеличивается реабсорбция натрия и лития в проксимальных канальцах, что в некоторых ситуациях может привести к накоплению в организме токсичных количеств лития.
Биотрансформация (метаболизм) - изменение химической структуры лекарственных веществ и их физикохимических свойств под действием ферментов организма. Основной направленностью этого процесса является превращение липофильных веществ, которые легко реабсорбируются в почечных канальцах, в гидрофильные полярные соединения, которые быстро выводятся почками (не реабсорбируются в почечных канальцах). В процессе биотрансформации, как правило, происходит снижение активности (токсичности) исходных веществ.
Биотрансформация липофильных ЛВ в основном происходит под влиянием ферментов печени, локализованных в мембране эндоплазматического ретикулума гепатоцитов. Эти ферменты называются микросомальными, потому что
они оказываются связанными с мелкими субклеточными фрагментами гладкого эндоплазматического ретикулума (микросомами), которые образуются при гомогенизации печеночной ткани или тканей других органов и могут быть выделены центрифугированием (осаждаютсяв так называемой «микросомальной» фракции).
В плазме крови, а также в печени, кишечнике, легких, коже, слизистых оболочках и других тканях имеются немикросомальные ферменты, локализованные в цитозоле или митохондриях. Эти ферменты могут участвовать в метаболизме гидрофильных веществ.
Различают два основных вида метаболизма лекарственных веществ (этапы):
несинтетические реакции (метаболическая трансформация);
синтетические реакции (конъюгация).
биотрансформация (реакции метаболизма 1-й фазы), происходит под действием ферментов — окисление, восстановление, гидролиз.
конъюгация (реакции метаболизма 2-й фазы), при которой происходит присоединение к молекуле вещества остатков других молекул (глюкуроновой, серной кислот, алкильных радикалов), с образованием неактивного комплекса, легко выводимого из организма с мочой или калом.
Лекарственные вещества могут подвергаться или метаболической биотрансформации (при этом образуются вещества, называемые метаболитами), или конъюгации (образуются конъюгаты). Но большинство Л В сначала метаболизируется при участии несинтетических реакций с образованием реакционноспособных метаболитов, которые затем вступают в реакции конъюгации.
Кметаболической трансформации относятся следующие реакции: окисление, восстановление, гидролиз. Многие липофильные соединения подвергаются окислению в печени под влиянием микросомальной системы ферментов, известных как оксидазы смешанных функций, или монооксигеназы. Основными компонентами этой системы являются цитохром Р450 редуктаза и цитохром Р450 гемопротеин, который связывает молекулы лекарственного вещества и кислород в своем активном центре. Реакция протекает при участии НАДФН. В результате происходит присоединение одного атома кислорода к субстрату (лекарственному веществу) с образованием гидроксильной группы (реакция гидроксилирования).
Под действием некоторых лекарственных веществ (фенобарбитал, рифампицин, карбамазепин, гризеофульвин) может происходить индукция (увеличение скорости синтеза) микросомальных ферментов печени. В результате при одновременном назначении с индукторами микросомальных ферментов других препаратов (например, глюкокортикоидов, пероральных контрацептивов) повышается скорость метаболизма последних и снижается их действие. В некоторых случаях может увеличиваться скорость метаболизма самого индуктора, вследствие чего уменьшаются его фармакологические эффекты (карбамазепин).
Некоторые лекарственные вещества (циметидин, хлорамфеникол, кетоконазол, этанол) снижают активность (ингибиторы) метаболизирующих ферментов. Например, циметидин является ингибитором микросомального окисления и, замедляя метаболизм варфарина, может повысить его антикоагулянтный эффект и спровоцировать кровотечение. Известны вещества (фуранокумарины), содержащиеся в грейпфрутовом соке, которые угнетают метаболизм таких лекарственных веществ, как циклоспорин, мидазолам, алпразолам и, следовательно, усиливают их действие. При одновременном применении лекарственных веществ с индукторами или ингибиторами метаболизма необходимо корректировать назначаемые дозы этих веществ.
12. Пути выведения лекарственных веществ из организма, значение, понятие о квоте элиминации, периоде полувыведения (Т 1/2) и общем плазматическом клиренсе. Зависимость действия лекарственных веществ от пути выведения, примеры.
Выведение неизмененного лекарственного вещества или его метаболитов осуществляется всеми экскреторными органами (почками, кишечником, легкими, молочными, слюнными, потовыми железами и др.).
Основным органом выведения лекарств из организма являются почки. Выведение лекарств почками происходит путем фильтрации и с помощью активного или пассивного транспорта. Липоидорастворимые вещества легко фильтруются в клубочках, но в канальцах они вновь пассивно всасываются. Препараты, слабо растворимые в липоидах, быстрее выводятся с мочой, поскольку они плохо реабсорбируются в почечных канальцах. Кислая реакция мочи способствует выведению щелочных соединений и затрудняет экскрецию кислых. Поэтому при интоксикации лекарствами кислого характера (например, барбитуратами) применяют натрия гидрокарбонат или другие щелочные соединения, а при интоксикации алкалоидами, имеющими щелочной характер, используют аммония хлорид. Ускорить выведение лекарств из организма можно и назначением сильнодействующих мочегонных средств, например, осмотических диуретиков или фуросемида, на фоне введения в организм большого количества жидкости (форсированный диурез). Выведение из организма оснований и кислот происходит путем активного транспорта. Этот процесс идет с затратой энергии и с помощью определенных ферментных систем-переносчиков. Создавая конкуренцию за переносчик каким-либо веществом, можно замедлить выведение лекарства (например, этамид ипенициллин секретируются с помощью одних и тех же ферментных систем, поэтому этамидзамедляет выведение пенициллина).
Препараты, плохо всасывающиеся из желудочно-кишечного тракта, выводятся кишечником и применяются при гастритах, энтеритах и колитах (например, вяжущие средства, некоторыеантибиотики используемые при кишечных инфекциях). Кроме того, из печеночных клеток лекарства и их метаболиты попадают в желчь и с нею поступают в кишечник, откуда либо повторно всасываются, доставляются в печень, а затем с желчью в кишечник (кишечно- печеночная циркуляция), либо выводятся из организма с каловыми массами. Не исключается и прямая секреция ряда лекарств и их метаболитов стенкой кишечника.
Через легкие выводятся летучие вещества и газы (эфир, закись азота, камфора и т.д.). Для ускорения их выброса необходимо увеличить объем легочной вентиляции.
Многие лекарственные препараты могут экскретироваться с молоком, особенно слабые основания и неэлектролиты, что следует учитывать при лечении кормящих матерей.
Некоторые лекарственные вещества частично выводятся железами слизистой оболочки полости рта, оказывая местное (например, раздражающее) действие на путях выведения. Так, тяжелые металлы (ртуть, свинец, железо, висмут), выделяясь слюнными железами, вызывают раздражение слизистой оболочки полости рта, возникают стоматиты и гингивиты. Кроме того, они вызывают появление темной каймы по десневому краю, особенно в области кариозных зубов, что обусловлено взаимодействием тяжелых металлов с сероводородом в полости рта и образованием практически нерастворимых сульфидов. Такая «кайма» является диагностическим признаком хронического отравления тяжелыми металлами.
При длительном применении дифенина и вальпроата натрия (противосудорожныепрепараты) раздражение слизистой оболочки десны может быть причиной возникновения гипертрофического гингивита («дифениновый гингивит»).Уровень элиминации любого лекарственного вещества оценивают при помощи двух основных тестов:
- во-первых, определяют время, в течение которого элиминирует половина введенной дозы химиопрепарата, то есть находят полупериод жизни последнего (Т 1/2);
- во-вторых, вычисляют процент той части однократной дозы препарата, которая элиминирует на протяжении суток (коэффициент, или квота, элиминации).
Эти два критерия элиминации любого лекарственного вещества не являются стабильными, ибо зависят от комплекса условий. Среди последних существенная роль отводится свойствам самого препарата и состоянию организма. Они зависят от скорости метаболизма лекарственного вещества в тканях и жидких средах организма, интенсивности его экскреции, функционального состояния печени и почек, пути введения химиопрепарата, длительности и условий хранения, липоидорастворимости, химического строения и т. д.
Элиминация жирорастворимых, ионизированных лекарственных веществ, связанных с белками, осуществляется медленнее» чем препаратов водорастворимых, ионизированных, не связанных с белками. При введении высоких доз лекарственных средств элиминация их удлиняется, что обусловлено интенсификацией всех процессов, участвующих в транспорте, распределении, метаболизме и выделении химиопрепаратов.
Элиминация большинства лекарственных средств у детей значительно ниже, чем у взрослых. Особенно замедлена она у недоношенных детей первых месяцев жизни. Резко удлиняют элиминацию врожденные и приобретенные энзимопатии (недостаточность глюкозо-6-фосфатдегидрогеназы, N-ацетилтрансферазы в др.), заболевания печени и почек, протекающие с недостаточностью их функций.
На скорость элиминации влияют и другие факторы:
пол больного, температура тела, физиологические биоритмы, пребывание ребенка в постели и т. д. Данные о полупериоде жизни препаратов позволяет врачу более обоснованно назначать разовую и суточную, дозу того или иного лекарственного средства, кратность введения его.
источник
Ферменты (энзимы) – это специфические белки, которые участвуют в биохимических реакциях, могут ускорять или замедлять их течение. В печени вырабатывается большое количество таких соединений в связи с ее важной ролью в обмене жиров, белков и углеводов. Их активность определяется по результатам биохимического анализа крови. Такие исследования важны для оценки состояния печени и для диагностики многих заболеваний.
Ферменты печени – это группа биологически активных белков, которые могут вырабатываться исключительно клетками этого органа. Они могут находиться на внутренней или наружной мембране, внутри клеток или в крови. В зависимости от роли энзимов, их разделяют на несколько категорий:
- гидролазы – ускоряют расщепление сложных соединений на молекулы;
- синтетазы – принимают участие в реакциях синтеза сложных биологических соединений из простых веществ;
- трансферазы – участвуют в транспорте молекул через мембраны;
- оксиредуктазы – являются основным условием нормального течения окислительно-восстановительных реакциях на клеточном уровне;
- изомеразы – необходимы для процессов изменения конфигурации простых молекул;
- лиазы – формируют дополнительные химические связи между молекулами.
От локализации печеночных ферментов зависит их функция в процессах клеточного обмена. Так, митохондрии участвуют в обмене энергии, гранулярная эндоплазматическая сеть синтезирует белки, гладкая – жиры и углеводы, на лизосомах находятся белки-гидролазы. Все энзимы, которые вырабатывает печень, можно обнаружить в крови.
В зависимости от того, какие функции выполняют энзимы и где они находятся в организме, их разделяют на 3 большие группы:
- секреторные – после секреции клетками печени поступают в кровь и находятся здесь в максимальной концентрации (факторы свертываемости крови, холинэстераза);
- индикаторные – в норме содержатся внутри клеток и высвобождаются в кровь только при их повреждении, поэтому могут служить индикаторами степени поражения печени при ее заболеваниях (АЛТ, АСТ и другие);
- экскреторные – выводятся из печени с желчью, а повышение их уровня в крови свидетельствует о нарушении этих процессов.
Для диагностики состояния печени имеет значение каждый из энзимов. Их активность определяют при подозрении на основные патологии печени и для оценки степени повреждения печеночной ткани. Для получения более полной картины может потребоваться также диагностика пищеварительных ферментов, энзимов желудочно-кишечного тракта, поджелудочной железы и желчевыводящих путей.
Биохимия крови – это важный этап диагностики болезней печени. Все патологические процессы в этом органе могут происходить с явлениями холестаза или цитолиза. Первый процесс представляет собой нарушение оттока желчи, которую выделяют гепатоциты. При остальных нарушениях происходит разрушение здоровых клеточных элементов с высвобождением их содержимого в кровь. По наличию и количеству энзимов печени в крови можно определить стадию болезни и характер патологических изменений в органах гепатобилиарного тракта.
Синдром холестаза (затруднение желчеотделения) сопровождает воспалительные заболевания печени, нарушение секреции желчи и патологии желчевыводящих путей. Эти явления вызывают следующие изменения в биохимическом анализе:
- экскреторные энзимы повышены;
- увеличены также компоненты желчи, в том числе билирубин, желчные кислоты, холестерин и фосфолипиды.
Отток желчи может нарушаться при механическом давлении на желчные протоки (воспаленной тканью, новообразованиями, камнями), сужении их просвета и других явлениях. Комплекс характерных изменений показателей крови становится основанием для более подробного исследования состояния желчного пузыря и желчевыводящих путей.
Цитолиз (разрушение гепатоцитов) может происходить при инфекционных и незаразных гепатитах либо при отравлениях. В таком случае содержимое клеток высвобождается, а индикаторные ферменты появляются в крови. К ним относятся АЛТ (аланинаминотрансфераза), АСТ (аспартатаминотрансфераза), ЛДГ (лактатдегидрогеназа) и альдолаза. Чем выше показатели этих соединений в крови, тем обширнее степень поражения паренхимы органа.
Щелочная фосфатаза, которая обнаруживается в крови, может иметь не только печеночное происхождение. Небольшое количество этого фермента вырабатывается костным мозгом. О заболеваниях печени можно говорить, если происходит одновременное повышение уровня ЩФ и гамма-ГГТ. Дополнительно может обнаруживаться увеличение показателей билирубина, что говорит о патологиях желчного пузыря.
ГГТ обычно повышается с щелочной фосфатазой. Эти показатели свидетельствуют о развитии холестаза и о возможных заболеваниях желчевыводящей системы. Если этот фермент повышается изолированно, есть риск незначительного повреждения печеночной ткани на начальных стадиях алкоголизма или других отравлениях. При более серьезных патологиях наблюдается одновременное увеличение печеночных энзимов.
АЛТ (аланинаминотрансфераза) – это наиболее специфичный фермент печени. Он находится в цитоплазме и других органов (почек, сердца), но именно в печеночной паренхиме он присутствует в наибольшей концентрации. Его повышение в крови может указывать на различные заболевания:
- гепатит, интоксикации с повреждением печени, цирроз;
- инфаркт миокарда;
- хронические заболевания сердечно-сосудистой системы, которые проявляются некрозом участков функциональной ткани;
- травмы, повреждения или ушибы мышц;
- тяжелая степень панкреатита – воспаления поджелудочной железы.
Взаимодействие ряда лекарственных веществ в процессе их распределения в организме можно рассматривать как один из важных фармакокинетических этапов, который характеризует их биотрансформацию, ведущую в большинстве случаев к образованию метаболитов.
Метаболизм (биотрансформация) - процесс химической модификации лекарственных веществ в организме .
Метаболические реакции подразделяют на несинтетические (когда лекарственные вещества претерпевают химические превращения, подвергаясь окислению, восстановлению и гидролитическому расщеплению или нескольким из этих превращений) - I фаза метаболизма и синтетические (реакция конъюгации и др.) - II фаза. Обычно несинтетические реакции представляют собой лишь начальные стадии биотрансформации, а образующиеся продукты могут участвовать в синтетических реакциях и затем элиминировать.
Продукты несинтетических реакций могут обладать фармакологической активностью. Если активностью обладает не само вещество, введенное в организм, а какой-либо метаболит, то его называют пролекарством.
|
Некоторые лекарственные вещества, продукты метаболизма которых обладают важной в терапевтическом отношении активностью |
|
|
Лекарственное вещество |
Активный метаболит |
|
Аллопуринол |
Аллоксантин |
|
Амитриптилин |
Нортриптилин |
|
Ацетилсалициловая кислота* |
Салициловая кислота |
|
Ацетогексамид |
Гидроксигексамид |
|
Глютетимид |
4-гидроксиглютетимид |
|
Диазелам |
Дезметилдиазепам |
|
Дигитоксин |
Дигоксин |
|
Имипрамин |
Дезипрамин |
|
Кортизон |
Гидрокортизон |
|
Лидокаин |
Дезэтиллидокаин |
|
Метилдопа |
Метилнорадреналин |
|
Преднизон* |
Преднизолон |
|
Пропранолол |
4-гидроксипролранолол |
|
Спиронолактон |
Канренон |
|
Тримеперидин |
Нормеперидин |
|
Фенацетин* |
Ацетаминофен |
|
Фенилбутазон |
Оксифенбутазон |
|
Флуразепам |
Дезэтилфлуразепам |
|
Хлоралгидрат* |
Трихлорэтанол |
|
Хлордиазепоксид |
Дезметилхлордиазепоксид |
|
* пролекарства, терапевтическое действие оказывают главным образом продукты их метаболизма. |
|
Несинтетические метаболические реакции лекарственных веществ катализируются микросомальными ферментными системами эндоплазматического ретикулума печени или немикросомальных ферментных систем. К таким веществам относятся: амфетамин, варфарин, имипрамин, мепробамат, прокаинамид, фенацетин, фенитоин, фенобарбитал, хинидин.
В синтетических реакциях (реакциях конъюгации) лекарственное вещество или метаболит - продукт несинтетической реакции, соединяясь с эндогенным субстратом (глюкуроновой, серной кислотами, глицином, глутамином), образуют конъюгаты. Они, как правило, не обладают биологической активностью и, будучи высокополярными соединениями, хорошо фильтруются, но плохо реабсорбируются в почках, что способствует их быстрому выведению из организма.
Самыми распространенными реакциями конъюгации являются : ацетилирование (основной путь метаболизма сульфаниламидов, а также гидралазина, изониазида и прокаинамида); сульфатирование (реакция между веществами с фенольными или спиртовыми группами и неорганическим сульфатом. Источником последнего могут быть серосодержащие кислоты, например цистеин); метилирование (инактивируются некоторые катехоламины, ниацинамид, тиоурацил). Примеры различных типов реакций метаболитов лекарственных веществ приведены в таблице.
|
Типы реакций метаболизма лекарственных веществ |
|
|
Тип реакции |
Лекарственное вещество |
|
I. НЕСИНТЕТИЧЕСКИЕ РЕАКЦИИ (катализируются ферментами эндоплазматического ретикулума или немикросомальными ферментами) |
|
|
Окисление |
|
|
Алифатическое гидроксилирование, или окисление боковой цепочки молекулы |
Тиолентал, метогекситал, пентазоцин |
|
Ароматическое гидроксилирование, или гидроксилирование ароматического кольца |
Амфетамин, лидокаин, салициловая кислота, фенацетин, фенилбутазон, хлорпромазин |
|
O-дезалкилирование |
Фенацетин, кодеин |
|
N-дезалкилирование |
Морфин, кодеин, атропин, имипрамин, изопреналин, кетамин, фентанил |
|
S-дезалкилирование |
Производные барбитуровой кислоты |
|
N-окисление |
Аминазин, имипрамин, морфин |
|
S-окисление |
Аминазин |
|
Дезаминирование |
Фенамин, гисгамин |
|
Десульфирование |
Тиобарбитураты, тиоридазин |
|
Дегалогенизация |
Галотан, метоксифлуран, энфлуран |
|
Восстановление |
|
|
Восстановление азогруппы |
Сульфаниламид |
|
Восстановление нитрогруппы |
Нитразепам, хлорамфеникол |
|
Восстановление карбоновых кислот |
Преднизолон |
|
Восстановление, катализируемое алкогольдегидрогеназой |
Этанол, хлоралгидрат |
|
Эфирный гидролиз |
Ацетилсалициловая кислота, норзпинефрин, кокаин, прокаинамид |
|
Амидный гидролиз |
Лидокаин, пилокарпин, изониазид новокаинамид фентанил |
|
II. СИНТЕТИЧЕСКИЕ РЕАКЦИИ |
|
|
Конъюгация с глюкуроновой кислотой |
Салициловая кислота, морфин, парацетамол, налорфин, сульфаниламиды |
|
Конъюгация с сульфатами |
Изопреналин, морфин, парацетамол, салициламид |
|
Конъюгация с аминокислотами: |
|
|
Салициловая кислота, никотиновая кислота |
|
Изоникотиновая кислота |
|
Парацетамол |
|
Ацетилирование |
Новокаинамид, сульфонамиды |
|
Метилирование |
Норадреналин, гистамин, тиоурацил, никотиновая кислота |
Превращение некоторых лекарственных веществ, принятых перорально, существенно зависит от активности ферментов, вырабатываемых микрофлорой кишечника, где гидролизуются нестойкие сердечные гликозиды, что существенно снижает их кардиальный эффект. Ферменты, вырабатываемые резистентными микроорганизмами, катализируют реакции гидролиза и ацетилирования, вследствие которых антимикробные средства теряют свою активность.
Существуют примеры, когда ферментативная активность микрофлоры способствует образованию лекарственных веществ, которые проявляют свою активность. Так, фталазол (фталилсульфатиазол) вне организма практически не проявляет противомикробной активности, но под влиянием ферментов микрофлоры кишечника гидролизуется с образованием норсульфазола и фталевой кислоты, оказывающих противомикробный эффект. При участии ферментов слизистой оболочки кишечника гидролизуются резерпин и ацетилсалициловая кислота.
Однако главным органом, где осуществляется биотрансформация лекарственных веществ, является печень. После всасывания в кишечнике они через воротную вену попадают в печень, где и подвергаются химическим превращениям.
Через печеночную вену лекарственные вещества и их метаболиты поступают в системное кровообращение. Совокупность этих процессов называют «эффектом первого прохождения», или пресистемной элиминацией, в результате которой количество и эффективность вещества, поступающего в общий кровоток, может изменяться.
Следует иметь в виду, что при пероралъном приеме лекарств их биодоступностъ индивидуальна для каждого пациента и варьирует для каждого препарата . Вещества, подвергающиеся значительным метаболическим превращениям при первом прохождении в печени, могут не оказывать фармакологического эффекта, например лидокаин, нитроглицерин. Кроме того, метаболизм первого прохождения может осуществляться не только в печени, но и в других внутренних органах. Например, хлорпромазин сильнее метаболизируется в кишечнике, чем в печени.
На течение пресистемной элиминации одного вещества часто оказывают влияние другие лекарственные вещества. Например, аминазин снижает «эффект первого прохождения» пропранолола, в результате концентрация β-адреноблокатора в крови повышается.
Всасывание и пресистемная элиминация определяют биологическую доступность и, в значительной степени, эффективность лекарственных веществ .
Ведущую роль в биотрансформации лекарственных веществ играют ферменты эндоплазматической сети клеток печени, которые нередко называют микросомальными ферментами. Известно более 300 лекарственных веществ, способных изменять активность микросомальных ферментов . Вещества, повышающие их активность, получили название индукторов .
Индукторами ферментов печени являются: снотворные средства (барбитураты, хлоралгидрат), транквилизаторы (диазепам, хлордиазепоксид, мепробамат), нейролептики (хлорпромазин, трифлуоперазин), противосудорожные (фенитоин), противовоспалительные (фенилбутазон), некоторые антибиотики (рифампицин), диуретики (спиронолактон) и др.
Активными индукторами ферментных систем печени также считаются пищевые добавки, малые дозы алкоголя, кофе, хлорированные инсектициды (дихлордифенилтрихлорэтан (ДДТ), гексахлоран). В небольших дозах некоторые лекарственные средства, например фенобарбитал, фенилбутазон, нитраты, могут стимулировать собственный метаболизм (аутоиндукция).
При совместном назначении двух лекарственных веществ, одно из которых индуцирует печеночные ферменты, а второе метаболизируется в печени, дозу последнего необходимо увеличить, а при отмене индуктора - снизить. Классический пример такого взаимодействия - сочетание антикоагулянтов непрямого действия и фенобарбитала. Специальными исследованиями доказано, что в 14% случаев причиной кровотечений при лечении антикоагулянтами является отмена лекарственных веществ, индуцирующих микросомальные ферменты печени.
Очень большой индуцирующей активностью микросомальных ферментов печени обладает антибиотик рифампицин, несколько меньшей - фенитоин и мепробамат.
Фенобарбитал и другие индукторы ферментов печени не рекомендуется применять в сочетании с парацетамолом и другими лекарственными веществами, продукты биотрансформации которых токсичнее исходных соединений. Иногда индукторы ферментов печени используют для ускорения биотрансформации соединений (метаболитов), чужеродных для организма. Так фенобарбитал, который способствует образованию глюкуронидов, можно использовать для лечения желтухи с нарушенной конъюгацией билирубина с глюкуроновой кислотой.
Индукцию микросомальных ферментов часто приходится рассматривать как нежелательное явление, поскольку ускорение биотрансформации лекарств приводит к образованию неактивных или менее активных соединений и уменьшению терапевтического эффекта. Например, рифампицин может снизить результативность лечения глюкокортикостероидами, что приводит к повышению дозы гормонального препарата.
Значительно реже в результате биотрансформации лекарственного вещества образуются более активные соединения, В частности, при лечении фуразолидоном в течение 4-5 дней в организме накапливается двуоксиэтилгидразин, который блокирует моноаминооксидазу (МАО) и альдегиддегидрогеназу, катализирующую окисление альдегидов в кислоты. Поэтому пациентам, принимающим фуразолидон, не следует употреблять спиртные напитки, так как концентрация в крови уксусного альдегида, образующегося из этилового спирта, может достичь такого уровня, при котором развивается выраженное токсическое действие этого метаболита (синдром ацетальдегида).
Лекарственные вещества, снижающие или полностью блокирующие активность ферментов печени, получили название ингибиторов .
К лекарственным веществам, угнетающим активность ферментов печени, относят наркотические анальгетики, некоторые антибиотики (актиномицин), антидепрессанты, циметидин и др. В результате применения комбинации лекарственных веществ, одно из которых ингибирует ферменты печени, замедляется скорость метаболизма другого лекарственного вещества, повышаются его концентрация в крови и риск побочных действий. Так, антагонист гистаминовых H2-репепторов циметидин дозозависимо угнетает активность ферментов печени и замедляет метаболизм антикоагулянтов непрямого действия, что повышает вероятность кровотечений, а также β-адреноблокаторов, что приводят к выраженной брадикардии и артериальной гипотензии. Возможно угнетение метаболизма антикоагулянтов непрямого действия хинидином. Развивающиеся при таком взаимодействии побочные эффекты могут иметь тяжелое течение. Хлорамфеникол угнетает обмен толбутамида, дифенилгидантоина и неодикумарина (этил бискумацетата). Описано развитие гипогликемической комы при комбинированной терапии хлорамфениколом и толбутамидом. Известны летальные случаи при одновременном назначении больным азатиоприна или меркаптопурина и аллопуринола, ингибирующего ксантиноксидазу и замедляющего метаболизм иммуносупрессивных препаратов.
Способность одних веществ нарушать метаболизм других иногда специально используют в медицинской практике. Например, дисульфирам применяют при лечении алкоголизма. Этот препарат блокирует метаболизм этилового спирта на стадии ацетальдегида, накопление которого вызывает неприятные ощущения. Подобным образом действуют также метронидазол и противодиабетические средства из группы производных сульфонилмочевины.
Своеобразную блокаду активности фермента используют при отравлении метиловым спиртом, токсичность которого определяется формальдегидом образующимся в организме под влиянием фермента алкогольдегидрогеназы. Он катализирует также превращение этилового спирта в уксусный альдегид, причем сродство фермента к этиловому спирту выше, чем к метиловому. Поэтому, если в среде находятся оба спирта, фермент катализирует главным образом биотрансформацию этанола, и формальдегид, обладающий значительно более высокой токсичностью, чем уксусный альдегид, образуется в меньшем количестве. Таким образом, этиловый спирт можно использовать в качестве противоядия (антидота) при отравлении метиловым спиртом.
Этиловый спирт изменяет биотрансформацию многих лекарственных веществ . Однократное его применение блокирует инактивацию различных лекарственных веществ и может усиливать их действие. В начальной стадии алкоголизма активность микросомальных ферментов печени может увеличиваться, что ведет к ослаблению действия лекарственных веществ вследствие ускорения их биотрансформации. Напротив, на более поздних стадиях алкоголизма, когда многие функции печени нарушены, следует учитывать, что действие лекарственных веществ, биотрансформация которых в печени нарушена, может заметно усилиться.
Взаимодействие лекарственных веществ на уровне метаболизма может реализовываться через изменение печеночного кровотока. Известно, что факторы лимитирующие метаболизм препаратов с выраженным эффектом первичной элиминации (пропранолол, верапамил и др.) - это величина печеночного кровотока и в значительно меньшей степени активность гепатоцитов. В связи с этим любые лекарственные вещества, уменьшающие регионарное печеночное кровообращение, снижают интенсивность метаболизма данной группы препаратов и повышают их содержание в плазме крови.
К взаимодействиям, снижающим концентрацию лекарственных веществ, относятся:
Уменьшение всасывания в ЖКТ.
Индукция печеночных ферментов.
Снижение клеточного захвата.
I.Уменьшение всасывания в ЖКТ.
Анионообменная смола холестирамин связывает в ЖКТ препараты тиреоидных гормонов и сердечные гликозиды, препятствуя тем самым их всасыванию. Возможно, это средство взаимодействует и с другими препаратами, поэтому желательно, чтобы между приемом холестирамина и других средств прошло не меньше 2 ч.
Ионы алюминия, содержащиеся в антацидных средствах, образуют нерастворимые комплексы с тетрациклинами, также препятствуя их всасыванию.
Двухвалентные ионы железа тоже подавляют всасывание тетрациклинов.
Каолин/пектин в суспензии связывает дигоксин, уменьшая его всасывание в 2 раза. Однако этот эффект не проявляется, если каолин/пектин принимать не раньше чем через 2 ч после дигоксина.
Кетоконазол - это слабое основание, диссоциирующее только в кислой среде. Поэтому Н2-блокаторы (ранитидин, фамотидин и др.), снижающие кислотность желудочного содержимого, препятствуют диссоциации и всасыванию кетоконазола.
На всасывание флуконазола снижение кислотности желудочного содержимого не влияет.
Аминосалициловая кислота при приеме внутрь по неясному пока механизму снижает всасывание рифампицина.
II.Индукция печеночных ферментов.
Если главный путь элиминации препарата - метаболизм, то ускорение метаболизма приводит к снижению концентрации препарата в органах-мишенях. Большая часть лекарственных веществ метаболизируется в печени - органе с большой клеточной массой, высоким кровотоком и содержанием ферментов. Первая реакция в метаболизме многих препаратов катализируется микросомальными ферментами печени, связанными с цитохромом Р450 и содержащимися в эндоплазматическом ретикулуме. Эти ферменты окисляют молекулы лекарственных средств с помощью различных механизмов - гидроксилирования ароматического кольца, N-деметилирования, О-деметилирования и сульфоокисления. Молекулы продуктов этих реакций обычно более полярны, чем молекулы их предшественников, и потому легче удаляются почками.
Экспрессия некоторых изоферментов цитохрома Р450 регулируется, и их содержание в печени может увеличиваться под действием некоторых лекарственных средств.
Типичное вещество, вызывающее индукцию микросомальных ферментов печени, - это фенобарбитал. Так же действуют и другие барбитураты. Индуцирующий эффект фенобарбитала проявляется уже в дозе 60 мг/сут.
Индукцию микросомальных ферментов печени вызывают также рифампицин, карбамазепин, фенитоин, глутетимид; она наблюдается у курильщиков, при воздействии хлорсодержащих инсектицидов типа ДДТ и постоянном употреблении алкоголя.
Фенобарбитал, рифампицин и другие индукторы микросомальных ферментов печени вызывают снижение сывороточной концентрации многих лекарственных средств, и в том числе - варфарина, хинидина, мексилетина, верапамила, кетоконазола, итраконазола, циклоспорина, дексаметазона, метилпреднизолона, преднизолона (активного метаболита преднизона), стероидных пероральных контрацептивов, метадона, метронидазола и метирапона. Эти взаимодействия имеют большое клиническое значение. Так, если у больного на фоне непрямых антикоагулянтов достигается должный уровень свертываемости крови, но одновременно он принимает какой-либо индуктор микросомальных ферментов печени, то при отмене последнего (например, при выписке) сывороточная концентрация антикоагулянта возрастет. В результате может возникнуть кровоточивость.
Существуют значительные индивидуальные различия в индуцируемости ферментов метаболизма лекарственных средств. У одних больных фенобарбитал резко повышает этот метаболизм, у других - почти не влияет.
Фенобарбитал не только вызывает индукцию некоторых изоферментов цитохрома Р450 , но и усиливает печеночный кровоток, стимулирует секрецию желчи и транспорт органических анионов в гепатоцитах.
Некоторые лекарственные вещества могут усиливать также конъюгацию других веществ с билирубином.
III.Снижение клеточного захвата.
Производные гуанидина, используемые для лечения артериальной гипертонии (гуанетидин и гуанадрел), переносятся в адренергические нейроны благодаря активному транспорту биогенных аминов. Физиологическая роль этого транспорта - обратный захват адренергических медиаторов, но с его помощью могут переноситься против концентрационного градиента и многие другие сходные по структуре соединения, включая производные гуанидина.
Ингибиторы обратного захвата норадреналина препятствуют захвату этих препаратов адренергическими нейронами, блокируя тем самым их действие. Мощными ингибиторами обратного захвата норадреналина являются трициклические антидепрессанты. В связи с этим при одновременном приеме трициклических антидепрессантов (дезипрамина, имипрамина, протриптилина, нортриптилина и амитриптилина) и гуанетидина либо гуанадрела гипотензивный эффект последних почти полностью подавляется. Доксепин и хлорпромазин в меньшей степени блокируют обратный захват норадреналина, но и они оказывают дозозависимое антагонистическое действие по отношению к производным гуанидина. Так же влияет и эфедрин. У больных с тяжелой артериальной гипертонией подобные лекарственные взаимодействия могут приводить к неэффективности лечения, гипертоническому кризу и инсульту.
Гипотензивный эффект клонидина также частично подавляется трициклическими антидепрессантами. Клонидин действует на сердечно-сосудистый центр продолговатого мозга, вызывая снижение симпатического тонуса. Именно здесь его эффект и блокируется трициклическими антидепрессантами.
Смотрите также:
ЛЕКАРСТВЕННЫЕ ВЗАИМОДЕЙСТВИЯ
Перечисленные механизмы абсорбции (всасывания) «работают», как правило, параллельно, но преобладающий вклад вносит обычно один из них (пассивная диффузия, фильтрация, активный транспорт, пиноцитоз). Так, в ротовой полости и в желудке главным образом реализуется пассивная диффузия, в меньшей степени - фильтрация. Другие механизмы практически не задействованы.
В тонком кишечнике нет препятствий для реализации всех механизмов всасывания; какой из них доминирует, зависит от лекарственного средства.
В толстом кишечнике и прямой кишке преобладают процессы пассивной диффузии и фильтрации. Они же являются основными механизмами всасывания лекарственных средств через кожу.
Применение любого лекарства с лечебной или профилактической целью начинается с его введения в организм или нанесения на поверхность тела. От путей введения зависят скорость развития эффекта, его выраженность и продолжительность. Существующие пути введения обычно подразделяют на ЭНТЕРАЛЬНЫЕ (то есть через пищеварительный тракт: введения через рот, под язык, в 12-перстную кишку, в прямую кишку или ректально), и ПАРЕНТЕРАЛЬНЫЕ (то есть минуя пищеварительный тракт: в/венное введение, в/артериальное, в/мышечное, п/кожное, ингаляции - аэрозоли, газы, порошки); интратекальное или субарахноидальное введение; наконец, - местное применение лекарств: внутриматочное, введение во влагалище, введение в мочевой пузырь, внутрибрюшинное и т. д.).
От пути введения лекарственного средства во многом зависит, сможет ли оно попасть к месту действия (в биофазу) (например, в очаг воспаления) и оказать лечебный эффект.
II. РАСПРЕДЕЛЕНИЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ В ОРГАНИЗМЕ. БИОЛОГИЧЕСКИЕ БАРЬЕРЫ. ДЕПОНИРОВАНИЕ
После абсорбции лекарственные вещества попадают, как правило, в кровь, а затем разносятсяв разные органы и ткани. Характер распределения лекарственного средства определяется множеством факторов, в зависимости от которых лекарство будет распределяться в организме равномерно или неравномерно. Следует сказать, что большинство лекарственных средств распределяется неравномерно и лишь незначительная часть - относительно равномерно (ингаляционные средства для наркоза). Наиболее важными факторами, влияющими на характер распределения лекарственного средства, являются: 1) растворимость в липидах,
2) степень связывания с белками плазмы крови, 3) интенсивность регионарного кровотока.
Растворимость в липидах лекарственного средства определяет способность его проникать через биологические барьеры. Это прежде всего, стенка капилляров и клеточные мембраны, являющиеся основными структурами различных гистогематических барьеров, в частности, таких как, гематоэнцефалический и плацентарный барьеры. Неионизированные жирорастворимые лекарственные средства легко проникают через клеточные мембраны и распределяются во всех жидких средах организма. Распределение лекарственных средств, плохо проникающих через клеточные мембраны (ионизированные лекарственные вещества), осуществляется не столь равномерно.
Проницаемость ГЭБ возрастает при повышении осмотического давления плазмы крови. Различные заболевания могут изменять распределение лекарств в организме. Так развитие ацидоза может способствовать проникновению в ткани лекарств - слабых кислот, которые меньше диссоциируются в таких условиях.
Иногда распределение лекарственного вещества зависит от сродства препарата к тем или иным тканям, что приводит к их накоплению в отдельных органах и тканях. В качестве примера можно назвать образование тканевого депо в случае использования препаратов, содержащих йод (J) в тканях щитовидной железы. При использовании тетрациклинов последние могут избирательно накапливаться в костной ткане, в частности, зубах. Зубы в таком случае, особенно у детей, могут приобрести желтую окраску.
Такая избирательность действия обусловлена сродством тетрациклинов к биологическим субстратам костной ткани, а именно образованием тетрациклинкальциевых комплексов по типу хелатов (hela - клешня рака). Данные факты важно помнить, особенно педиатрам и акушер-гинекологам.
Некоторые препараты могут в больших количествах накапливаться внутри клеток, образуя клеточные депо (акрихин). Происходит это за счет связывания лекарственного вещества с внутриклеточными белками, нуклепротеидами, фосфолипидами.
Некоторые средства для наркоза в силу своей липофильности могут образовывать жировые депо, что также следует учитывать.
Депонируются лекарственные средства, как правило, за счет обратимых связей, что в принципе, определяет продолжительность их нахождения в тканевых депо. Однако если образуются стойкие комплексы с белками крови (сульфадиметоксин) или тканей (соли тяжелых металлов), то нахождение этих средств в депо существенно удлиняется.
Следует также иметь ввиду, что после всасывания в системный кровоток большая часть лекарственного вещества в первые минуты попадает в те органы и ткани, которые наиболее активно перфузируются кровью (сердце, печень, почки). Медленнее происходит насыщение лекарственным средством мышц, слизистных оболочек, кожи и жировой ткани. Для достижения терапевтических концентраций лекарственных веществ в этих тканях требуется время от нескольких минут до нескольких часов.
Наиболее наглядно влияние состояния гемодинамики на распределение лекарственных средств прослеживается в условиях патологии. Дело в том, что нарушения гемодинамики могут существенно изменять кинетику распределения. Так, при геморрагическом шоке или при застойной сердечной недостаточности перфузия большинства органов уменьшается. Нарушение скорости гломерулярной фильтрации и печеночного кровотока приводят к снижению соответственно почечного и печеночного клиренса, что сразу же скажется возрастанием концентрации препарата в плазме крови. Соответственно, будут увеличены интенсивность и длительность действия препарата. В качестве примера можно указать на увеличение продолжительности действия тиопентала при шоке.
Многие лекарственные вещества обладают сильным физико-химическим сродством к различным белкам плазмы крови. Наиболее важными в этом отношении являются альбумины и в меньшей степени кислые альфа-гликопроитеиды. Такое средство лекарства приводит в конечном счете к тому, что после всасывания оно может циркулировать в крови не только в свободной форме, но и в форме, связанной с белками. Это так называемое, ЭКСТРАЦЕЛЛЮЛЯРНОЕ (внеклеточное) депо лекарственного вещества, его своеобразный резервуар в крови. Фракция связанного с белками плазмы препарата является временным депо и предупреждает резкие колебания концентрации несвязанного вещества в крови и жидких средах организма. Связывание лекарственных ввеществ с белками плазмы ограничивает их концентрацию в тканях и в месте действия, так как только свободный (несвязанный) препарат может проходить через мембраны. Вещество же, находящееся в комплексе с белком, лишено специфической активности. Связывание с белками снижает диффузию лекарственного вещества в клетку и поэтому замедляет процесс метабонизма. Связывание с белками снижает количество лекарственного вещества, способного фильтроваться в почечных клубочках, в результате чего замедляется и процесс его выведения (экскреция).
Практически ощутимо, если лекарственное вещество связывается с белками очень активно, то есть более чем на 90%. Сила взаимодействия белков крови и лекарства выражается сродством или аффинитетом. Из этого определения (положения) вытекают важный вывод:
Если А - лекарство,
а О - белок, то А + В = АО
Как видно из данного уравнения, свободная и связанная части лекарственного вещества находятся в состоянии динамического равновесия. Так как лекарство активно только лишь в свободном состоянии, то в связи с белком оно неактивно. Несколько упрощенное сравнение можно допустить, что в свободном состоянии лекарство действует на фармакологические рецепторы тканей как ключ к замку, а в связи с белком - этот ключ не работает.
От степени аффинитета, то есть силы связывания лекарства с белком зависит:
1) скорость поступления лекарственного вещества в ткани. Поскольку активность лекарственного вещества определеяется частью, способной к диффузии, то препараты с высокой степенью аффинитета, высоким сродством к белкам, такие, как длительно действующие сульфаниламиды (аффинитет > 90%), действуют медленно и содержатся в интерстициальной (межклеточной) жидкости и в клетках тканей в невысоких концентрациях.
Другим примером является сердечный гликозид (дигитоксин), связывающийся с белками на 97%. После приема этого препарата внутрь он начинает действовать лишь через 5-6-7 часов.
2) От степени аффинитета лекарственные средства с белками плазмы зависит длительность их действия. Дигитоксин после 1-кратного приема оказывает фармакологический эффект в течение 2-3 дней, а остаточное его действие реализуется даже через несколько недель (14-21 день). Если при хронической сердечной недостаточности, связываеия лекарств с белками плазмы снижается, то при хронической легочной недостаточности или в послеоперационном периоде повышается (примерно на 10%). У больных со сниженной функции почек процент связывания с белками кислых лекарственных средств со свойствами кислот уменьшается.
3) Степень аффинитета лекарства с белками крови влияет на различие эффектов лекарственных веществ у людей с различной патологией. Например, при развитии у больного с ожоговой болезнью глубокой гипопротеинемии фракция свободного лекарственного вещества увеличивается, что в такой ситуации требует снижения терапевтических доз препарата. Аналогичная ситуация может развиться при голодании, когда, если не будет снижена доза лекарства, на обычную его дозу разовьется токсический эффект (аналогично и при лучевой болезни).
4) Одновременное применение препаратов, связывающихся с одними и теми же радикалами белковых молекул может вызвать эффект конкуренции их за связь с белками. Если в таком случае эти препараты обладают различной связывающейся способностью, то есть различным аффинитетом, может произойти внезапное повышение концентрации одного из них, иногда до опасного уровня. Так, если больной получает непрямой антикоагулянт (препарат типа фенилина, неодокумарина), коагуляционный потенциал которого, скоррегирован, то при дополнительном введении (воспаление суставов) салицилатов или бутадиона в плазме крови может значительно повыситься уровень свободного препарата (антикоагулянта) вследствие вытеснения его салицилатом (бутадионом) из комплекса с белками. В результате возникает риск кровотечения. Схематично это можно отобразить следующим образом:
А + О = АО + В = ВО + А, где В - бутадион.
Эти фармакокинетические данные стали известны лишь в последние годы.
Какова же дальнейшая судьба лекарственных средств в организме? После сывания и распределения препараты могут:
1) метаболизироваться под влиянием адекватных ферментов;
2) изменяться спонтанно, превращаясь в другие вещества без воздействия ферментов;
3) либо могут выводиться из организма (или экскретироваться) в неизменном виде.
Некоторые лекарственные вещества, спонтанно изменяются (эмбихин), превращаясь в другие вещества при соответствующих изменениях кислотности среды в организме. Таким образом, в живом организме лекарственные вещества подвергаются определенным изменениям или БИОТРАНСФОРМАЦИИ. Под биотрансформацией (или превращением, или метаболизмом) понимают комплекс физико-химических и биохимических превращений лекарственных веществ, способствующих их переводу в более простые, ионизированные, более полярные и, следователно, водорастворимые компоненты (метаболиты), которые легче выводятся из организма. Другими словами, какой бы структурой ксенобиотик не обладал, встречающийся с ним адекватный фермент переводит его в состояние, удобное для выведения из организма (как правило ксенобиотик становится менее липофильным) или в состояние для использования в качестве энергетического и пластического материала (кокарбоксилаза, натрия нуклеинат). Хотя некоторые лекарственные вещества биотрансформируясь, образуют метаболиты, более активные по сравнению с вводимыми в организм веществами, подавляющее большинство лекарств инактивируется, разлагается, трансформируется до более простых, фармакологически менее активных и менее токсичных метабонитов. Биотрансформация введенных лекарств происходит преимущественно в печени, но может в почках, стенке кишечника, легких, мышцах и других органах. Процессы биотрансформации сложны и обычно включают ряд последовательлных стадий, каждая из которых опосредуется определенным ферментом крови.
Различают два (2) типа реакций метаболизма лекарственных препаратов в организме: НЕСИНТЕТИЧЕСКИЕ и СИНТЕТИЧЕСКИЕ.
1. К несинтетическим реакциям относятся ОКИСЛЕНИЕ, ВОССТАНОВЛЕНИЕ и ГИДРОЛИЗ. Все несинтетические реакции метаболизма, называемые также метаболической трансформацией лекарственных препаратов, также можно разделить в зависимости от локализации 2-х основных биотрансформирующих систем на 2 группы:
а) основная группа реакций, по которым биотрансформируются большинство лекарственных средств, это реакции катализируемые ферментами эндоплазматического ретикулума гепатоцитов или МИКРОСОМАЛЬНЫЕ реакции;
б) реакции, катализируемые ферментами другой локализации, НЕМИКРОСОМАЛЬНЫЕ реакции.
То есть, если микросомальная биотрансформирующая система, представлена ферментами эндоплазматического ретикулуна гепатоцитов печени, то немикросомальная система - ферментами иной локализации.
Микросомальные реакции окисления или восстановления лекарственных средств, а точнее их отдельных активных групп в структуре лекарственной молекулы, происходят при участии монооксигеназных систем, основными компонентами которых являются цитохром Р-450 и никотин-амидаденин-динуклеотид фосфорированный восстановленный (НАДФ Н).
Эти цитохромы являются первичными компонентами окислительной ферментной монооксигеназной системы. В большинстве случаев фармакологическая активность таких метаболитов становится меньше активности исходного вещества.
Дальнейшее окисление лекарственных веществ происходит под влиянием других окислительных ферментов, таких как ОКСИДАЗЫ и РЕДУКТАЗЫ, при обязательном участии НАДФ и молекулярного кислорода.
Микросомальные ферменты в основном катализируют процессы окисления многих лекарственных средств, то реакции ВОССТАНОВЛЕНИЯ и ГИДРОЛИЗА этих средств, связаны не только с микросомальными, но и немикросомальнми энзимами. Хотя немикросомальные ферменты участвуют в биотрансформации небольшого числа лекарственных средств, они все же играют важную роль в их метаболизме. Немикросомальная биотрансформация препаратов происходит также в печени, но может протекать в плазме крови и другиз тканях (желудке, кишечнике, легких). В качестве примера можно привести биотрансформацию ацетилхолина в плазме крови, осуществляемую ферментом ЭСТЕРАЗОЙ, в нашем случае - АЦЕТИЛХОЛИНЭСТЕРАЗОЙ. По таким реакциям биотрансформируются ряд общеупотребительных лекарств, напрмер, аспирин и сульфаниламиды.
В основе синтетических реакций лежит образование парных эфиров лекарственных средств с глюкуроновой, серной, уксусной кислотами, а также с глицином и глутатионом, что помогает созданию вы
сокополярных соединений, хорошо растворимых в воде, мало растворимых в липидах, плохо проникающих в ткани и в большинстве случаев фармакологически неактивных. Естественно, что эти метаболиты хорошо выводятся из организма. Таким образом, синтетические реакции ведут к образованию, синтезу нового метаболита и осуществляется с помощью реакций коньюгации, ацетилирования, метилирования и пр.
В качестве примера, биотрансформации лекарственных средств по синтетическим реакциям можно привести следующую иллюстрацию. В печени взрослых антибиотик левомицетин подвергается коньгации с клюкуроновой кислотой на 90% и только на 10% его экскретируется с мочой в неизменном виде. Образующиеся глюкурониды легко биотрансформируются и выводятся. Таким же путем из органинзма выводятся эстрогенные и глюкокортикоидные препараты, алкалоиды опия, салицилаты, барбитураты и другие средства.
С точки зрения эволюции более древний путь биотрансформации - это присоединение к ксенобиотику (коньюгация) высокополярных групп: глюкуроновой кислоты, сульфата, глицина, фосфата, ацетила, эпоксидной группы, делающих ксенобиотики более растворимыми в воде. Эволюционно более молодой путь - окислительно-восстановительный (реакции окисления, восстановления, гидролиза) рассматривается как начальная фаза биотрансформации. Продукты окисления или восстановления (I фаза) обычно подвергаются затем коньюгированию (II фаза). Таким образом, можно сказать, что реакции I фазы биотрансформации лекарственных средств обычно являются несинтетическими, тогда как реакции II фазы - синтетические.
Как правило, только после II фазы биотрансформации образуются неактивные или малоактивные соединения, поэтому именно синтетические реакции можно считать исинными реакциями дезинтоксикации ксенобиотиков, в том числе и лекарств.
С практической точки зрения важным является то обстоятельство, что с помощью ряда средств можно активно влиять на процессы микросомального преобразования лекарств. Замечено, что под влиянием лекарственных средств может развиваться как ИНДУЦИРОВАНИЕ (возрастание активности), так и ДЕПРЕССИЯ микрогомальных ферментов. Веществ, стимулирующих биотрансформацию путем индукции синтеза ферментативных белков печени, значительно больше, чем веществ, подавляющих этот синтез. К таким веществами индукторам, которых в настоящее время описано более 200, относят фенобарбитал, барбитураты, гексобарбитал, кофеин, этанол, никотин, бутадион, нейролептики, димедрол, хинин, кордиамин, многие хлорсодержащие пестициды и инсектициды.
В активации этими веществами ферментов печени участвует микросомальная глюкуронилтрансонфаза. При этом возрастает синтез РНК и микросомальных белков. Важно помнить, что индукторами усиливается не только метаболизм лекарств в печени, но и их выведение с желчью.
Все эти вещества ускоряют процессы метаболизма печени в 2-4 раза лишь за счет индуцирования синтеза микросомальных ферментов. При этом ускоряется метаболизм не только вводимых вместе с ними или на их фоне лекарственных препаратов, но и их самих. Однако есть и большая группа веществ (ингибиторы), подавляющих и даже разрушающих цитохром Р-450, то есть основной микросомальный фермент. К числу такимх лекарственных средств относится группа местных анестетиков, антиаритмических средств (анаприлин или индерал, вискен, эралдин), а также циметицин, левомицетин, бутадион, антихолинэстеразные средства, ингибиторы МАО. Эти вещества пролонгируют эффекты препаратов, введенных вместе с ними. Кроме того, многие из ингибиторов вызывают явление аутоингибирования метаболизма (верапамил, пропранолол). Из сказанного следует, что надо при комбинации лекарств у больного учитывать такую возможность. Например, индукция микросомальных ферментов печеночных клеток фенобарбиталом лежит в основе применения этого препарата для устранения гипербилирубинемии у новорожденных с гемолитической болезнью.
Снижение эффективности лекарственных средств при их повторном применении называется толерантностью. Использование того же фенобарбатала в качестве снотворного приводит к постепенному развитию привыкания, т. е. к толерантности, что диктует необходимость повышения дозы лекарства. Особым видом привыкания является тахифилаксия.
ТАХИФИЛАКСИЯ - возникающее очень быстро привыкание, иногда уже после первого введения вещества. Так, введение эфедрина внутривенно повторно с интервалом в 10-20 минут вызывает меньший подъем АД, чем при первой иньекции. Аналогичная ситуация прослеживается при закапывании растворов эфедрина в нос.
Вещества-индукторы, активируя микросомальные ферменты, способствуют усиленному выделению из организма витамина Д, в результате чего может развиться размягчение костей и произойти патологический перелом. Все это примеры взаимодействия лекарств.
Необходимо также помнить, что фармакологические средства можно разделить на 2 группы по скорости инактивации в печени: первые окисляются с малой скоростью, например, дифенин, карбамазенин; вторые - со средней или большой скоростью, например, имизин, изадрин, лидокаин, анаприлин.
Кроме того, метаболизм лекарственных веществ зависит как от вида и рода животных, расовой принадлежности больного, так и от возраста, пола, питания (у вегетарианцев скорость биотрансформации лекарств меньше, если в пище много белков - метаболизм усилен), состояния нервной системы, пути применения, от одновременного использования других лекарственных средств.
Более того, важно помнить, что у каждого человека своя, генетически детерминированная скорость биотрансформации. По этому поводу можно сослаться на пример с алкоголем, когда имеется индивидуальная особенность работы алькогольдегидрогеназы у индивидуума. Эти особенности индивидуальной работы ферментов в зависимости от генотипа изучает фармакогенетика.
Великолепным примером генетической зависимости может служить инактивация противотуберкулезного средства изониазида (фтивазида) путем ацетилирования. Установлено, что скорость этого процесса генетически обусловлена. Имеются лица, которые медленно инактивируют изониазид. При этом его концентрации в организме снижаются более постепенно, чем у людей с быстрой инактивацией препарата. Среди европейской популяции медленных ацетиляторов, по данным некоторых авторов отмечается 50-58, 6%, а быстрых - до 30-41, 4%. При этом, если народы Кавказа и шведы в основном быстрые ацетиляторы, то эскимосы - наоборот - относятся к медленным ацетиляторам.
Зависимость индивидуальной биотрансформации и изучает наука ФАРМАКОГЕНЕТИКА.
У медленных ацетиляторов определенная доза лекарственного средства дает более высокую концентрацию в крови, а потому у них может быть больше побочных эффектов. Действительно изониазид содает у 20% больных с туберкулезом, медленных ацетиляторов, осложнения в виде периферической нейропатии, а у быстрых ацетиляторов - только в 3% случаев.
Заболевания печени меняют биотрансформацию лекарственных веществ в данном органе. Для веществ, медленно трансформирующихся в печени, важную роль играет функция печеночных клеток, уровень активности которых снижается при гепатите, циррозе, уменьшая инактивацию этих веществ. Такие многофакторные особенности биотрансформации лекарств делают необходимым изучение данной проблемы в каждом конкретном случае.
Последним этапом взаимодействия лекарств с живым организмом является их выведение или ЭКСКРЕЦИЯ.
Лекарственные препараты, за исключением препаратов для ингаляционного наркоза, как правило, экскретируются не через те структуры, в которых происходила абсорбция (всасывание). Основными путями экскреции являются почки, печень, ЖКТ, легкие, кожа, слюнные железы, потовые железы, молоко матери. Нас в клиническом плане особенно интересуют почки.
Выведение лекарств почками определяется тремя процессами, осуществляемыми в нефроне:
1) пассивной клубочковой ФИЛЬТРАЦИЕЙ;
2) пассивной диффузией через канальцы или РЕАБСОРБЦИЕЙ;
3) активной канальцевой СЕКРЕЦИЕЙ.
Как видим, для лекарств характерны все физиологические процессы в нефроне. Неионизированные лекарственные вещества, хорошо абсорбирующиеся, могут подвергаться фильтрации в почечных клубочках, но из просвета почечных канальцев они могут вновь диффундировать в клетки, выстилающие канальцы. Таким образом, только очень небольшое количество препарата появляется в моче.
Ионизированные лекарственные вещества, плохо абсорбирующиеся, экскретируются почти полностью путем клубочковой фильтрации и не реабсорбируются.
Пассивная диффузия - двунаправленный процесс, и лекарственные вещества могут диффундировать через стенку канальцев в любом направлении в зависимости от концентрации их и pH среды (например, акрихин, салицилаты).
Значение pH мочи влияет на экскрецию некоторых слабых кислот и оснований. Так, слабые кислоты быстро экиминируются при щелочной реакции мочи, например барбитураты и салицилаты, а слабые основания быстро экскретируются при кислой среде (фенамин). Поэтому при остром отравлении барбитуратами необходимо подщелачивать мочу, что достигается в/венным введением растворов гидрокарбоната натрия (соды), последнее улучшает экскрецию снотворного.
Если же значение pH мочи не соответствует оптимальнму для экскреции лекарственного средства значению, действие этих лекарственных веществ может быть пролонгировано.
При щелочной реакции мочи канальцевая реабсорбция слабых кислот минимальна, так как основная масса этих веществ находится в ионизированном состоянии в щелочной среде. Аналогичная ситуация в отношении слабых оснований при кислой реакции мочи. Выведение слабых оснований и кислот может быть ускорено, если высокий диурез поддерживается введением маннитола и диуретиков (мочегонных), а также корригируется значением pH мочи до оптимального применительно к данному препарату.
При патологии почек способность их экскретировать лекарственные вещества снижается. В результате даже при использовании нормальных доз препаратов уровень их в крови повышается и пролонгируется действие лекарств. В связи с этим при назначении препаратов типа, аминогликозидных антибиотиков (стрептомицин, гентамицин), кумариновых антикоагулянтов, больным со сниженной функцией почек (почечная недостаточность), требуется особый режим наблюдения.
В заключении данного раздела несколько слов о термине «ЭЛИМИНАЦИЯ». В литературе часто термины «элиминация» и «экскреция» употребляют как синонимы. Но необходимо помнить, что ЭЛИМИНАЦИЯ - это более широкий термин, соответствующий сумме всех метаболических (биотрансформация) и экскреторных процессов, в результате которых активное вещество исчезает из организма.
Следствием недостаточности экскреции или элиминации может быть накопление или кумуляция лекарственного средства в организме, в его тканях. Кумуляция - (аккумулятор - накопитель) есть следствие недостаточности экскреции и элиминации, и, как правило, связана с патологией органа экскреции (печени, ЖКТ и др.) или с усилением связывания с белками плазмы, что снижает количество вещества, способного фильтроваться в клубочках.
Имеются три (3) основных пути борьбы с кумуляцией:
1) уменьшение дозы лекарственного вещества;
2) перерыв в назначении лекарств (2-3-4 дня-2 недели);
3) на первом этапе введение большой дозы (дозы насыщения), а потом перевод больного на низкую, поддерживающую дозу. Таким образом, используют, например, сердечные гликозиды (дигитоксин).
Преферанская Нина Германовна
Ст. преподаватель кафедры фармакологии фармацевтического факультета ММА им. И.М. Сеченова
Гепатопротекторы препятствуют разрушению клеточных мембран, предотвращают повреждение печеночных клеток продуктами распада, ускоряют репаративные процессы в клетках, стимулируют регенерацию гепатоцитов, восстанавливают их структуру и функции. Они применяются для лечения острых и хронических гепатитов, жировой дистрофии печени, цирроза печени, при токсических повреждениях печени, в том числе связанных с алкоголизмом, при интоксикации промышленными ядами, лекарственными препаратами, тяжелыми металлами, грибами и других поражениях печени.
Одним из ведущих патогенетических механизмов поражения гепатоцитов является избыточное накопление свободных радикалов и продуктов перекисного окисления липидов при воздействии токсинов экзогенного и эндогенного происхождения, приводя, в конечном итоге, к повреждению липидного слоя клеточных мембран и разрушению клеток печени.
Лекарственные средства, применяемые для лечения заболеваний печени, обладают разными фармакологическими механизмами защитного действия. Гепатопротекторное действие большинства препаратов связывают с ингибированием ферментативного перекисного окисления липидов, с их способностью нейтрализовать различные свободные радикалы, оказывая при этом антиоксидантный эффект. Другие препараты являются строительным материалом липидного слоя клеток печени, оказывают мембраностабилизирующий эффект и восстанавливают структуру мембран гепатоцитов. Третьи индуцируют микросомальные ферменты печени, повышают скорость синтеза и активность этих ферментов, способствуют усилению биотрансформации веществ, активируют метаболические процессы, что способствует быстрому выведению из организма чужеродных токсичных соединений. Четвертые препараты обладают широким спектром биологической активности, содержат комплекс витаминов и незаменимых аминокислот, повышают устойчивость организма к воздействию неблагоприятных факторов, уменьшают токсические эффекты, в том числе и после принятия алкоголя и др.
Выделить препараты с каким-то одним механизмом действия очень трудно, как правило, эти препараты обладают одновременно несколькими из перечисленных выше механизмов. В зависимости от происхождения они подразделяются на препараты: растительного происхождения, синтетические лекарственные средства, животного происхождения, гомеопатические и биологически активные добавки к пище. По составу их различают на монокомпонентные и комбинированные (комплексные) препараты.
Лекарственные средства, преимущественно ингибирующие перекисное окисление липидов
К ним относятся препараты и фитопрепараты плодов расторопши пятнистой (остро-пестрой). Растительные флавоноидные соединения, выделенные из плодов и млечного сока расторопши пятнистой, содержат комплекс изомерных полигидроксифенолхроманонов, главными из которых являются силибинин, силидианин, силикристин и др. Свойства расторопши известны на протяжении более 2000 лет, она использовалась в Древнем Риме для лечения различных отравлений. Гепатопротекторное действие биофлавоноидов, выделенных из плодов расторопши пятнистой обусловлено его антиоксидантными, мембраностабилизирующими свойствами и стимуляцией репаративных процессов в печеночных клетках.
Основным активным биофлавоноидом в расторопше пятнистой является силибинин. Он оказывает гепатопротекторное и антитоксическое действие. Взаимодействует с мембранами гепатоцитов и стабилизирует их, предотвращая потерю трансаминаз; связывает свободные радикалы, ингибирует процессы перекисного окисления липидов, предупреждает разрушение клеточных структур, при этом уменьшается образование малонового диальдегида и поглощение кислорода. Препятствует проникновению в клетку ряда гепатотоксических веществ (в частности, яда бледной поганки). Стимулируя РНК-полимеразу, увеличивает биосинтез белков и фосфолипидов, ускоряет регенерацию поврежденных гепатоцитов. При алкогольных поражениях печени блокирует выработку ацетальдегида и связывает свободные радикалы, сохраняет запасы глутатиона, способствующего процессам детоксикации в гепатоцитах.
Силибинин (Silibinin). Синонимы: Силимарин, Силимарин Седико быстрорастворимый, Силегон, Карсил, Легалон. Выпускается в драже 0,07 г, капсулах 0,14 г и суспензии 450 мл. Силимарин – это смесь изомерных флавоноидных соединений (силибинина, силидианина, силикристина) с преобладающим содержанием силибинина. Биофлавоноиды активируют синтез белков и ферментов в гепатоцитах, воздействуют на метаболизм в гепатоцитах, оказывают стабилизирующее воздействие на мембрану гепатоцитов, ингибируют дистрофические и потенцируют регенеративные процессы в печени. Силимарин препятствует накоплению гидроперекисей липидов, уменьшает степень повреждения клеток печени. Заметно снижает повышенный уровень трансаминаз в сыворотке крови, уменьшает степень жировой дистрофии печени. Стабилизируя клеточную мембрану гепатоцитов, замедляет поступление в них токсических продуктов метаболизма. Силимарин активирует обмен веществ в клетке, результатом чего является нормализация белоксинтетической и липотропной функции печени. Улучшаются показатели иммунологической реактивности организма. Силимарин практически не растворяется в воде. Благодаря слабокислым свойствам, может образовывать соли со щелочными веществами. Более 80% препарата выделяется с желчью в виде глюкуронидов и сульфатов. В результате расщепления кишечной микрофлорой выделившегося с желчью силимарина до 40% вновь реабсорбируется, что создает его кишечно-печеночный кругооборот.
Силибор – препарат, содержащий сумму флавоноидов из плодов расторопши пятнистой (Silibbum marianum L). Форма выпуска: таблетки, покрытые оболочкой по 0,04 г.
Силимар , сухой очищенный экстракт, получаемый из плодов расторопши пятнистой (Silybum marianum L), содержит флаволигнаны (силибинин, силидианин и др.), а также другие вещества, в основном флавоноиды, 100 мг в одной таблетке. Силимар обладает рядом свойств, обусловливающих его защитное действие на печень при воздействии различных повреждающих агентов. Он проявляет антиоксидантные и радиопротекторные свойства, усиливает детоксикационную и внешнесекреторную функции печени, оказывает спазмолитическое и небольшое противовоспалительное действие. При острой и хронической интоксикации, вызываемой четыреххлористым углеродом, Силимар оказывает выраженное гепатозащитное действие: подавляет нарастание индикаторных ферментов, тормозит процессы цитолиза, препятствует развитию холестаза. У больных с диффузными поражениями печени, в том числе алкогольного генеза, препарат нормализует функционально-морфологические показатели гепатобилиарной системы. Силимар уменьшает жировую дегенерацию клеток печени и ускоряет их регенерацию за счет активации РНК-полимеразы.
Гепатофальк планта – комплексный препарат, содержащий экстракты из плодов расторопши, чистотела и термелика. Фармакологический эффект комбинированного растительного препарата определяется совокупным действием его компонентов. Препарат оказывает гепатопротективное, спазмолитическое, анальгезирующее, желчегонное (холеретическое и холекинетическое) действие. Стабилизирует мембраны гепатоцитов, повышает синтез белка в печени; оказывает отчетливое спазмолитическое действие на гладкую мускулатуру; обладает антиоксидантной, противовоспалительной и антибактериальной активностью. Препятствует проникновению в клетку ряда гепатотоксических веществ. При алкогольных поражениях печени блокирует выработку ацетальдегида и связывает свободные радикалы, сохраняет запасы глутатиона, способствующего процессам детоксикации в гепатоцитах. Алкалоид хелидонин, содержащийся в чистотеле, обладает спазмолитическим, анальгезирующим и желчегонным действием. Куркумин – действующее вещество термелика яванского оказывает желчегонное (как холеретическое, так и холекинетическое) и противовоспалительное действие, снижает насыщенность желчи холестерином, обладает бактерицидной и бактериостатической активностью в отношении золотистого стафилококка, сальмонелл и микобактерий.
Гепабене содержит экстракт расторопши пятнистой со стандартизированным количеством флавоноидов: 50 мг силимарина и не менее 22 мг силибинина, а также экстракт дымянки аптечной, содержащей не менее 4,13 мг алкалоидов дымянки аптечной в пересчете на протопин. Лечебные свойства Гепабене определяются оптимальным сочетанием гепатопротекторного действия экстракта расторопши пятнистой и нормализующего секрецию желчи и моторику желчевыводящих путей влияния дымянки аптечной Основным действующим веществом дымянки лекарственной является производное фумаровой кислоты – алкалоид протопин. Нормализует как слишком слабое, так и повышенное желчевыделение, снимает спазм сфинктера ОДДИ, нормализует моторную функцию желчевыводящих путей при их дискинезии, как по гиперкинетическому, так и по гипокинетическому типу. Эффективно восстанавливает дренажную функцию желчевыводящих путей, предупреждая развитие застоя желчи и образование конкрементов в желчном пузыре. При приеме препарата может возникать послабляющее действие и увеличиваться диурез. Выпускается в капсулах. Применяют внутрь, во время еды по одной капсуле 3 раза в сутки.
Сибектан , в одной таблетке которого содержится: экстракт из пижмы, жома плодов расторопши пятнистой, зверобоя, березы по 100 мг. Препарат оказывает мембраностабилизирующее, регенерирующее, антиоксидантное, гепатопротекторное и желчегонное действие. Нормализует липидный и пигментный обмен, усиливает детоксикационную функцию печени, тормозит процессы липопероксидации в печени, стимулирует регенерацию слизистых оболочек и нормализует моторику кишечника. Принимают за 20–40 мин. до еды по 2 таблетки 4 раза в сутки. Курс 20–25 дней.
Лекарственные средства, преимущественно восстанавливающие структуру мембран гепатоцитов и оказывающие мембраностабилизирующий эффект Повреждение гепатоцитов часто сопровождается нарушением целостности мембран, это приводит к попаданию ферментов из поврежденной клетки в цитоплазму. Наряду с этим повреждаются межклеточные связи, ослабевает связь между отдельными клетками. Нарушаются важные процессы для организма – всасывание триглицеридов, необходимых для образования хиломикронов и мицелл, снижается желчеобразование, продукция белков, нарушается обмен веществ и способность гепатоцитов выполнять барьерную функцию. При приеме препаратов этой подгруппы происходит ускорение регенерации клеток печени, усиливается синтез белков и фосфолипидов, которые являются пластическим материалом мембран гепатоцитов, нормализуется обмен фосфолипидов клеточных мембран. Эти препараты проявляют антиоксидантное действие, т.к. в печени взаимодействуют со свободными радикалами и переводят их в неактивную форму, что препятствует дальнейшему разрушению клеточных структур. В состав данных препаратов входят эссенциальные фосфолипиды, которые являются пластическим материал для поврежденных клеток печени, состоящих на 80% из гепатоцитов.
Эссенциале Н и эссенциале форте Н . Выпускается в капсулах, содержащих по 300 мг «эссенциальных фосфолипидов», для приема внутрь во время еды. Препарат обеспечивает печень высокой дозой готовых к усвоению фосфолипидов, которые проникают в клетки печени, внедряются в мембраны гепатоцитов и нормализуют ее функции, в том числе и детоксикационную. Восстанавливается клеточная структура гепатоцитов, тормозится формирование соединительной ткани в печени, все это способствует регенерации печеночных клеток. Ежедневный прием препарата способствует активации фосфолипидзависимых ферментных систем печени, уменьшает уровень энергозатрат, улучшает метаболизм липидов и белков, преобразует нейтральные жиры и холестерин в легко метаболизирующиеся формы, стабилизируются физико-химические свойства желчи. При острых и тяжелых формах поражения печени (печеночная предкома и кома, некроз клеток печени и токсические ее поражения, при операциях в области гепатобиларной зоны и др.) используют раствор для внутривенного медленного введения в ампулах из темного стекла по 5 мл, содержащий 250 мг «эссенциальных фосфолипидов». Вводят 5–10 мл в день, при необходимости дозу увеличивают до 20 мл/день. Нельзя смешивать с другими препаратами.
Эссливер форте – комбинированный препарат, содержащий эссенциальные фосфолипиды 300 мг и комплекс витаминов: тиамина мононитрат, рибофлавина, пиридоксина, токоферола ацетата по 6 мг, никотинамида 30 мг, цианкобаламина 6 мкг, оказывает гепатопротекторное, гиполипидемическое и гипогликемическое действие. Регулирует проницаемость биомембран, активность мембраносвязанных ферментов, обеспечивая физиологическую норму процессов окислительного фосфорилирования в клеточном метаболизме. Восстанавливает мембраны гепатоцитов путем структурной регенерации и методом конкурентного ингибирования перекисных процессов. Ненасыщенные жирные кислоты, встраиваясь в биомембраны, принимают на себя токсикогенные воздействия вместо мембранных липидов печени и нормализуют функцию печени, повышают ее дезинтоксикационную роль.
Фосфоглив – в одной капсуле содержится 0,065 г фосфатидилхолина и 0,038 г динатриевой соли глицерризиновой кислоты. Препарат восстанавливает клеточные мембраны гепатоцитов с помощью глицерофосфолипидов. В молекуле фосфатидилхолина соединены глицерин, высшие жирные кислоты, фосфорная кислота и холин, все необходимые вещества для построения клеточных мембран. Молекула глициризиновой кислоты схожа со строением гормонов коры надпочечников (например, кортизоном), за счет этого она обладает противовоспалительными и антиаллергическими свойствами, обеспечивает эмульгирование фосфатидилхолина в кишечнике. Содержащаяся в ее структуре глюкуроновая кислота связывает и инактивирует образующиеся токсичные продукты. Применяют внутрь по 1–2 капсулы 3 раза в сутки в течение месяца. Дозу можно увеличит до 4 капсул за один прием и 12 капсул в сутки.
Ливолин форте – комбинированный препарат, в одной капсуле которого содержится 857,13 мг лецитина (300 мг фосфатидилхолина) и комплекс необходимых витаминов: Е, В1, В6 – по 10 мг, В2 – 6 мг, В12 – 10 мкг и РР – 30 мг. Входящие в состав фосфолипиды являются основными элементами в структуре клеточной оболочки и митохондрий. При применении препарата регулируется липидный и углеводный обмен, улучшается функциональное состояние печени, активируется ее важнейшая детоксикационная функция, сохраняется и восстанавливается структура гепатоцитов, тормозится формирование соединительной ткани печени. Входящие витамины выполняют функцию коэнзимов в процессах окислительного декарбоксилирования, дыхательного фосфорилирования, обладают антиоксидантным действием, защищают мембраны от воздействия фосфолипаз, препятствуют образованию перекисных соединений и ингибируют свободные радикалы. Применяют по 1–2 капсулы 2–3 раза в день во время еды, курс 3 месяца, при необходимости курс повторяют.
Препараты, улучшающие метаболические процессы в организме Они обеспечивают детоксикацию клеток, стимулируют регенерацию клеток за счет повышения активности микросомальных ферментов печени, улучшения микроциркуляции и питания клеток, а также улучшают метаболические процессы в гепатоцитах.
Средство, влияющее на метаболические процессы, Тиоктовая кислота (липоевая кислота, липамид, тиоктацид). Фармакологическое действие – гиполипидемическое, гепатопротективное, гипохолестеринемическое, гипогликемическое. Тиоктовая кислота участвует в окислительном декарбоксилировании пировиноградной и a-кетокислот. По характеру биохимического действия она близка к витаминам группы В. Участвует в регулировании липидного и углеводного обмена, стимулирует обмен холестерина, улучшает функцию печени. Применяют внутрь, в начальной дозе 200 мг (1 таблетка) 3 раза в сутки, поддерживающая доза 200–400 мг/сут. При применении препарата могут наблюдаться диспепсия, аллергические реакции: крапивница, анафилактический шок; гипогликемия (в связи с улучшением усвоения глюкозы). При тяжелых формах диабетической полинейропатии вводят в/в по 300–600 мг или в/в капельно, в течение 2–4 нед. В дальнейшем переходят на поддерживающую терапию таблетированными формами – 200–400 мг/сут. После в/в введения возможны побочные нежелательные реакции – такие, как развитие судорог, диплопии, точечных кровоизлияний в слизистые и кожу, нарушение функции тромбоцитов; при быстром введении ощущение тяжести в голове, затруднение дыхания.
Альфа-липоевая кислота является коферментом окислительного декарбоксилирования пировиноградной кислоты и альфа-кетокислот, нормализует энергетический, углеводный и липидный обмены, регулирует метаболизм холестерина. Улучшает функции печени, снижает повреждающее влияние на нее эндогенных и экзогенных токсинов. Применяют внутрь в/м и в/в. При в/м инъекции доза, вводимая в одно место, не должна превышать 2 мл. В/в введение капельное, предварительно разбавив 1–2 мл 250 мл 0,9% раствора натрия хлорида. При тяжелых формах полинейропатии – в/в по 12–24 мл ежедневно в течение 2–4 нед., затем переходят на поддерживающую терапию внутрь 200–300 мг/сут. Препарат светочувствителен, поэтому ампулы из упаковки необходимо доставать только непосредственно перед использованием. Раствор для инфузии пригоден для введения в течение 6 час., если он защищен от воздействия света.
Эспа-липон выпускается в таблетках, покрытых оболочкой и в растворах для инъекций. Одна таблетка содержит 200 мг или 600 мг, этилендиаминовой соли альфа-липоевой кислоты, а в 1 мл раствора его содержится 300 мг или 600 мг, ампулы соответственно по 12 мл и 24 мл. При применении препарата происходит стимулирование окислительного декарбоксилирования пировиноградной кислоты, a-кетокислот, регулирование липидного и углеводного обмена, улучшаются функции работы печени, происходит защита от неблагоприятного действия эндо- и экзо-факторов.
Адеметионин (Гептрал) является предшественником физиологических тиоловых соединений, участвующих в многочисленных биохимических реакциях. Это эндогенное вещество, обнаруженное почти во всех тканях и жидкостях организма, получено синтетическим путем, обладает гепатопротективным, детоксикационным, регенерирующим, антиоксидантным, антифиброзирующим и нейропротекторным действием. Его молекула включена в большинство биологических реакций, в т.ч. как донор метильной группы в реакциях метилирования, в составе липидного слоя клеточной мембраны (трансметилирование); как предшественник эндогенных тиоловых соединений – цистеина, таурина, глютатиона, коэнзима А (транссульфатирование); как предшественник полиаминов – путресцина, стимулирующего регенерацию клеток, пролиферацию гепатоцитов, спермидина, спермина, входящих в структуру рибосом (аминопропилирование). Обеспечивает окислительно-восстановительный механизм клеточной детоксикации, стимулирует детоксикацию желчных кислот – повышает содержание в гепатоцитах конъюгированных и сульфатированных желчных кислот. Стимулирует синтез в них фосфатидилхолина, повышает подвижность и поляризацию мембран гепатоцитов. Гептрал включается в биохимические процессы организма, одновременно стимулируя выработку эндогенного адеметионина, в первую очередь в печени и мозге. Проникая через гематоэнцефалический барьер, проявляет антидепрессивное действие, которое развивается в первую неделю и стабилизируется в течение второй недели лечения. Терапия гептралом сопровождается исчезновением астенического синдрома у 54% пациентов и уменьшением его интенсивности у 46% больных. Антиастенический, антихолестатический и гепатопротективный эффекты сохранялись в течение 3 месяцев после прекращения лечения. Выпускается в таблетках по 0,4 г лиофилизированного порошка. Поддерживающая терапия внутрь 800–1600 мг/сут. между приемами пищи, глотать, не разжевывая, желательно в первой половине дня. При интенсивной терапии в первые 2–3 недели лечения назначают в/в 400–800 мг/сут. (очень медленно) или в/м, порошок растворяют только в специальном прилагаемом растворителе (раствор L-лизина). Основные побочные эффекты при приеме внутрь – изжога, боль или неприятные ощущения в эпигастральной области, диспептические явления, возможны аллергические реакции.
Орнитина аспартат (гепа-Мерц гранулы) . Фармакологическое действие – дезинтоксикационное, гепатопротективное, способствует нормализации КОС организма. Участвует в орнитиновом цикле мочевинообразования (образование мочевины из аммиака), утилизирует аммонийные группы в синтезе мочевины и снижает концентрацию аммиака в плазме крови. При приеме препарата активируется выработка инсулина и соматотропного гормона. Препарат выпускается в гранулах для приготовления растворов, для приема внутрь. 1 пакетик содержит 3 г орнитина аспартата. Применяют внутрь, по 3–6 г 3 раза в сутки после еды. Концентрат для инфузий, в ампулах по 10 мл, в 1 мл которого содержится 500 мг орнитина аспартата. Вводят в/м по 2–6 г/сут. или в/в струйно по 2–4 г/сут.; кратность введения 1–2 раза в сутки. При необходимости в/в капельно: 25–50 г препарата разводят в 500–1500 мл изотонического раствора натрия хлорида, 5% раствора глюкозы или дистиллированной воды. Максимальная скорость инфузии 40 кап./мин. Продолжительность курса лечения определяется динамикой концентрации аммиака в крови и состоянием больного. Курс лечения можно повторять каждые 2–3 мес.
Гепасол А , комбинированный препарат, в 1 л раствора содержится: 28,9 г L-аргинина, 14,26 г L-яблочной кислоты, 1,33 г L-аспарагиновой кислоты, 100 мг никотинамида, 12 мг рибофлавина и 80 мг пиридоксина.
Действие основано на влиянии L-аргинина и L-яблочной кислоты на процессы метаболизма и обмена веществ в организме. L-аргинин способствует превращению аммиака в мочевину, связывает токсичные ионы аммония, образующиеся при катаболизме белков в печени. L-яблочная кислота необходима для регенерации L-аргинина в этом процессе и в качестве энергетического источника для синтеза мочевины. Рибофлавин (В2) превращается во флавин-мононуклеотид и флавин-аденин-динуклеотид. Оба метаболита фармакологически активны и в составе коферментов играют важную роль в окислительно-восстановительных реакциях. Никотинамид переходит в депо в форме пиридин нуклеотида, который играет важную роль в окислительных процессах организма. Совместно с лактофлавином никотинамид участвует в промежуточных процессах метаболизма, в форме трифосфопиридина нуклеотида – в синтезе белка. Снижает уровень сывороточных липопротеинов очень низкой плотности и низкой плотности и в тоже время повышает уровень липопротеинов высокой плотности, поэтому используется в терапии гиперлипидемий. D-пантенол, как кофермент А, являясь основой промежуточных процессов метаболизма, участвует в метаболизме углеводов, глюконеогенезе, катаболизме жирных кислот, в синтезе стерола, стероидных гормонов и порфирина. Пиридоксин (В6) является составной частью групп многих ферментов и коферментов, играет значительную роль в процессах метаболизма углеводов и жиров, необходим для образования порфирина, а также синтеза Hb и миоглобина. Терапия устанавливается индивидуально, с учетом исходной концентрации аммиака в крови и назначается в зависимости от динамики состояния больного. Обычно назначают в/в капельное введение 500 мл раствора со скоростью 40 кап./мин. Введение препарата может повторяться каждые 12 ч и до 1,5 л в сутки.
Аргинин содержится в гепатопротекторных препаратах Сарженор и Цитраргин .
Цитрат бетаина Бофур – в его состав входит бетаин и цитрат (анион лимонной кислоты). Бетаин – аминокислота, производное глицина с метилированной аминогруппой, присутствующая в печени и почках человека, основной липотропный фактор. Способствует профилактике жирового перерождения печени и снижает уровень холестерина в крови, увеличивает дыхательные процессы в пораженной клетке. Цитрат представляет собой важное звено в цикле трикарбоновых кислот (цикл Кребса). Выпускается в гранулах по 250 г для приема внутрь.
К индукторам микросомальных ферментов печени относятся также флумецинол (зиксорин) и производное барбитуровой кислоты фенобарбитал, обладающий противосудорожным и снотворным действием.
Препараты животного происхождения Гепатамин , комплекс белков и нуклеопротеидов, выделенных из печени крупного рогатого скота; Сирепар – гидролизат экстракта печени; Гепатосан – препарат, получаемый из печени свиньи.
Препараты животного происхождения, содержат комплекс белков, нуклеотидов и других активных веществ, выделенных из печени крупного рогатого скота. Они нормализуют метаболизм в гепатоцитах, повышают ферментативную активность. Обладают липотропным эффектом, способствуют регенерации паренхиматозной ткани печени и оказывают детоксикационное действие.
Растительное сырье для улучшения функции печени и пищеварения
Лив-52 , содержащий соки и отвары многих растений, обладает гепатотропным действием, способствует улучшению функции печени, аппетита и отхождению газов из кишечника.
Тыквеол содержит жирное масло, полученное из семян тыквы обыкновенной, в состав которого входят каротиноиды, токоферолы, фосфолипиды, флавоноиды; витамины: В1, В2,С, Р, РР; жирные кислоты: насыщенные, ненасыщенные и полинасыщенные – пальмитиновая, стеариновая, олеиновая, линолевая, линоленовая, арахидоновая и др. Препарат оказывает гепатопротекторное, антиатеросклеротическое, антисептическое, желчегонное действие. Выпускается во флаконах по 100 мл и в пластиковых флаконах-капельницах по 20 мл. Применяют по 1 ч. ложке за 30 мин. до еды 3–4 раза в день, курс лечения 1–3 месяца.
Бонджигар выпускается в сиропе и твердых желатиновых капсулах, содержит смесь растительных компонентов, обладающих противовоспалительным, гепатопротекторным, мембраностабилизирующим, детоксицирующим и липотропным действием. Предотвращает поражение и нормализует функции печени, защищает ее от действия повреждающих факторов и накопления токсических продуктов метаболизма. Применяют внутрь, после еды, по 2 столовые ложки сиропа или 1–2 капсулы 3 раза в день в течение 3 недель.
Гомеопатические препараты
Гепар композитум – комплексный препарат, содержащий фитокомпоненты: Lycopodium и Carduus marianus, суис-органные препараты печени, поджелудочной железы и желчного пузыря, катализаторы и серу, поддерживает метаболические функции печени.
Хепель – в состав этого препарата входит расторопша пятнистая, чистотел, плаун булавовидный, чемерица, фосфор, колоцинт и др. Антигомотоксический препарат обладает антиоксидантной активностью, защищает гепатоциты от повреждения свободных радикалов, а также антипролиферативным и гепатопротекторным действием. Выпускается в таблетках, применяют под язык по 1 таблетке 3 раза в день.
Комплексный гомеопатический препарат Галстена применяется в комплексном лечении острых и хронических заболеваний печени, заболеваний желчного пузыря (хронический холецистит, постхолецистэктомический синдром) и хронического панкреатита. Выпускается во флаконах по 20 мл. Назначают детям до 1 года по 1 капле, до 12 лет – 5 капель, взрослым – 10 капель. В острых случаях возможен прием каждые полчаса-час до наступления улучшения состояния, но не более 8 раз, после чего принимать 3 раза в день.
Биологически активные добавки к пище (БАД) Овесол – комплексный препарат, содержащий вытяжку овса молочной спелости в сочетании с желчегонными травами и маслом куркумы. Выпускается в виде капель по 50 мл и таблеток по 0,25 г. Ежедневный прием препарата по 1 таблетке 2 раза во время еды в течение месяца улучшает дренажные функции желчевыводящих путей, устраняет застой и нормализует биохимический состав желчи, препятствует образованию желчных камней. БАД бережно очищает печень от шлаков и токсичных продуктов эндогенного и экзогенного происхождения, улучшает метаболическую функцию печени, способствует вымыванию песка.
Гепатрин – в его составе три главных компонента: экстракт расторопши, экстракт артишока и эссенциальные фосфолипиды. БАД применяется с профилактической целью, для защиты клеток печени от повреждения при применении лекарств, алкоголя, от неблагоприятного воздействия эндо-, экзотоксинов и употребления чрезмерно жирной пищи. Выпускается в капсулах по 30 штук.
Эссенциал ойл – высококачественный рыбий жир, полученный из гренландского лосося методом холодной обработки и стабилизированный от окисления витамином Е. В одной капсуле содержатся: ненасыщенные жирные кислоты (омега-3): 180 мг эйкзапентаеновой кислоты, 120 мг докозагексаеновой к-ты и 1мг D-альфа-токоферола. В качестве БАД употреблять взрослым по 1–3 капсуле в день во время еды. Курс приема 1 месяц.
Гепавит Лайф формула содержит комплекс витаминов группы В и жирорастворимые витамины А, Е, К, фосфолипидный комплекс, активирующий функции печени, активные компоненты растительного сырья, обладающие антиоксидантным, желчегонным, детоксикационным действием. Выпускается в капсулах (таблетках), применяют по 1 капс. (табл.) 1–2 раза в сутки.
Тыквэйнол – БАД , изготовленная на основе пищевых масел морского и растительного происхождения – эйконола и тыквеола, полученных по отечественным технологиям с использованием щадящих режимов переработки сырья. Тыквэйнол содержит комплекс биологически активных веществ: насыщенные и полиненасыщенные жирные кислоты – эйкозапентаеновую, докозагексаеновую, линоленовую, линолевую, пальмитиновую, стеариновую, арахидоновую и др., каротиноиды, токоферолы, фосфолипиды, стерины, фосфатиды, флавоноиды, витамины А, D, Е, F, В1, В2, С, Р, РР. Благодаря сочетанию активных соединений морского и растительного происхождения способствует очищению организма от жировых и известковых отложений, улучшению кровообращения, повышению эластичности кровеносных сосудов, укреплению сердечной мышцы, предупреждению инфаркта миокарда, улучшению зрения, исчезает шум в голове, а также оказывает гепатопротекторное, желчегонное, противоязвенное, антисептическое действие; тормозит чрезмерное развитие клеток предстательной железы; способствует снижению воспалительных процессов и ускорению регенерации тканей при заболеваниях слизистой желудочно-кишечного тракта, слизистой полости рта, желчевыводящих путей, мочеполовой системы и кожи. При приеме БАД улучшается состав желчи, нормализуется нарушенное функциональное состояние желчного пузыря, снижается риск возникновения желчекаменной болезни и холецистита. Нормализует секреторную и моторноэвакуаторную функции желудка и улучшает обмен веществ. При лечебном приеме необходимо уменьшить содержание растительного масла в суточном рационе на 10 г. С профилактической целью Тыквэйнол рекомендуется употреблять курсами по 2 г в день в течение не менее 1 месяца два раза в год, в осенне-зимний и весенний периоды года. Особенно необходим Тыквэйнол людям, подверженным умственным и физическим перегрузкам, студентам и школьникам для повышения обучаемости и толерантности к нагрузкам. В дозе по 1 г в день Тыквэйнол полезен всем здоровым людям для профилактики.
Ливер Райт содержит экстракта печени 300 мг, холина битартрат 80 мг, экстракта расторопши 50 мг, инозитола 20 мг; цистеина 15 мг; витамина В12 6 мкг. Предупреждает гепатотоксическое действие ацетальдегида, продукта метаболизма алкоголя, восстанавливает клеточные эндоплазматические мембраны, состоящие из фосфоглицеридов, синтезируемых на основе инозитола и холина, снижает уровень молочной кислоты в крови за счет улучшения метаболизма при участии цистеина, способствует накоплению глютатиона в результате действия цистеина, что предупреждает перекисное окисление липидов, улучшает мик
Это действие препарата в месте его приложения +может привести к рефлекторному ответу +может быть побочным -это разновидность резорбтивного действия
Это всегда побочное действие -определяется дозой вещества +определяется концентрацией вещества
Действие вещества развивающееся после его поступления в системный кровоток называется :
Резорбтивным -рефлекторным -этиотропным -местным +общим
Факторы воздействующие на лекарство в желудке :
Пепсин -панкреатические ферменты +кислая среда -умеренно щелочная среда -фермент инсулиназа
Количество лекарства, поступившее в системный кровоток -соотношение между назначенной дозой и массой человека +предположительный объем жидкости организма, необходимый для равномерного распределения введенной дозы лекарственного вещества +отношение между принятой дозой и концентрацией вещества в крови
Объем крови, в котором растворено лекарство
Любому прямому действию +действию нежелательному в процессе лечения -любому рефлекторному
Синергистическому -антагонистическое +идиосинкразии +действию, вызывающему аллергию
Перенос лекарства через мембрану со стороны низкой
концентрации в пространство с большей концентрацией осуществляется :
Пассивной диффузией -облегченной диффузией -пиноцитозом +активным транспортом
Транспортом с затратами энергии -фагоцитозом +транспортом с участием переносчиков
Биологический смысл реакций биотрансформации с участием цитохромов Р -450:
Окислить молекулу лекарственного вещества
Ацетилирование лекарственного вещества означает :
Присоединение остатка уксусной кислоты с участием ацетил-КоА -присоединение глюкуроновой кислоты -синоним микросомального окисления -то же, что и гидролиз -присоединение гидроксильных групп +вид конъюгации
Вид химического превращения, происходящего в печени
Быстрее обезвреживаются печенью +меньше обезвреживаются печенью +имеют другие показатели биодоступности +не разрушаются ферментами ЖКТ
Легче проникают через гематоэнцефалический барьер
К понятию « полипрагмазия » имеет отношение следующее явление :
Сенсибилизация -толерантность
Необоснованное назначение большого количества лекарств -абстиненция -идиосинкразия
Процессам микросомального окисления веществ в печени присущи следующие черты :
Способность к индукции +возможность ингибирования +неспецифичность субстрата
Строгая химическая специфичность субстрата -присоединение метильных радикалов -присоединение остатка уксусной кислоты
Термин « привыкание » соответствует :
Усилению действия лекарства при повторном введении -понятию «лекарственная зависимость» +понятию «толерантность»
Ослаблению действия лекарства при повторном применении -понятию «абстиненция»
Выберите вариант ответа который соответствует наиболее быстрому удалению лекарства почками :
Вещество слабо фильтруется и слабо реабсорбируется -вещество хорошо фильтруется и хорошо реабсорбируется
Вещество хорошо фильтруется и секретируется канальцами, но не
реабсорбируется -вещество хорошо фильтруется, хорошо реабсорбируется и секретируется канальцами
Привыкание к лекарственному веществу может быть следствием :
Индукции микросомальных ферментов печени -подавления цитохромов Р-450 -повышения чувствительности рецепторов
Снижения чувствительности рецепторов органов - мишеней -снижения метаболизма данного лекарственного вещества
Если какое - то вещество ингибирует систему микросомального окисления печени то можно ожидать :
Снижения скорости метаболизма лекарств +пролонгирования эффекта препаратов +возможной кумуляции веществ -укорочения периода элиминации
Снижения эффективности действия препаратов
Индукция микросомальных ферментов печени может :
Потребовать уменьшения дозы некоторых веществ +потребовать увеличения дозы некоторых веществ
Способствовать проникновению веществ через гемато-
энцефалический барьер +способствовать удалению чужеродных веществ из организма
Препятствовать удалению чужеродных веществ из организма
Лекарственное средство попадает в кровоток минуя печеночный барьер при применении в виде :
Капсул +таблеток под язык
Внутривенных инъекций -настоев внутрь +ингаляций
Ускорение выведения лекарственного вещества с мочой достигается при :
Увеличении фильтрации в клубочках -усилении канальцевой реабсорбции -применении альдостерона и вазопрессина +активации канальцевой секреции в почках
Повышении степени связывания лекарства с белками
Понятие « фармакокинетика » включает :
Абсорбцию вещества +распределение вещества в организме +биотрансформацию вещества -взаимодействие с рецепторами -эффекты действия -механизм действия +экскрецию вещества +период полужизни вещества
Механизм побочных эффектов вещества
При назначении ацетилсалициловой кислоты наряду с
противовоспалительным действием может возникнуть язва желудка . Этот эффект можно охарактеризовать как :
Симптоматическое действие +побочное действие -канцерогенность -эмбриотоксичность +ульцерогенное действие
Понятие « гистогематические барьеры » включает :
Гематоофтальмический барьер -мембраны лизосом +плацентарный барьер +гематоэнцефалический барьер
Пресистемная элиминация лекарства – это :
Процесс удаления вещества из крови почками +удаление лекарства до его попадания в общий кровоток -секреция вещества железами желудка
Биотрансформация вещества в печени после всасывания в кровь
Пролонгирование эффектов лекарственных веществ достигается при :
Создании депо в жировой ткани -нарушении всасывания в кишечнике +увеличении связывания с белками плазмы
Повышении клубочковой фильтрации в почках -усилении биотрансформации в печени
Вторичными внутриклеточными посредниками в действии лекарств могут быть :
Циклические нуклеотиды (цАМФ, цГМФ) -активаторы ионных каналов +ионы кальция -аденилатциклаза
Процесс метаболической трансформации лекарств включает :
Окисление -метилирование
Восстановление +гидролиз -ацетилирование
Реакция конъюгации лекарств подразумевает :
Окисление +взаимодействие с глюкуроновой кислотой
Взаимодействие с глутатионом +ацетилирование -взаимодействие с хлористоводородной кислотой -гидролиз
Понятие « аффинитет » подразумевает :
Способность образовывать комплексы с циторецепторами -вид комбинированного действия лекарств +сродство вещества к рецептору
Способность вещества вызывать сенсибилизацию организма
К вторичным передатчикам (« мессенджерам ») относятся :
Циклические нуклеотиды (цАМФ, цГМФ) -аденилатциклаза +диацилглицерол (ДАГ)
Лиганды мембранных рецепторов +ионизированный кальций +инозитол 1,4,5-трифосфат (НФ3)
К препаратам - дженерикам относятся :
Оригинальные препараты, впервые появившиеся на фармацевтическом рынке +воспроизведенные лекарственные препараты
Наиболее дорогие препараты из данной фармакологической группы -препараты, классифицируемые по особенностям своего химического строения
Учитывая существенную роль ферментов эндоплазматического ретикулюма в инактивации чужеродных веществ, метаболические превращения лекарственных веществ подразделяют на превращения, которые катализируются микросомальными ферментами печени (и, возможно, ферментами других тканей) и на превращения, которые катализируются ферментами, локализованными в других частях клетки (немикросомальные).
В состав микросомальных ферментов входят оксидазы со смешанными функциями (их еще называют микросомальными монооксигеназами или ферментами свободного окисления), а также различные эстеразы (глюкозо-6-фосфатаза, магний-зависимые нуклеозидфосфатазы, неспецифические эстеразы), ферменты синтеза белков, липидов, фосфолипидов, гликопротеидов, желчных кислот, наконец, ферменты, катализирующие реакции конъюгации. Из их числа в механизмах детоксикации ксенобиотиков (и в том числе лекарств) участвуют:
Оксидазы со смешанными функциями (т.е. микросомальные оксигеназы);
Эстеразы;
Ферменты конъюгации.
Таким образом микросомальные ферменты, в основном, осуществляют окисление, восстановление, гидролиз и конъюгацию ксенобиотиков (в т.ч. лекарств).
Микросомальные монооксигеназы катализируют биотрансформацию преимущественно липотропных ксенобиотиков, а ткаже эндогенных стероидов, ненасыщенных жирных кислот, простагландинов. Эти монооксигеназы, участвуя в метаболизме липотропных ядов и лекарственных веществ, катализируют такие реакции окисления, как С-гидроксилирование в алифатической цепи, в ароматическом и алициклическом кольцах, в алкильных боковых цепях, N-гидроксилирование, O-, N-, S-дезалкилирование, окислительное дезаминирование, дезамидирование и эпоксидирование.
Помимо окислительных превращений, эти ферменты катализируют реакции восстановления ароматических нитро- и азосоединений, реакции восстановительного дегалогенирования. В результате этих реакций ксенобиотики приобретают реактивные группы - -ОН, -СООН, -NН 2 , -SН и др. Образующиеся таким путем метаболиты легко вступают в реакцию конъюгации с образованием малотоксичных соединений, которые затем выводятся из организма, в основном с мочой, желчью и калом.
Микросомальные монооксигеназы представляют собой полиферментный комплекс, локализованный на гладком эндоплазматическом ретикулуме и связанный с двумя внемитохондриальными цепями переноса электронов, генерирующих восстановленные формы НАДФ и НАД. Источником НАДФ.Н 2 служит главным образом пентозофосфатный цикл, а НАД.Н 2 - гликолиз.
Общим самоокисляющимся (аутооксидабельным) звеном этих полифемерментных комплексов является цитохром Р-450. В состав этого комплекса входят также цитохром в 5 , НАДФ.Н-цитохром-Р-450-редуктаза (ФП 1) и НАД.Н-цитохром в 5 -редуктаза (ФП 2).
Цитохром Р 450 представляет собой гемсодержащий белок, широко распространенный в тканях животных и растений. Он локализован в глубоких слоях мембран эндоплазматической сети. При взаимодействии с СО восстановленный цитохром образует карбонильный комплекс, характеризующийся полосой поглощения при 450 нм, что и определило название фермента. Цитохрому Р 450 присуще многообразие изоформ и широта субстратной специфичности. Эту широту субстратной специфичности характеризуют как специфичность к гидрофобности веществ.
Цитохром Р 450 является важнейшим компонентом микросомальной монооксигеназной системы. Этот фермент отвечает за активацию молекулярного кислорода (путем переноса на него электронов) и за связывание субстрата. Цитохром Р450 использует активированный кислород для окисления субстрата и образования воды.
Другой компонент микросомальной монооксигеназной системы НАДФ*Н 2 цитохромР 450 редуктаза (ФП 1) служит переносчиком электронов с НАДФ*Н 2 на цитохром Р 450 . Этот фермент - флавопротеид, содержащий ФАД и ФМН, связан с фракцией поверхностных мембранных белков эндоплазматического ретикулума. Этот фермент способен передавать электроны не только на цитохром Р 450 , но и на другие акцепторы (на цитохром в 5 , цитохром с).
Цитохром в 5 представляет собой гемопротеид, который, в отличие от цитохрома Р 450 , локализирован в основном на поверхности мембран эндоплазматического ретикулума. Цитохром в 5 способен получать электроны не только от НАДФ*Н 2 , но и от НАД*Н 2 участвуя в функционировании НАД*Н 2 -зависимой цепи транспорта электронов.
В состав этой цепи также входит фермент НАД*Н 2 -цитохром-В 5 -редуктаза (ФП 2).
Этот фермент, так же как и цитохром В 5 , не фиксирован строго на определенных участках мембраны эндоплазматической сети, а способен менять свою локализацию, передавая электроны с НАД*Н 2 на цитохром В 5 .
В процессе метаболизма ксенобиотиков, где ведущую роль играют НАДФ*Н 2 -зависимые реакции, имеет место взаимодействие НАДФ*Н 2 и НФД*Н 2 -зависимых цепей. Установлена тесная функциональная связь цитохромов Р 450 и В 5 . Они могут образовывать сложные гемпротеидные комплексы, что обеспечивает высокую скорость катализируемых ими реакций превращения ксенобиотиков.
Среди схем биотрансформации ксенобиотиков под воздействием монооксигеназ наибольшее распространение получила схема Эстабрука, Гильденбрандта и Барона. Согласно этой схеме предполагается, что вещество –SH (в том числе – лекарство) на первой стадии взаимодействует с окисленной формой цитохрома Р 450 (Fe 3+) с образованием фермент-субстратного комплекса (SH-Fe 3+). На второй стадии фермент-субстратный комплекс восстанавливается электроном, поступающим от НАДФ*Н 2 посредством НАДФ*Н 2 -цитохромР 450 -редуктазы (ФП 1) при возможном участии цитохрома В 5 . Образуется восстановленный фермент-субстратный комплекс (SH-Fe 2+). Третья стадия характеризуется взаимодействием восстановленного фермент-субстратного комплекса с кислородом с образованием трехкомпонентного комплекса SH-Fe 2+ -О 2 . Присоединение кислорода осуществляется с большой скоростью. На четвертой стадии тройной фермент-субстрат-кислородный комплекс восстанавливается вторым электроном, который, по-видимому, поступает из НАД*Н 2 -специфической цепи переноса, включающей НАД*Н 2 -цитохром-В 5 -редуктазу (ФП 2) и, возможно, цитохром В 5 . Образуется восстановленный комплекс SH-Fe 2+ -О 2 1- .
Пятая стадия характеризуется внутримолекулярными превращениями восстановленного тройного фермент-субстрат-кислородного комплекса (SH-Fe 2+ -О 2 1- ↔ SH-Fe 3+ -О 2 2-) и его распадом с освобождением воды и гидроксилированного субстрата. При этом цитохром Р450 переходит в исходную окисленную форму.
При функционировании монооксигеназ генерируются активные радикалы, в первую очередь - супероксидный анион (О 2 -): тройной фермент-субстрат-кислородный комплекс до восстановления вторым электроном может вступать в обратимую реакцию превращения в окисленный фермент-субстратный комплекс и при этом генерируется супероксидный анион О 2 - .
Схему Эстабрука, Гильденбрандта и Барона можно представить следующим образом:
В отличие от митохондриальной дыхательной цепи, в которой молекулярный кислород, являющийся непосредственным акцептором электронов на последнем участке цепи, идет только на образование воды, в микросомальной монооксигеназной системе, наряду с образованием воды (на которое расходуется один атом кислорода), осуществляется при посредстве цитохрома Р 450 непосредственное присоединение кислорода (его второго атома) к окисляемому субстрату (лекарственному веществу) и происходит его гидроксилирование.
Кроме того, в отличие от митохондриальной цепи, где энергия, освобождающаяся в процессе переноса электронов, реализуется в виде АТФ на трех участках дыхательной цепи благодаря сопряжению окисления с фосфорилированием, в микросомальной цепи энергия окисления вообще не освобождается, а используется лишь редуцирующие эквиваленты НАДФ*Н 2 , необходимые для восстановления кислорода до воды. Поэтому окислительное гидроксилирование рассматривают, как свободное (т.е. не сопровождаемое образованием АТФ окисление).
Микросомальные монооксигеназные системы катализируют различные реакции окислительного превращения липотропных ксенобиотиков, в том числе лекарств. Наибольшее значение придается следующим окислительным реакциям превращения лекарственных веществ:
1) гидроксилированию ароматических соединений (например: салициловая кислота→ гентизиновая кислота → диокси- и триоксибензойная кислоты);
2) гидроксилированию алифатических соединений (например: мепробамат → кетомепробамат);
3) окислительному дезаминированию (например: фенамин → бензойная кислота);
4) S-дезалкилированию (например: 6-метилтиопурин → 6-тиопурин);
5) О-дезалкилированию (например: фенацетин → параацетамидофенол);
6) N-дезалкилированию (например: ипрониазид → изониазид);
7) сульфоокислению (например: тиобарбитал → барбитал);
8) N-окислению (например: диметиланилин → N-окись диметиланилина).
Помимо окислительных ферментных систем эндоплазматический ретикулюм печени содержит восстановительные ферменты. Эти ферменты катализируют восстановление ароматических нитро- и азосоединений в амиды. По химической природе восстановительные ферменты являются флавопротеидами, у которых простетической группой является ФАД. В качестве примера можно привести восстановление пронтозина в сульфаниламид.
Микросомальные ферменты печени (эстеразы) принимают участие также в реакциях гидролиза лекарственных веществ (сложных эфиров и амидов). Гидролиз – очень важный путь инактивации многих препаратов. В качестве примера может служить превращения ацетилсалициловой кислоты (сложный эфир) в салициловую кислоту и уксусную кислоту; ипрониазида (амид) в изоникотиновую кислоту и изопропилгидрозин, метаболизирующихся, в основном, путем гидролиза.
Фармакодинамика лекарственных средств. Основные принципы действия лекарственных веществ. Понятие о специфических рецепторах, агонистах и антагонистах. Фармакологические эффекты. Виды действия лекарственных средств.
Фармакодинамика
Фармакодинамика состоит из первичной и вторичной фармакологических реакций. Первичная фармакологическая реакция представляет собой взаимодействие биологически активных веществ, включая лекарственные вещества, с циторецепторами (или мы просто говорим с рецепторами). В результате такого взаимодействия развивается вторичная фармакологическая реакция в виде изменения метаболизма и функций органов и клеток. Нерецепторные механизмы действия лекарственных средств встречаются редко. Например, отсутствуют рецепторы для ингаляционных наркозных средств, плазмозаменителей, осмотических мочегонных средств.
Что же такое циторецепторы? Циторецепторы – это биомакромолекулы белковой природы созданы природой для эндогенных лигандов – гормонов, нейромедиаторов и так далее.
Лиганды – это вещества, способные связываться с циторецептором и вызывать специфический эффект. Они могут быть эндогенные, о чем говорилось выше (гормоны, нейромедиаторы), а также экзогенные, это ксенобиотики (например, лекарственные средства). Рецепторы имеют активные центры – это функциональные группы аминокислот, фосфатидов, сахаров и так далее. Лекарственные средства устанавливают с рецепторами физико-химические связи – вандерваальсовы, ионные, водородные – по принципу комплементарности, то есть активные группы лекарств взаимодействуют с соответствующими группами активного центра рецептора. Эти связи у большинства лекарств непрочные и обратимые. Но бывают прочные ковалентные связи лекарственного вещества и рецептора. Эта связь необратима. Например, тяжелые металлы, противоопухолевые средства. Такие лекарственные вещества высокотоксичны.
По отношению к рецепторам лекарственные вещества обладают: аффинитетом и внутренней активностью. Аффинитет (сродство) – это способность образовывать комплекс с рецептором. Внутренняя активность – это способность вызывать клеточный ответ.
В зависимости от выраженности аффинитета и наличия внутренней активности лекарственные вещества делят на 2 группы: агонисты и антагонисты. Агонисты (от греч. соперник) или миметики (от греч. подражать) – это вещества с умеренным аффинитетом и высокой внутренней активностью. Агонисты делятся на: полные агонисты, они вызывают максимальный ответ; частичные агонисты (парциальные). Они вызывают менее значительный ответ. Антагонисты или блокаторы – это вещества с высоким аффинитетом, но лишенные внутренней активности. Они препятствуют развитию клеточного ответа. Вещества, которые блокируют активные центры рецепторов, являются конкурентными антагонистами. Антагонисты, обладая высоким аффинитетом, более продолжительно связываются с циторецепторами. Некоторые вещества могут проявлять свойства агонистов-антагонистов, когда одни рецепторы возбуждаются, а другие – угнетаются.
Лекарственные средства могут присоединяться не к активному центру, а к аллостерическому центру рецептора. В этом случае они модифицируют структуру активного центра, и изменяет реакцию на лекарства или эндогенные лиганды. Например, аллостерическими рецепторами являются бензодиазепиновые рецепторы, когда лекарства бензодиазепинового ряда взаимодействуют с бензодиазепиновыми (аллостерическими) рецепторами, повышается аффинитет ГАМК-рецепторов к ГАМКислоте.
Циторецепторы классифицируют на 4 типа. 1 –рецепторы, непосредственно сопряженные с ферментами мембраны клеток. 2 – рецепторы ионных каналов мембраны клеток, они повышают проницаемость мембран для натрия, калия, кальция, хлора и обеспечивают мгновенный клеточный ответ. 3 – рецепторы, взаимодействующий с G-белками (мембранные белки). При возбуждении таких рецепторов образуются внутриклеточные биологически активные вещества – вторичные мессенджеры (от англ. «посредник», «вестник»), например цАМФ. 4 – рецепторы-регуляторы транскрипции. Эти рецепторы находятся внутри клетки (ядро, цитоплазма, то есть ядерные, цитозольные белки). Эти рецепторы взаимодействуют с гормонами (тиреоидные, стероидные), витамины А и Д. В результате такого взаимодействия изменяется синтез многих функционально активных белков.
Типовые механизмы действия лекарственных веществ. Их можно разделить на 2 группы: высокоизбирательные (рецепторные), неизбирательные (не связаны с рецептором). Различают 6 видов рецепторных механизмов действия лекарств.
1. Миметический эффект – это воспроизведение действия эндогенного (естественного) лиганда, то есть лекарственное вещество взаимодействует с рецептором и вызывает те же эффекты, что и эндогенный лиганд. Для проявления миметического действия надо, чтоб лекарственное вещество имело большое структурное сходство с лигандом (ключ-замок). Вещества, возбуждающие рецептор называются миметиками. Например, миметик карбахолин (лекарственный препарат) возбуждает рецептор – «холинорецептор». Эндогенный лиганд этого рецептора является ацетилхолин. Лекарственные средства, обладающими миметическим эффектом, называются «агонистами». Агонисты непосредственно возбуждают рецептор или повышают функцию рецептора:
2. Литический эффект или конкурентная блокада естественного лиганда. В этом случае лекарственное вещество лишь сходно с естественным лигандом. Этого достаточно, чтоб связаться с рецептором, но недостаточно, чтоб возбудить его. То, связавшись частично с рецептором, лекарственное вещество и сам не может возбудить рецептор и не дает возможности естественному лиганду соединиться с рецептором. Эффект лиганда отсутствует, наступает блокада рецептора. Лекарственные вещества, блокирующие рецепторы называются «блокаторами» или «литиками» (адренолитики, холинолитики).
рецептор лиганд блокатор
Если концентрация эндогенного лиганда повышается, то он может вытеснить (путем конкуренции) лекарственное вещество из связи с рецептором. Лекарственные средства, которые препятствуют действию «лиганд-агонистов» называются антагонистами. Они бывают конкурентными и неконкурентными.
3. Аллостерическое или неконкурентное взаимодействие. Кроме активного центра рецептор имеет еще аллостерический центр, который регулирует скорость ферментативных реакций. Лекарственное средство, связываясь с аллостерическим центром либо «открывает» активный центр, либо «закрывает» его. В первом случае рецептор «активируется», во втором – «блокируется.
4. Активация либо ингибирование ферментов (внутриклеточное или внеклеточное). В этих случаях рецептором для лекарственных веществ выступают ферменты. Например, лекарства: фенобарбитал, зиксорин – активируют микросомальные ферменты. Ниламид ингибирует фермент МАО.
5. Изменение функций транспортных систем и проницаемости мембран клеток и органелл. Например, верапамил, нифедипин блокируют медленные кальцевые каналы. Антиаритмические средства, местные анестетики изменяют проницаемость мембран для ионов.
6. Нарушение функциональной структуры макромолекулы. Например, противосудорожные, противоопухолевые средства.
К неизбирательным типовым механизмам действия лекарств относят. 1. Прямое физико-химическое взаимодействие лекарственных веществ. Например, натрия гидрокарбонат нейтрализует соляную кислоту желудка при повышенной кислотности, активированный уголь адсорбирует токсины. 2. Связь лекарственных средств с низкомолекулярными компонентами организма (ионы, микроэлементы). Например, трилон Б связывает ионы кальция в организме.
Виды действия лекарственных средств.
1. Резорбтивное действие (резорбция – всасывание) – это действие лекарственных средств, которое развивается после всасывания их в кровь. Это действие еще называют «общее действие». Например, нитроглицерин под язык. Инъекционные формы препаратов.
2. Местное действие – это действие лекарственных средств на месте его приложения (кожа, слизистые). Например, мази, пасты, присыпки, полоскания с использованием препаратов, оказывающих противовоспалительное, вяжущее, прижигающее действие.
Рефлекторное действие – это, когда лекарственный препарат действует на нервные окончания, что приводит к появлению ряда рефлексов со стороны органов и систем. Может одновременно развиваться и рефлекторное и местное и резорбтивное действия. Примеры рефлекторного действия. Валидол (под язык) рефлекторно расширяет сосуды сердца, в результате чего исчезают боли в сердце. Горчичники оказывают и местное (покраснение кожи) и рефлекторное действие. Действие горчичников на кожу сопровождается местным действием (покраснение кожи) и рефлекторным, связанным с раздражением чувствительных нервных окончаний горчичным эфирным маслом. При этом развивается 2 рефлекса.
Первый – аксон-рефлекс замыкается на уровне спинного мозга. При этом расширяются сосуды того органа, который топографически связан с рефлексогенными зонами Захарьина-Геда, на которые положили горчичник. Это расширение сосудов больного органа называется трофическим действием горчичников.
Второй рефлекс замыкается на уровне коры головного мозга. Больной чувствует боль жжение в месте нанесения горчичников, а ощущения формируются в коре головного мозга. Итак, в коре головного мозга возникают 2 очага возбуждения: один связан с горчичником, второй – связан с больным органом. Если доминирует очаг возбуждения с рецепторов кожи, то реализуется «отвлекающее» действие, то есть снимается боль с внутренних органов (стенокардия, кашель при бронхитах).
4. Центральное действие – это действие лекарственных средств на центральную нервную систему. Например, снотворные, успокаивающие, наркозные средства.
5. Избирательное действие – это преимущественное действие лекарственных средств на определенные органы и системы или на определенные рецепторы. Например, сердечные гликозиды.
6. Неизбирательное (протоплазматическое) действие лекарственных веществ, когда препарат действует однонапрвленно на большинство органов и тканей организма. Например, антисептическое действие солей тяжелых металлов обусловлено блокадой SH-групп тиоловых ферментов любых тканей организма. Этим объясняется и терапевтическое и токсическое действие лекарств. Хинин, например, оказывает мемраностабилизирующее действие в сердце, гладких мышцах, центральной нервной системе, периферической нервной системе. Поэтому хинин многообразен как лекарственный препарат и у него многообразны побочные эффекты.
7. Прямое действие – непосредственное действие лекарственного средства на определенный орган или процесс. Например, сердечные гликозиды прямо действуют на сердце (увеличивают силу сердечных сокращений).
8. Косвенное действие лекарственных средств. Под косвенным действием подразумевают вторичные изменения функций органа в результате прямого влияния препарата на другой орган или систему. Например, сердечные гликозиды за счет прямого действия на сердце увеличивает силу сердечных сокращений, что вызывает улучшение общей гемодинамики, в том числе и почек. В результате – косвенно увеличивается диурез. Таким образом, мочегонное действие сердечных гликозидов – это косвенное действие.
9. Главное действие препарата – это то действие, которое лежит в основе его лечебного или профилактического применения: дифенин – противосудорожное действие, новокаин – обезболивающее (местное действие), фуросемид – мочегонное.
10. Побочное действие – это способность лекарственного средства вызывать помимо главного действия, другие виды действия на органы и системы нежелательные и даже приносящие вред. Например, при спазме кишечника хорошо помогает атропин – он «снимает» спазм, но одновременно вызывает сухость во рту (это – побочный эффект).
Стоматологам! При длительном применении противосудорожного средства дифенина (при эпилепсии) может возникнуть гиперпластический гингивит (воспаление слизистой десны). Однако это побочное действие дифенина иногда используют стоматологи для ускорения регенерации слизистой оболочки полости рта.
11. Токсическое действие – это резкие сдвиги функций органов и систем, выходящие за пределы физиологических при назначении чрезмерно больших доз препаратов или в результате повышенной чувствительности больного к этому препарату. Токсическое действие препаратов может проявляться по-разному6 аллергической реакцией, угнетение сердечно-сосудистой деятельности, угнетение дыхания, угнетение кроветворения и так далее.
Можно выделить еще обратимое действие лекарственных веществ, необратимое действие лекарственных средств. Пример обратимого действия – это прозерин, который обратимо ингибирует холинэстеразу (связь с этим ферментом непрочная и недлительная). Пример необратимого действия – действие прижигающих средств (коагуляция белков)Реакции, обусловленные длительным приемом и отменой лекарственных средств: кумуляция, сенсибилизация, привыкание, тахифилаксия, синдром «отдачи», синдром «отмены», лекарственная зависимость.
1. Кумуляция – это накопление лекарственного вещества или его эффектов в организме. Кумуляция бывает двух видов. Во-первых – это материальная (физическая), когда в организме накапливается само лекарственное вещество. Причины: медленная инактивация препарата, стойкое связывание с белками крови, патология печени, почек, повторная реабсорбция и так далее. Для предотвращения материальной кумуляции надо: уменьшить дозу вещества, увеличить интервалы между приемами! Во-вторых – это функциональная кумуляция , когда накапливается эффект лекарственного средства. Такую кумуляцию можно наблюдать при приеме алкоголя. Сам этиловый спирт быстро окисляется в организме и не накапливается. Но при частом применении его эффект усиливается (накапливается) и проявляется в виде психоза («белая горячка»).
2. Сенсибилизация – это усиление действия лекарственных веществ при их повторном введении даже в малых дозах. Это реакция иммунной природы и она может возникнуть к любым лекарственным средствам (анафилактический шок).
3. Привыкание (толерантность) – это снижение эффекта при повторном введении лекарственного средства в той же дозе. Например, при постоянном приеме снотворных средств или капель от насморка они перестают действовать, то есть наступает привыкание. При постоянном приеме морфина также наступает привыкание, что вынуждает «морфинистов» увеличивать дозу морфина до 10 – 14 грамм в сутки.
Причины привыкания. Снижение чувствительности рецепторов к некоторым препаратам. Например, снижается чувствительность к некоторым противоопухолевым средствам, что вынуждает менять препарат. Снижение возбудимости чувствительных нервных окончаний (слабительные). Ускоренная инактивация препарата в силу индукции микросомальных ферментов печени (фенобарбитал). Включение механизмов компенсации, которые снижают вызванный препаратом сдвиг. Например, даем препарат, снижающий артериальное давление, в организме наступает задержка жидкости и компенсаторно повышается артериальное давление. Аутоингибирование, то есть за счет избытка лекарственного вещества происходит связывание с рецептором нескольких молекул лекарственного вещества. Наступает «перегрузка» рецептора. В результате, эффект препарата снижается.
Эффект «привыкания» можно устранить: если делать перерывы в лечении, чередовать препараты, комбинировать с другими лекарственными средствами.
4. Тахифилаксия – это острая форма привыкания, которая развивается после повторного введения препарата в пределах от нескольких минут до одних суток. Например, вводим эфедрин и наблюдаем значительное повышение артериального давления, а при повторном введении через несколько минут эффект слабый, а еще через несколько минут эффект еще слабее. Тахифилаксия наступает к эфедрину, адреналину, норадреналину. Тахифилаксия объясняется тем, что при повторном введении препарат не может полностью связаться с рецептором, так как он еще занят первой порцией препарата.
5. Синдром (феномен) отдачи наступает после внезапного прекращения введения препарата. При этом наступает суперкомпенсация процесса с резким обострением болезни по сравнению с долечебным периодом. Растормаживание регуляторных процессов. Например, после внезапной отмены клофелина у больного с гипертонической болезнью, может наступить гипертонический криз (резкий подъем артериального давления). Наступил взрыв регуляторных реакций. Чтобы избежать феномена «отдачи» надо постепенно уменьшать дозу препарата (не отменять внезапно).
6. Синдром (феномен) «отмены» наступает после внезапного прекращения введения препарата. В отличие от синдрома «отдачи», в данном случае наступает подавление физиологической функции. Например, при назначении больному гормональных препаратов глюкокортикоидов подавляется выработка собственных гормонов (по принципу обратной связи). Надпочечники как бы атрофируются. И резкая отмена препарата сопровождается острой гормональной недостаточностью.
7. Лекарственная «зависимость» развивается при повторном приеме психотропных лекарственных средств. Лекарственная зависимость бывает психическая и физическая. По определению экспертов ВОЗ психическая зависимость – это состояние, при котором лекарственное средство вызывает чувство удовлетворения и психического подъема. Это состояние требует периодического и постоянного введения лекарственного средства, чтобы испытать удовольствие и избежать дискомфорта. Другими словами, психическая зависимость – это «пристрастие» или болезненное влечение. Психическая зависимость обусловлена способностью наркотиков повышать освобождение дофамина в полосатом теле, гипоталамусе, лимбической системе, коре больших полушарий. по мере развития пристрастия лекарство изменяет обмен веществ в клетках мозга и становится необходимым регулятором функции многих нейронов. Внезапное лишение тонизирующего средства вызывает синдром «абстиненции» (синдром 2отнятия», «лишения»). Этот синдром проявляется рядом физических расстройств и наступает «физическая зависимость». Физические расстройства могут быть очень серьезными: нарушение сердечно-сосудистой системы, возбуждение, бессонница, судороги или угнетение, депрессия, попытки к самоубийству. Чтобы прервать синдром абстиненции человек должен ввести наркотик и готов идти на «все», чтобы его достать. Вещества, вызывающие лекарственную зависимость: алкоголь и подобные вещества, барбитураты, препараты опия, кокаин, фенамин, вещества типа каннабиса (гашиш, марихуана), галлюциногены (ZSD, мескалин), эфирные растворители (толуол, ацетон,CCL 4).
Факторы, влияющие на фармакокинетику и фармакодинамику лекарственных веществ. Химическая структура и физико-химические свойства лекарственных веществ. Значение стереоизомерии, липофильности, полярности, степени диссоциации.