أ. أ. الخلايا الليمفاوية، ب. وحيدات، ج. العدلات
ب. أ. العدلات، ب. وحيدات، ج. الخلايا الليمفاوية
خامسا أ. وحيدات، ب. العدلات، ج. الخلايا الليمفاوية
- تحديد الخلايا التي تضمن القضاء على عيوب الأنسجة في موقع الالتهاب:
أ. الخلايا اللمفاوية التائية
ب. الخلايا الليمفاوية
ب. الخلايا الليفية
ز. حيدات
د- المنسجات
E. الخلايا المتنيّة
- أسباب تطور الالتهاب العقيم يمكن أن تكون:
أ. تجلط الأوعية الوريدية
ب. نخر الأنسجة
ب- نزف في الأنسجة
د. التدخل الجراحي الذي يتم إجراؤه في ظل ظروف معقمة تمامًا
د. الإدارة الوريدية للبروتين الأجنبي المعقم
E. فرط التأكسج في الأنسجة العابرة
G. الإدارة المعوية للبروتين الأجنبي غير المعقم
- تم الكشف عن التصاق (التصاق) الكريات البيض ببطانة الأوعية الدموية الدقيقة في المقام الأول:
أ. في الشرايين
ب. في الميتاريولات
ب. في الشعيرات الدموية
د. في الأوردة postcapillary
- يرتبط حدوث "الانفجار التنفسي" في الكريات البيض بما يلي:
أ. من تفعيل أوكسيديز NADPH
ب. مع تفعيل مسار أحادي الفوسفات السداسي لأكسدة الجلوكوز
ب. مع تكوين مستقلبات الأكسجين النشطة
د. مع تفعيل تحلل السكر اللاهوائي
- حدد المواد التي لها خصائص الجاذبات الكيميائية للعدلات:
أ. عديدات السكاريد الدهنية للبكتيريا
ب. الليكوترين B4
خامسا انترلوكين-8
د. المكون C5a من نظام المجاملة
هاء-إنترلوكين-2
جي انترلوكين -1
Z. الليزوزيم
- أشر إلى الخصائص التي يمتلكها البراديكينين:
أ- يسبب هبوطاً في ضغط الدم
ب- يقبض العضلات الملساء للأعضاء المجوفة
ب. يزيد من نفاذية الأوعية الدموية الدقيقة
د- يهيج نهايات أعصاب الألم
د- يعتبر جاذباً كيميائياً للكريات البيضاء
- أي من الخلايا التالية تصنف على أنها "خلايا التهابية مزمنة"؟
أ. البلاعم
ب. الخلايا الليمفاوية
ب. الخلايا الظهارية
د- الخلايا البدينة
د- العدلات
E. الحمضات
- ما هي التغيرات الفيزيائية والكيميائية التي لوحظت في بؤرة الالتهاب العقيم الحاد؟
أ. الحماض
ب. القلاء
ب. فرط حاسة الشم
ز. فرط الحركة
د. نقص التعرق
E. نقص حاسة الشم
جي ديزونيا
- يعتبر الالتهاب بمثابة رد فعل وقائي وتكيفي للجسم لأنه:
أ. يحد من موقع الضرر، ويمنع انتشار العامل الفلوغوني ومنتجات التغيير في الجسم
ب. يثبط نشاط العامل الفلوجيني ومنتجات تغيير الأنسجة
ب. يمنع حساسية الجسم
D. يحشد عوامل دفاع الجسم المحددة وغير المحددة
د. يعزز ترميم أو استبدال هياكل الأنسجة التالفة
- حدد أسباب فرط أيونات الكالسيوم في الإفرازات الالتهابية
أ. الحماض خارج الخلية
ب. زيادة التحلل البروتيني
ب. نقص الطاقة
د- التحلل الخلوي المكثف
د- العمليات التكاثرية
E. زيادة نفاذية جدار الشعيرات الدموية
- حدد العوامل الداخلية التي يؤدي فائضها إلى فك الأكسدة والتفسفر في خلايا التركيز الالتهابي:
أ. أيونات الكالسيوم
أيونات B.K+
ب. الأحماض الدهنية غير المشبعة
ز. الجلايكورتيكويدات
أيونات D.H+
هاء الدينتروفينول
- العوامل التي تساهم في تطور احتقان الدم الشرياني في موقع الالتهاب هي:
أ. كولاجيناز
ب- الهيستامين
ب. النورإبينفرين
جي براديكينين
د- انخفاض نشاط المستقبلات الوعائية
E. زيادة نشاط الهيالورونيداز
- أي من هذه العوامل تعتبر وسيطة للالتهاب من أصل خلوي؟
أ. براديكينين
ب. مكونات النظام المكمل
ب. الإنزيمات
ز. البروستاجلاندين
د. الليكوترين
هاء-إنترلوكين-1
ز. الإنترفيرون
- يتميز الالتهاب الحاد بما يلي:
ب. زيادة نفاذية جدران الأوعية الدموية الدقيقة
D. تسلل تركيز الالتهاب مع الكريات البيض وحيدة النواة
هـ- وذمة في مكان الالتهاب
- عواقب تفعيل النظام التكميلي هي:
أ. تحفيز إطلاق الهستامين بواسطة الخلايا البدينة
ب. تحلل الخلايا المهاجمة
ب. تفعيل الكريات البيض متعددة الأشكال
د- إثارة نهايات أعصاب الألم
- عند الهجرة إلى مكان الالتهاب:
أ. تخترق الخلايا المحببة جدار الأوعية الدموية بشكل سلبي مع تدفق السوائل
ب. تمر الخلايا المحببة بشكل فعال عبر الشقوق البينية والغشاء القاعدي لجدار الأوعية الدموية
ب. تمر الخلايا المحببة عبر جدار الأوعية الدموية عبر الخلايا
د. تمر الخلايا المحببة عبر جدار الأوعية الدموية عن طريق كثرة الخلايا
- يتضمن نظام كاليكريين كينين ما يلي:
أ. عامل هاجمان
ب. البريكاليكرين
ب. النظام المكمل
جي براديكينين
- أي من الشروط التالية تعتبر إلزامية لالتصاق كريات الدم البيضاء ببطانة الأوعية الدموية الدقيقة أثناء الالتهاب؟
أ- تباطؤ تدفق الدم
ب. تكون جلطات الدم في الأوعية الدموية
د. ظهور المحددات على الغشاء
- تحديد التسلسل الصحيح للتغيرات في ديناميكا الدم في موقع الالتهاب
1. احتقان الدم الشرياني (النشط).
2. تشنج الأوعية الدموية ونقص تدفق الدم
3. تدفق الدم متشنج
4. احتقان الدم الوريدي (السلبي).
5. ستاز
خامسا 2،1،4،3،6،5
- ما هي العلامات التي قد تشير إلى وجود عملية التهابية حادة؟
أ. كثرة الكريات البيضاء
ب- الحمى
ب. زيادة في ESR
د- زيادة محتوى الجلوبيولين جاما في مصل الدم
د- تراكم بروتين سي التفاعلي في الدم
هاء - تجلط الدم
ز. كثرة الكريات الحمر
ح. نقص بروتينات الدم
- الاختلافات الرئيسية بين الإفرازات القيحية والإفرازات القيحية أثناء الالتهاب هي أن الأخير يحتوي على:
أ- وجود عدد كبير من خلايا الدم (الكريات البيض، وما إلى ذلك)
ب. وجود عدد كبير من عناصر الأنسجة المدمرة والتالفة
ب. كمية قليلة من البروتينات (<3-5%)
د. كمية كبيرة من البروتين (>3-5%)
- يبدأ تفعيل نظام كاليكريين كينين بتفعيل:
أ. كينينوجين ذو وزن جزيئي مرتفع
ب. عامل هاجمان
V. بريكاليكرينا
جي براديكينينا
- تتميز الاستجابة الالتهابية الحادة بما يلي:
أ. تشكيل الأورام الحبيبية الالتهابية
ب. زيادة نفاذية الأوعية الدموية الدقيقة
ب. تراكم الخلايا العملاقة متعددة النوى في مكان الالتهاب
د- تراكم العدلات في مكان الالتهاب
- أي من الخصائص التالية تمتلكها المكونات النشطة في النظام المكمل؟
أ. إنها تتحلل الخلايا الأجنبية
ب. بمثابة جاذبات كيميائية للعدلات وحيدات
ب. بمثابة الأوبسونين
د- يسبب تحلل الخلايا البدينة
- أي من المواد التالية تعتبر "وسطاء" للالتهاب؟
أ. كينينز
ب. البروستاجلاندين EI، E2
ب. الأمينات الحيوية
أيونات D.K+
أيونات D.H+
هاء - الليمفوكينات
جيه ليوكوترين
ح. الأحماض النووية
- وسطاء الالتهابات الذين يسببون زيادة في نفاذية الأوعية الدموية أثناء الالتهاب هم:
أ. الهيبارين
ب- الهيستامين
في. براديكينين
ز. الإنترفيرون
د. السيروتونين
E. الليكوترين
- أي من العوامل المذكورة لها تأثير محفز على عملية التكاثر في موقع الالتهاب؟
أ. كيلونز
ب. مثبطات الكيلون
G. cGMP
د- الجلايكورتيكويدات
هاء-إنترلوكين-2
- ما هي العوامل التي تساهم في تطور الوذمة في موقع الالتهاب:
أ- زيادة ضغط الدم الجرمي
ب. زيادة الضغط الجرمي لسائل الأنسجة
ب. انخفاض الضغط الجرمي لسائل الأنسجة
د. زيادة نفاذية جدار الأوعية الدموية
د. انخفاض الضغط الاسموزي لسائل الأنسجة
هـ- زيادة الضغط في القسم الوريدي من الشعيرات الدموية
ز. زيادة الضغط الأسموزي لسائل الأنسجة
- تشمل العوامل التي تعزز التصاق (التصاق) العدلات ببطانة الأوعية الدموية الدقيقة أثناء الالتهاب ما يلي:
أ. عامل نخر الورم (TNF)
ب- الإنترلوكين 1
B. جزء C5a من النظام التكميلي
G. عديدات السكاريد الدهنية للبكتيريا
د- عامل تنشيط الصفائح الدموية
E. الليكوترين
- تحديد العوامل المسببة للألم أثناء الالتهاب:
أ. المجموعة E البروستاجلاندين
ب- الهيستامين
ب. الحماض
ز. أيونات فرط البوتاسيوم
د. كينينا
هـ- ارتفاع درجة حرارة الأنسجة
ز- التهيج الميكانيكي للنهايات العصبية
- حدد المواد التي لها خصائص الجاذبات الكيميائية للعدلات
أ. إنترلوكين -2
ب. عديدات السكاريد الدهنية للبكتيريا
ب. الليكوترين B4
ج. انترلوكين-8
D. جزء من النظام التكميلي C5a
هـ- عامل تنشيط الصفائح الدموية
- اختر الاجابة الصحيحة:
أ- التغيير هو تغيير في بنية خلايا الأنسجة والأعضاء
ب. التغيير هو تغيير في عملية التمثيل الغذائي وبنية ووظيفة الخلايا مما يؤدي إلى تعطيل عمليات الحياة الطبيعية
- تطلق العدلات المشاركة في الاستجابة الالتهابية مواد تسبب العمليات التالية:
أ. انجذاب كيميائي للخلايا الوحيدة
ب. تحلل الخلايا البدينة
ب. زيادة نفاذية الأوعية الدموية
د- تدمير خلايا الأنسجة
الضغط الميكانيكي للمستقبلات
زيادة استثارة المستقبلات
عمل المواد النشطة بيولوجيا
تدمير المستقبلات
حمى
93. أشر إلى الإجابة الصحيحة
الرابط الرئيسي في التسبب في تفاعلات حساسية الريجين وفقًا لـ P. GELL وR. COMBES
94. أشر إلى الإجابة الصحيحة
الرابط الرئيسي في التسبب في تفاعلات الحساسية المضادة للمستقبلات
() تكوين الأجسام المضادة لمستقبلات الخلية
() تكوين الأجسام المضادة للخلايا (IgE)
() تكوين الأجسام المضادة للمستضدات على الخلايا
() تكوين الخلايا اللمفاوية التائية الحساسة
() تشكيل الأجسام المضادة المترسبة
95. أشر إلى عدة إجابات صحيحة
مميزات التحسس النشط
يظهر بعد 7-10 أيام من ملامسة المستضد
يظهر بعد ساعات قليلة من تناول المصل
96. أشر إلى عدة إجابات صحيحة
مميزات التحسس السلبي
تعتمد شدتها على تكرار الاتصال بالمستضد
يتطور بعد إعطاء الأجسام المضادة عالية العيار
تعتمد شدتها على كمية الأجسام المضادة المحقونة
يستمر أشهر، سنوات
يتطور عند التعرض لجرعات صغيرة من المستضد
يستمر 2-3 أسابيع
97. أشر إلى عدة إجابات صحيحة
البيروجينات الذاتية
عامل نخر الورم
السموم الداخلية البكتيرية
المستقلبات البكتيرية
انترلوكين-1
السموم البكتيرية
انترلوكين-6
98. أشر إلى عدة إجابات صحيحة
وسطاء التفاعلات التحسسية السامة للخلايا
إطراء
الانزيمات الليزوزومية
الهستامين
أنيون فوق أكسيد
مشتقات حمض الأراكيدونيك
99. أشر إلى الإجابة الصحيحة
آلية زيادة درجة حرارة الجسم أثناء الحمى
() انخفاض في إنتاج الحرارة
() الحد من انتقال الحرارة
() زيادة في إنتاج الحرارة
() زيادة في انتقال الحرارة
100. أشر إلى الإجابة الصحيحة
آلية خفض درجة حرارة الجسم أثناء الحمى
() تقليل انتقال الحرارة
() زيادة في انتقال الحرارة
() زيادة في إنتاج الحرارة
() التوازن بين توليد الحرارة ونقل الحرارة
() زيادة في انتقال الحرارة
101. أشر إلى عدة إجابات صحيحة
مراحل التأثير المباشر للخلايا اللمفاوية التائية في تفاعلات الحساسية المتأخرة
الكيميائية المرضية
منيع
نقص التحسس
ضربة قاتلة
تعرُّف
تحلل الخلايا المستهدفة
التحسس
102. أشر إلى عدة إجابات صحيحة
آليات تلف الخلايا أثناء التفاعلات السامة للخلايا
عمل الليكوترين
تكملة التنشيط
إطلاق السموم اللمفاوية عن طريق الخلايا الليمفاوية التائية الحساسة
عمل الليبوكسينات
عمل الهستامين
Opsonization بواسطة الغلوبولين المناعي
103. أشر إلى عدة إجابات صحيحة
مسببات الحساسية الداخلية الأولية
أنسجة عصبية
قشرة الغدة الكظرية
المبايض
النخاع الكظرية
كبيبات الكلى
104. أشر إلى عدة إجابات صحيحة
الأشكال السريرية لتفاعلات حساسية ريجين
داء المصل
الربو القصبي
قشعريرة
فقر الدم الانحلالي
نقص في عدد كريات الدم البيضاء
التهاب الجلد التماسي
105. أشر إلى عدة إجابات صحيحة
العوامل اليوزينية التي تعمل على تعطيل BAS
الهيستاميناز
البروتين الأساسي
أريل سلفاتاز
محلقة الأدينيلات
فسفوليباز أ
فسفوليباز د
فسفوديستراز
106. أشر إلى عدة إجابات صحيحة
مكونات الحماية الأنزيمية للخلايا من الجذور الحرة
البروتين الأساسي
فسفوليباز د
ديسموتاز فوق أكسيد
الجلوتاثيون بيروكسيديز
فسفوليباز أ
فسفوديستراز
الكاتلاز
107. أشر إلى عدة إجابات صحيحة
التصاق جزيئات العدلات بجدار الأوعية الدموية
انترلوكين-1
الغلوبولين المناعي G (IgG)
الغلوبولين المناعي أ (IgA)
الغلوبولين المناعي M (IgM)
تحديد
إطراء
التكاملات
108. أشر إلى عدة إجابات صحيحة
آليات زيادة درجة حرارة الجسم أثناء الحمى
توسع الأوعية المحيطية
تعزيز عمليات الأكسدة
انقباض الأوعية الدموية الطرفية
انخفاض التعرق
زيادة التعرق
زيادة اقتران الأكسدة والفسفرة
109. أشر إلى عدة إجابات صحيحة
أسباب الحالة الإقفارية
الانسداد الوريدي
تشنج الشرايين
انسداد الشرايين
ضغط الوريد
ضغط الشرايين
تخثر الوريد
110. أشر إلى عدة إجابات صحيحة
عواقب احتقان الدم الشرياني
تكاثر الأنسجة الضامة
تطور نقص الأكسجة وفرط ثنائي أكسيد الكربون في الدم
تمزق جدار الوعاء الدموي
تحسين إمدادات الدم إلى العضو
ضمور الحمة في الأعضاء
111. أشر إلى عدة إجابات صحيحة
ويشارك عدد كبير من الآليات الفيزيولوجية العصبية والكيميائية العصبية المختلفة في التسبب في متلازمات الألم الناشئة عن الالتهاب، والتي تؤدي حتما إلى تغيرات في الحالة النفسية الفسيولوجية للمريض. يؤدي الضرر الخارجي أو الداخلي إلى سلسلة من العمليات الفيزيولوجية المرضية التي تؤثر على الجهاز المسبب للألم بأكمله (من مستقبلات الأنسجة إلى الخلايا العصبية القشرية)، بالإضافة إلى عدد من الأنظمة التنظيمية الأخرى في الجسم. يؤدي الضرر الخارجي أو الداخلي إلى إطلاق مواد فعالة وعائيًا مما يؤدي إلى تطور الالتهاب. لا تسبب هذه المواد النشطة في الأوعية الدموية أو ما يسمى بالوسطاء الالتهابيين مظاهر نموذجية للالتهاب فحسب، بما في ذلك تفاعل الألم الواضح، ولكنها تزيد أيضًا من حساسية مستقبلات الألم للتهيجات اللاحقة.
هناك عدة أنواع من وسطاء الالتهابات التي تزيد من حساسية مستقبلات الألم للتهيج.
. وسطاء البلازما للالتهابات 1. نظام كاليكريين كينين: براديكينين، كاليدين 2. المكونات المتممة: C2-C4، C3a، C5 - سموم الحساسية المفرطة، C3b - أوبسونين، C5-C9 - مجمع الهجوم الغشائي 3. نظام الإرقاء وانحلال الفيبرين: عامل التخثر الثاني عشر (عامل هاجمان) ، الثرومبين، الفيبرينوجين، الفيبرينوببتيدات، البلازمين، الخ.
وسطاء الالتهاب الخلوية 1. الأمينات الحيوية: الهستامين، السيروتونين، الكاتيكولامينات. 2. مشتقات حمض الأراكيدونيك:
- البروستاجلاندين (PGE1، PGE2، PGF2α، الثرومبوكسان A2، البروستاسيكلين I2)، الليوكوترين (LTV4، MRS (A) - مادة بطيئة التفاعل في الحساسية المفرطة)، الدهون الكيميائية 3. عوامل المحببة: البروتينات الكاتيونية، البروتياز المحايدة والحمضية، الإنزيمات الليزوزومية 4. عوامل الانجذاب الكيميائي: عامل الانجذاب الكيميائي للعدلات، عامل الانجذاب الكيميائي اليوزيني، إلخ. 5. جذور الأكسجين: O 2 -أكسيد فائق، H 2 O 2، NO، مجموعة OH-hydroxyl 6. الجزيئات اللاصقة: Selectins، integrins 7. السيتوكينات: IL- 1، IL-6، عامل نخر الورم، الكيموكينات، الإنترفيرون، عامل تحفيز المستعمرة، إلخ. 8. النيوكليوتيدات والنيوكليوسيدات: ATP، ADP، الأدينوزين 9. الناقلات العصبية والببتيدات العصبية: المادة P، الببتيد المرتبط بجين الكالسيتونين، النيوروكينين A، الغلوتامات، الأسبارتات، النورإبينفرين، الأسيتيل كولين.
حاليًا، تم تحديد أكثر من 30 مركبًا كيميائيًا عصبيًا تشارك في آليات إثارة وتثبيط الخلايا العصبية المسببة للألم في الجهاز العصبي المركزي. من بين مجموعة كبيرة من الناقلات العصبية والهرمونات العصبية والمعدلات العصبية التي تتوسط في توصيل الإشارات المسببة للألم، هناك جزيئات بسيطة - أحماض أمينية مثيرة - BAK (الغلوتامات، الأسبارتات)، ومركبات جزيئية عالية معقدة (المادة P، النيوروكينين A، جين الكالسيتونين الببتيد المرتبط ، وما إلى ذلك). تلعب VACs دورًا مهمًا في آليات الإحساس بالألم. عند تنشيط المستقبلات الأيونية: مستقبلات NMDA , تتسبب مستقبلات AMPA ومستقبلات الغلوتامات المعدنية في دخول أيونات Ca 2+ بشكل مكثف إلى الخلية وتغيير في نشاطها الوظيفي. يتم تشكيل فرط استثارة الخلايا العصبية المستمر ويحدث فرط التألم.
في الآونة الأخيرة، تم إيلاء أهمية كبيرة لآليات توعية الخلايا العصبية المسببة للألم. أكسيد النيتريك(NO)، والذي يعمل في الدماغ كجهاز إرسال غير نمطي خارج المشبكي. يلعب أكسيد النيتريك دورًا رئيسيًا في العمليات الالتهابية. يؤدي الحقن الموضعي لمثبطات NO سينسيز في المفصل إلى منع انتقال مسببات الألم والالتهاب بشكل فعال.
كينينزهي واحدة من أقوى المعدلات الطحالب. التأثير الاستثاري المباشر للبراديكينين على النهايات العصبية الحسية يتم بوساطة مستقبلات B2 ويرتبط بتنشيط غشاء فسفوليباز C. التأثير الاستثاري غير المباشر للبراديكينين على نهايات العصب الوارد يرجع إلى تأثيره على عناصر الأنسجة المختلفة (الخلايا البطانية، الخلايا الليفية والخلايا البدينة والبلاعم والعدلات) وتحفيز تكوين وسطاء التهابات فيها، والتي تتفاعل مع المستقبلات المقابلة على النهايات العصبية، وتنشط غشاء أدينيلات سيكلاز. بدوره، يحفز إنزيم محلقة الأدينيلات والفوسفوليباز C تكوين الإنزيمات التي تفسفر بروتينات القناة الأيونية. نتيجة فسفرة بروتينات القناة الأيونية هي تغيير في نفاذية الغشاء للأيونات، مما يؤثر على استثارة النهايات العصبية والقدرة على توليد نبضات عصبية.
تجمع كلمة الألم بين مفهومين متناقضين. من ناحية، وفقًا للتعبير الشائع للأطباء الرومان القدماء: "الألم هو حارس الصحة"، ومن ناحية أخرى، فإن الألم، إلى جانب وظيفة الإشارة المفيدة التي تحذر الجسم من الخطر، يسبب عددًا من المشاكل المرضية. الآثار، مثل التجربة المؤلمة، ومحدودية الحركة، وضعف دوران الأوعية الدقيقة، وانخفاض الدفاع المناعي، وعدم تنظيم وظائف الأعضاء والجهاز. يمكن أن يؤدي الألم إلى أمراض خلل التنظيم الشديدة ويمكن أن يسبب الصدمة والموت [كوكوشكين إم إل، ريشتنياك في كيه، 2002].
الألم هو العرض الأكثر شيوعا للعديد من الأمراض. ويعتقد خبراء منظمة الصحة العالمية أن 90% من جميع الأمراض ترتبط بالألم. المرضى الذين يعانون من الألم المزمن هم أكثر عرضة لطلب المساعدة الطبية بخمس مرات مقارنة بغيرهم من السكان. ليس من قبيل الصدفة أن القسم الأول من الدليل الأساسي للطب الباطني المكون من 10 مجلدات، والذي نُشر تحت رئاسة تحرير تي آر هاريسون (1993)، مخصص لوصف الجوانب الفيزيولوجية المرضية للألم. الألم دائمًا أمر شخصي، ويعتمد إدراكه على شدة الضرر وطبيعته وموضعه، وعلى طبيعة العامل المدمر، وعلى الظروف التي حدث فيها الضرر، وعلى الحالة النفسية للشخص، وتجربته الحياتية الفردية و الحالة الاجتماعية.
ينقسم الألم عادة إلى خمسة مكونات:
- مكون إدراكي يسمح للشخص بتحديد موقع الضرر.
- مكون عاطفي عاطفي يشكل تجربة نفسية وعاطفية غير سارة.
- مكون لاإرادي يعكس التغيرات المنعكسة في عمل الأعضاء الداخلية ونغمة الجهاز الكظري الودي.
- مكون حركي يهدف إلى القضاء على آثار المنبهات الضارة.
- المكون المعرفي الذي يشكل موقفًا شخصيًا تجاه الألم الذي يحدث في لحظة معينة بناءً على الخبرة المتراكمة [والدمان أ.ف.، إيجناتوف يو.د.، 1976].
رئيسي العوامل المؤثرة على إدراك الألم، نكون:
- عمر.
- دستور.
- تربية.
- خبرة سابقة.
- مزاج.
- توقع الألم.
- يخاف.
- روسا.
- جنسية [ميلزاك ر.، 1991].
بادئ ذي بدء، يعتمد إدراك الألم على جنس الفرد. عند تعرض النساء لمحفزات مؤلمة متساوية الشدة، يكون المؤشر الموضوعي للألم (توسع الحدقة) أكثر وضوحًا. باستخدام التصوير المقطعي بالإصدار البوزيتروني، وجد أن النساء يعانين من تنشيط أكثر وضوحًا لهياكل الدماغ أثناء التحفيز المؤلم. أظهرت دراسة خاصة أجريت على الأطفال حديثي الولادة أن الفتيات يظهرن رد فعل وجهيًا أكثر وضوحًا استجابة للتحفيز المؤلم مقارنة بالأولاد. للعمر أيضًا تأثير كبير على إدراك الألم. تشير الملاحظات السريرية في معظم الحالات إلى أن شدة إدراك الألم تتناقص مع تقدم العمر. على سبيل المثال، تزداد نسبة الإصابة بالنوبات القلبية الصامتة لدى المرضى الذين تزيد أعمارهم عن 65 عامًا، كما تزيد أيضًا نسبة الإصابة بقرحة المعدة الصامتة. ومع ذلك، يمكن تفسير هذه الظواهر من خلال السمات المختلفة لمظاهر العمليات المرضية في الشيخوخة، وليس من خلال انخفاض في إدراك الألم على هذا النحو.
عند نمذجة الألم المرضي عن طريق تطبيق الكابسيسين على الجلد، عانى الشباب وكبار السن من الألم وفرط التألم بنفس الشدة. ومع ذلك، في كبار السن، كانت هناك فترة كمون أطول قبل ظهور الألم وقبل تطور الحد الأقصى لشدة الألم. عند كبار السن، يستمر الألم وفرط التألم لفترة أطول من الشباب. وخلص إلى أنه في المرضى المسنين، يتم تقليل مرونة الجهاز العصبي المركزي أثناء التحفيز المؤلم لفترة طويلة.
سريريًا، يؤدي هذا إلى شفاء أبطأ وزيادة حساسية الألم لفترة طويلة بعد إصابة الأنسجة. [ريشتنياك في كيه، كوكوشكين إم إل، 2003]. ومن المعروف أيضًا أن المجموعات العرقية التي تعيش في المناطق الشمالية من الكوكب تتحمل الألم بسهولة أكبر مقارنة بالجنوبيين [ميلزاك ر.، 1981]. كما ذكرنا سابقًا، الألم ظاهرة متعددة المكونات ويعتمد إدراكها على عوامل عديدة. لذلك، من الصعب جدًا إعطاء تعريف واضح وشامل للألم. التعريف الأكثر شيوعًا هو التعريف الذي اقترحه مجموعة من الخبراء من الرابطة الدولية لدراسة الألم: "الألم هو إحساس غير سار وتجربة عاطفية مرتبطة بتلف الأنسجة الفعلي أو المحتمل أو وصفها من حيث هذا الضرر. " يشير هذا التعريف إلى أن الإحساس بالألم يمكن أن يحدث ليس فقط عند تلف الأنسجة أو في ظروف خطر تلف الأنسجة، ولكن حتى في حالة عدم وجود أي ضرر.
وفي الحالة الأخيرة، تحديد آلية الألمهي الحالة النفسية والعاطفية للشخص (وجود الاكتئاب أو الهستيريا أو الذهان). بمعنى آخر، تفسير الشخص للإحساس بالألم ورد فعله العاطفي وسلوكه قد لا يرتبط بخطورة الإصابة. . يمكن تقسيم الألم إلى سطحي جسدي (في حالة تلف الجلد)، وجسدي عميق (في حالة تلف الجهاز العضلي الهيكلي)، وألم حشوي. يمكن أن يحدث الألم عندما تتضرر هياكل الجهاز العصبي المحيطي و/أو المركزي المشاركة في إجراء وتحليل إشارات الألم. ألم الاعتلال العصبي هو الألم الذي يحدث عند تلف الأعصاب الطرفية، وعندما تتضرر هياكل الجهاز العصبي المركزي يسمى الألم المركزي. [ريشتنياك في.ك.، 1985]. هناك مجموعة خاصة تتكون من الألم النفسي، الذي يحدث بغض النظر عن الضرر الجسدي أو الحشوي أو العصبي ويتم تحديده بواسطة عوامل نفسية واجتماعية. وفقا لمعايير الوقت، يتم التمييز بين الألم الحاد والمزمن.
الم حاد- هذا ألم جديد وحديث يرتبط ارتباطًا وثيقًا بالضرر الذي سببه، وكقاعدة عامة، هو أحد أعراض بعض الأمراض. ويختفي هذا الألم عند إزالة الضرر. [كاليوزني إل في، 1984].ألم مزمنوغالباً ما يكتسب صفة المرض المستقل، ويستمر لفترة طويلة من الزمن وقد لا يتم تحديد السبب المسبب لهذا الألم في بعض الحالات. وتعرفه الجمعية الدولية لدراسة الألم بأنه "الألم الذي يستمر إلى ما بعد فترة الشفاء الطبيعية". الفرق الرئيسي بين الألم المزمن والألم الحاد ليس عامل الوقت، ولكن العلاقات الفسيولوجية العصبية والكيميائية الحيوية والنفسية والسريرية مختلفة نوعياً. يعتمد تكوين الألم المزمن بشكل كبير على مجموعة من العوامل النفسية. الألم المزمن هو القناع المفضل للاكتئاب الخفي. يتم تفسير العلاقة الوثيقة بين الاكتئاب والألم المزمن من خلال الآليات البيوكيميائية الشائعة . يتم ضمان إدراك الألم من خلال نظام مسبب للألم معقد، والذي يتضمن مجموعة خاصة من المستقبلات الطرفية والخلايا العصبية المركزية الموجودة في العديد من هياكل الجهاز العصبي المركزي وتستجيب للتأثيرات الضارة. يتوافق التنظيم الهرمي متعدد المستويات للجهاز المستقبل للألم مع الأفكار النفسية العصبية حول التوطين الديناميكي لوظائف الدماغ ويرفض فكرة "مركز الألم" كبنية مورفولوجية محددة، والتي من شأنها أن تساعد إزالتها في القضاء على متلازمة الألم .
تم تأكيد هذا البيان من خلال العديد من الملاحظات السريرية التي تشير إلى أن التدمير الجراحي العصبي لأي من الهياكل المسببة للألم لدى المرضى الذين يعانون من متلازمات الألم المزمن لا يجلب سوى راحة مؤقتة. يتم تصنيف متلازمات الألم التي تنشأ نتيجة تنشيط المستقبلات المسببة للألم أثناء الإصابة والالتهاب ونقص التروية وتمدد الأنسجة على أنها متلازمات ألم جسدية. سريريًا، تتجلى متلازمات الألم الجسدي في وجود ألم مستمر و/أو زيادة حساسية الألم في منطقة الضرر أو الالتهاب. كقاعدة عامة، يمكن للمرضى تحديد موقع هذا الألم بسهولة وتحديد شدته وطبيعته بوضوح. مع مرور الوقت، يمكن لمنطقة زيادة حساسية الألم أن تتوسع وتتجاوز الأنسجة التالفة. تسمى المناطق التي تعاني من زيادة حساسية الألم للمنبهات الضارة بمناطق فرط التألم.
هناك فرط التألم الابتدائي والثانوي. يغطي فرط التألم الأولي الأنسجة التالفة، بينما يتم تحديد فرط التألم الثانوي خارج المنطقة المتضررة. من الناحية النفسية والفيزيائية، تتميز مناطق فرط التألم الجلدي الأولي بانخفاض في عتبات الألم وتحمل الألم للمنبهات الميكانيكية والحرارية الضارة.
تتمتع مناطق فرط التألم الثانوي بعتبة ألم طبيعية وانخفاض في تحمل الألم فقط للمنبهات الميكانيكية. الأساس الفيزيولوجي المرضي لفرط التألم الأولي هو التحسس (زيادة الحساسية) لمستقبلات الألم - الألياف A وC لعمل المنبهات الضارة. يتجلى تحسس مستقبلات الألم من خلال انخفاض عتبة التنشيط، وتوسيع مجالات الاستقبال، وزيادة تواتر ومدة التفريغ في الألياف العصبية، مما يؤدي إلى زيادة في التدفق المستقبل للألم [وول بي دي، ميلزاك ر.، 1994]. يؤدي الضرر الخارجي أو الداخلي إلى سلسلة من العمليات الفيزيولوجية المرضية التي تؤثر على الجهاز المسبب للألم بأكمله (من مستقبلات الأنسجة إلى الخلايا العصبية القشرية)، بالإضافة إلى عدد من الأنظمة التنظيمية الأخرى في الجسم. يؤدي الضرر الخارجي أو الداخلي إلى إطلاق مواد فعالة وعائيًا مما يؤدي إلى تطور الالتهاب. لا تسبب هذه المواد النشطة في الأوعية الدموية أو ما يسمى بالوسطاء الالتهابيين مظاهر نموذجية للالتهاب فحسب، بما في ذلك تفاعل الألم الواضح، ولكنها تزيد أيضًا من حساسية مستقبلات الألم للتهيجات اللاحقة. هناك عدة أنواع من وسطاء الالتهابات.
I. وسطاء الالتهاب في البلازما
- نظام كاليكريين كينين: براديكينين، كاليدين
- المكونات المكملة: C2-C4، C3a، C5 - سموم الحساسية المفرطة، C3b - أوبسونين، C5-C9 - مركب الهجوم الغشائي
- نظام الإرقاء وانحلال الفيبرين: العامل الثاني عشر (عامل هاجمان)، الثرومبين، الفيبرينوجين، الببتيدات الفيبرينية، البلازمين، إلخ.
ثانيا. وسطاء الالتهاب الخلوية
- الأمينات الحيوية: الهستامين، السيروتونين، الكاتيكولامينات
- مشتقات حمض الأراكيدونيك: - البروستاجلاندين (PGE1، PGE2، PGF2؟، الثرومبوكسان A2، البروستاسيكلين I2)، - الليكوترين (LTV4، MRS (A) - مادة الحساسية المفرطة بطيئة التفاعل)، - الدهون الكيميائية
- العوامل المحببة: البروتينات الكاتيونية، البروتياز المحايدة والحمضية، الإنزيمات الليزوزومية
- عوامل الانجذاب الكيميائي: عامل الجذب الكيميائي للعدلات، عامل الجذب الكيميائي اليوزيني، إلخ.
- جذور الأكسجين: O2-فوق أكسيد، H2O2، NO، مجموعة OH-هيدروكسيل
- جزيئات الالتصاق: الإنتغرينات، الإنتغرينات
- السيتوكينات: IL-1، IL-6، عامل نخر الورم، الكيموكينات، الإنترفيرون، عامل تحفيز المستعمرة، إلخ.
- النيوكليوتيدات والنيوكليوسيدات: ATP، ADP، الأدينوزين
- الناقلات العصبية والببتيدات العصبية: المادة P، الببتيد المرتبط بجين الكالسيتونين، النيوروكينين A، الغلوتامات، الأسبارتات، النورإبينفرين، الأسيتيل كولين.
حاليًا، تم تحديد أكثر من 30 مركبًا كيميائيًا عصبيًا تشارك في آليات إثارة وتثبيط الخلايا العصبية المسببة للألم في الجهاز العصبي المركزي. من بين مجموعة كبيرة من الناقلات العصبية والهرمونات العصبية والمعدلات العصبية التي تتوسط في توصيل الإشارات المسببة للألم، فهي موجودة كجزيئات بسيطة - تحفيز الأحماض الأمينية - BAK(الغلوتامات، الأسبارتات) والمركبات الجزيئية المعقدة العالية (المادة P، النيوروكينين A، الببتيد المرتبط بجينات الكالسيتونين، وما إلى ذلك).
تلعب VACs دورًا مهمًا في آليات الإحساس بالألم. يوجد الغلوتامات في أكثر من نصف الخلايا العصبية في العقد الظهرية ويتم إطلاقه تحت تأثير نبضات مسببة للألم. تتفاعل BACs مع عدة أنواع فرعية من مستقبلات الغلوتامات. هذه هي في المقام الأول مستقبلات الأيونوتروبيك: مستقبلات NMDA (N-methyl-D-aspartate) ومستقبلات AMPA (β-amino-3-hydroxy-5-methyl-4-isoxazole-propionic acid)، بالإضافة إلى مستقبلات الغلوتامات المعدنية. .
عندما يتم تنشيط هذه المستقبلات، تدخل أيونات Ca 2+ بشكل مكثف إلى الخلية ويتغير نشاطها الوظيفي. يتم تشكيل فرط استثارة الخلايا العصبية المستمر ويحدث فرط التألم. يجب التأكيد على أن حساسية الخلايا العصبية المسببة للألم الناتجة عن تلف الأنسجة يمكن أن تستمر لعدة ساعات أو أيام حتى بعد توقف تلقي النبضات المسببة للألم من المحيط. وبعبارة أخرى، إذا حدث فرط نشاط الخلايا العصبية المسببة للألم بالفعل، فإنه لا يتطلب إعادة شحن إضافية عن طريق النبضات من موقع الضرر. ترتبط الزيادة طويلة المدى في استثارة الخلايا العصبية المسببة للألم بتنشيط أجهزتها الوراثية - التعبير عن الجينات المبكرة والمستجيبة على الفور، مثل c-fos، وc-jun، وjunB وغيرها. على وجه الخصوص، تم إثبات وجود علاقة إيجابية بين عدد الخلايا العصبية الإيجابية ودرجة الألم. في آليات تنشيط الجينات الورمية الأولية، تلعب أيونات Ca 2+ دورًا مهمًا. مع زيادة تركيز أيونات Ca 2+ في العصارة الخلوية، بسبب زيادة دخولها عبر قنوات Ca التي تنظمها مستقبلات NMDA، يحدث التعبير عن c-fos، c-jun، وتشارك منتجات البروتين الخاصة بها في التنظيم استثارة غشاء الخلية على المدى الطويل . في الآونة الأخيرة، تم إعطاء أكسيد النيتريك (NO)، الذي يلعب في الدماغ دور جهاز إرسال غير نمطي خارج المشبكي، أهمية في آليات توعية الخلايا العصبية المسببة للألم.
حجمه الصغير ونقص الشحنة يسمحان لـ NO باختراق غشاء البلازما والمشاركة في نقل الإشارات بين الخلايا، مما يؤدي إلى توصيل الخلايا العصبية بعد وما قبل المشبكي وظيفيًا. يتم إنتاج NO من L-arginine في الخلايا العصبية التي تحتوي على إنزيم NO Synthetase. يتم إطلاق NO من الخلايا أثناء الإثارة التي يسببها NMDA ويتفاعل مع النهايات قبل المشبكي للعناصر C، مما يعزز إطلاق الأحماض الأمينية المثيرة للغلوتامات والنيوروكينين منها. [كوكوشكين إم إل وآخرون، 2002؛ شوماتوف ف.ب وآخرون، 2002]. يلعب أكسيد النيتريك دورًا رئيسيًا في العمليات الالتهابية. يؤدي الحقن الموضعي لمثبطات NO سينسيز في المفصل إلى منع انتقال مسببات الألم والالتهاب بشكل فعال.
كل هذا يدل على أن أكسيد النيتريك يتكون في المفاصل الملتهبة . Kinins هي من بين أقوى المعدِّلات الطحالبية. تتشكل بسرعة عند تلف الأنسجة وتسبب معظم التأثيرات الملحوظة في الالتهاب: توسع الأوعية، وزيادة نفاذية الأوعية الدموية، وتسرب البلازما، وهجرة الخلايا، والألم، وفرط التألم. أنها تنشط ألياف C، مما يؤدي إلى التهاب عصبي بسبب إطلاق المادة P والببتيد المرتبط بجين الكالسيتونين والناقلات العصبية الأخرى من النهايات العصبية.
التأثير الاستثاري المباشر للبراديكينين على النهايات العصبية الحسية يتم بوساطة مستقبلات B2 ويرتبط بتنشيط غشاء فسفوليباز C. التأثير الاستثاري غير المباشر للبراديكينين على نهايات العصب الوارد يرجع إلى تأثيره على عناصر الأنسجة المختلفة (الخلايا البطانية، الخلايا الليفية والخلايا البدينة والبلاعم والعدلات) وتحفيز تكوين وسطاء التهابات فيها، والتي تتفاعل مع المستقبلات المقابلة على النهايات العصبية، وتنشط غشاء أدينيلات سيكلاز. بدوره، يحفز إنزيم محلقة الأدينيلات والفوسفوليباز C تكوين الإنزيمات التي تفسفر بروتينات القناة الأيونية.
نتيجة فسفرة بروتينات القناة الأيونية هي تغيير في نفاذية الغشاء للأيونات، مما يؤثر على استثارة النهايات العصبية والقدرة على توليد نبضات عصبية. يحفز البراديكينين، الذي يعمل من خلال مستقبلات B2، تكوين حمض الأراكيدونيك مع التكوين اللاحق للبروستاجلاندين والبروستاسيكلين والثرومبوكسان والليكوترين. هذه المواد، التي لها تأثير طحلبي مستقل واضح، تعمل بدورها على تعزيز قدرة الهيستامين والسيروتونين والبراديكينين على توعية النهايات العصبية. ونتيجة لذلك، يزداد إطلاق التاكيكينين (المادة P والنيوروكينين A) من وكلاء C غير المايلينين، مما يؤدي إلى زيادة نفاذية الأوعية الدموية، مما يزيد من التركيز المحلي للوسطاء الالتهابيين. [ريشتنياك في كيه، كوكوشكين إم إل، 2001].
استخدام الجلايكورتيكويد يمنع تكوين حمض الأراكيدونيك عن طريق تثبيط نشاط الفسفوليباز A2. وبدورها، الأدوية المضادة للالتهابات غير الستيرويدية (مضادات الالتهاب غير الستيروئيدية)يمنع تكوين الأكسيد الداخلي الحلقي، وخاصة البروستاجلاندين. يجمع الاسم العام لمضادات الالتهاب غير الستيروئيدية بين المواد ذات التركيبات الكيميائية المختلفة التي لها تأثير مثبط على إنزيمات الأكسدة الحلقية. جميع مضادات الالتهاب غير الستيروئيدية لها تأثيرات مضادة للالتهابات وخافضة للحرارة ومسكنة بدرجات متفاوتة. ولسوء الحظ، فإن جميع مضادات الالتهاب غير الستيروئيدية تقريبًا لها آثار جانبية كبيرة عند استخدامها على المدى الطويل. أنها تسبب عسر الهضم والقرحة الهضمية ونزيف الجهاز الهضمي. قد يحدث أيضًا انخفاض لا رجعة فيه في معدل الترشيح الكبيبي، مما يؤدي إلى التهاب الكلية الخلالي والفشل الكلوي الحاد. مضادات الالتهاب غير الستيروئيدية لها تأثير سلبي على دوران الأوعية الدقيقة ويمكن أن تسبب تشنج قصبي [فيلاتوفا إي جي، فين إيه إم، 1999؛ تشيتشاسوفا إن في، 2001؛ ناسونوف إل، 2001].
من المعروف حاليًا أن هناك نوعين من إنزيمات الأكسدة الحلقية. يتشكل إنزيم الأكسدة الحلقية-1 (COX-1) في الظروف العادية، ويتشكل إنزيم الأكسدة الحلقية-2 (COX-2) أثناء الالتهاب. حاليًا، يهدف تطوير مضادات الالتهاب غير الستيروئيدية الفعالة إلى إنشاء مثبطات انتقائية لـ COX-2، والتي، على عكس المثبطات غير الانتقائية، لها آثار جانبية أقل وضوحًا بشكل ملحوظ. ومع ذلك، هناك أدلة على أن الأدوية ذات النشاط المثبط "المتوازن" تجاه COX-1 وCOX-2 قد يكون لها نشاط مضاد للالتهابات ومسكن أكثر وضوحًا مقارنة بمثبطات COX-2 المحددة. [ناسونوف إي إل، 2001].
جنبا إلى جنب مع تطوير الأدوية التي تمنع COX-1 و COX-2، يجري البحث عن أدوية مسكنة جديدة بشكل أساسي. من المفترض أن مستقبلات B1 هي المسؤولة عن الالتهاب المزمن. مضادات هذه المستقبلات تقلل بشكل كبير من مظاهر الالتهاب. بالإضافة إلى ذلك، يشارك البراديكينين في إنتاج ثنائي الجلسرين وينشط بروتين كيناز C، والذي بدوره يعزز حساسية الخلايا العصبية.
يلعب بروتين كيناز C دورًا مهمًا جدًا في الإحساس بالألم، ويتم البحث عن الأدوية التي يمكن أن تمنع نشاطه. . بالإضافة إلى تخليق وإطلاق وسطاء الالتهابات، وفرط استثارة الخلايا العصبية المسببة للألم في العمود الفقري وزيادة التدفق الوارد إلى الهياكل المركزية للدماغ، يلعب نشاط الجهاز العصبي الودي دورًا معينًا. لقد ثبت أن الزيادة في حساسية أطراف العناصر المسببة للألم عند تنشيط الألياف الودية بعد العقدية يتم التوسط فيها بطريقتين. أولاً، بسبب زيادة نفاذية الأوعية الدموية في منطقة الضرر وزيادة تركيز وسطاء الالتهابات (المسار غير المباشر)، وثانياً، بسبب التأثير المباشر للناقلات العصبية للجهاز العصبي الودي - النورإبينفرين والأدرينالين على المستقبلات الأدرينالية a2 الموجودة على غشاء مستقبلات الألم. أثناء الالتهاب، يتم تنشيط ما يسمى بالخلايا العصبية المسببة للألم "الصامتة"، والتي في حالة عدم وجود التهاب لا تستجيب لأنواع مختلفة من المحفزات المسببة للألم.
جنبا إلى جنب مع زيادة في تدفق مسبب للألم أثناء الالتهاب، هناك زيادة في التحكم التنازلي . يحدث هذا نتيجة لتنشيط نظام مضاد للألم. يتم تنشيطه عندما تصل إشارة الألم إلى الهياكل المضادة للألم في جذع الدماغ والمهاد والقشرة الدماغية. [ريشتنياك في كيه، كوكوشكين إم إل، 2001]. يؤدي تنشيط المادة الرمادية المحيطة بالمسالي ونواة الرفاء الكبيرة إلى إطلاق الإندورفين والإنكيفالين، اللذين يرتبطان بالمستقبلات، مما يؤدي إلى سلسلة من التغيرات الفيزيائية والكيميائية التي تقلل الألم. هناك ثلاثة أنواع رئيسية من المستقبلات الأفيونية:؟ -، ؟ - و؟ -المستقبلات. أكبر عدد من المسكنات المستخدمة تمارس تأثيرها من خلال التفاعل معها؟ -المستقبلات. حتى وقت قريب، كان من المقبول عمومًا أن المواد الأفيونية تعمل حصريًا على الجهاز العصبي وتنتج تأثيرًا مسكنًا من خلال التفاعل مع المستقبلات الأفيونية الموجودة في الدماغ والحبل الشوكي. ومع ذلك، توجد المستقبلات الأفيونية وروابطها في الخلايا المناعية ، في الأعصاب الطرفية ، في الأنسجة الملتهبة . من المعروف الآن أن 70٪ من مستقبلات الإندورفين والإنكيفالين موجودة في الغشاء قبل المشبكي لمستقبلات الألم، وفي أغلب الأحيان يتم قمع إشارة الألم (قبل الوصول إلى القرون الظهرية للحبل الشوكي).
هل ينشط الدينورفين؟ - المستقبلات ويمنع الخلايا العصبية البينية، مما يؤدي إلى إطلاق GABA، الذي يسبب فرط الاستقطاب لخلايا القرن الظهري ويمنع المزيد من نقل الإشارة . توجد المستقبلات الأفيونية في الحبل الشوكي بشكل رئيسي حول أطراف ألياف C في اللوحة الأولى من القرون الظهرية . يتم تصنيعها في أجسام الخلايا الصغيرة للعقد الظهرية ويتم نقلها بشكل قريب وبعيد على طول المحاور العصبية . تكون المستقبلات الأفيونية غير نشطة في الأنسجة غير الملتهبة بعد بداية الالتهاب، ويتم تنشيط هذه المستقبلات في غضون ساعات قليلة . يزداد أيضًا تخليق المستقبلات الأفيونية في الخلايا العصبية للعقد القرنية الظهرية أثناء الالتهاب، لكن هذه العملية، بما في ذلك وقت النقل عبر المحاور، تستغرق عدة أيام . لقد وجدت الدراسات السريرية أن حقن 1 ملغ من المورفين في مفصل الركبة بعد إزالة الغضروف المفصلي يعطي تأثيرًا مسكنًا واضحًا على المدى الطويل . وفي وقت لاحق، تم الكشف عن وجود المستقبلات الأفيونية في الأنسجة الزلالية الملتهبة .
وتجدر الإشارة إلى أن القدرة المواد الأفيونيةتم وصف التسبب في تأثير مسكن موضعي عند تطبيقه على الأنسجة في القرن الثامن عشر. وهكذا، نشر الطبيب الإنجليزي هيبردين عملاً في عام 1774 وصف فيه التأثير الإيجابي لتطبيق مستخلص الأفيون في علاج آلام البواسير. . يظهر تأثير مسكن جيد ديامورفينمع تطبيقه المحلي على التقرحات والمناطق الخبيثة من الجلد عند قلع الأسنان في حالات الالتهاب الشديد للأنسجة المحيطة بها . تعتمد التأثيرات المضادة لاستقبال الألم (التي تحدث خلال دقائق قليلة بعد استخدام المواد الأفيونية) في المقام الأول على منع انتشار جهود الفعل، وكذلك على انخفاض إطلاق الوسطاء المثيرين، وخاصة المادة P، من النهايات العصبية .يتم امتصاص المورفين بشكل سيئ من خلال الجلد الطبيعي ويتم امتصاصه بشكل جيد من خلال الجلد الملتهب. ولذلك، فإن تطبيق المورفين على الجلد يوفر فقط تأثير مسكن موضعي ولا يعمل بشكل نظامي.
في السنوات الأخيرة، بدأ عدد متزايد من المؤلفين يتحدثون عن مدى استصواب استخدام التسكين المتوازن، أي. الاستخدام المشترك لمضادات الالتهاب غير الستيروئيدية والمسكنات الأفيونيةمما يجعل من الممكن تقليل الجرعات وبالتالي الآثار الجانبية لكل من الأول والثاني [إجناتوف د.، زايتسيف أ.أ.، 2001؛ أوسيبوفا إن إيه، 1994؛ فيلاتوفا إي جي، فين إيه إم، 1999؛ ناسونوف إل، 2001].يتم استخدام المواد الأفيونية بشكل متزايد لعلاج آلام التهاب المفاصل [إجناتوف د.، زايتسيف أ. أ.، 2001]. على وجه الخصوص، يتم استخدام شكل بلعة من الترامادول حاليًا لهذا الغرض. هذا الدواء هو ناهض [دكتور ماشكوفسكي، 1993]، وبالتالي فإن احتمال الاعتماد الجسدي عند استخدام جرعات كافية منخفض. من المعروف أن المواد الأفيونية التي تنتمي إلى مجموعة الناهضات تسبب الاعتماد الجسدي بدرجة أقل بكثير مقارنة بالمواد الأفيونية الحقيقية. [فيلاتوفا إي جي، فين إيه إم، 1999].
ويُعتقد أن المواد الأفيونية، المستخدمة بالجرعات الصحيحة، أكثر أمانًا من مضادات الالتهاب غير الستيروئيدية التقليدية [إجناتوف د.، زايتسيف أ. أ.، 2001]. أحد أهم عوامل الألم المزمن هو إضافة الاكتئاب. وفقًا لبعض المؤلفين، يجب دائمًا استخدام مضادات الاكتئاب في علاج الألم المزمن، بغض النظر عن أسبابه المرضية. [فيلاتوفا إي جي، فين إيه إم، 1999].
تأثير مضاد للألم مضادات الاكتئابيتم تحقيقها من خلال ثلاث آليات. الأول هو انخفاض في أعراض الاكتئاب. ثانيًا، تعمل مضادات الاكتئاب على تنشيط أنظمة مضادات استقبال الألم السيروتونية والنورأدرينالية. الآلية الثالثة هي أن أميتريبتيلين ومضادات الاكتئاب ثلاثية الحلقات الأخرى تعمل كمضادات لمستقبل NMDA وتتفاعل مع نظام الأدينوزين الداخلي. وبالتالي، يشارك عدد كبير من الآليات الفسيولوجية العصبية والكيميائية العصبية المختلفة في التسبب في متلازمات الألم الناشئة عن الالتهاب، والتي تؤدي حتما إلى تغييرات في الحالة النفسية الفسيولوجية للمريض. لذلك، إلى جانب الأدوية المضادة للالتهابات والمسكنات، للعلاج المعقد القائم على العوامل المسببة للأمراض، كقاعدة عامة، من الضروري وصف مضادات الاكتئاب.
الأدب
- Valdman A.V.، Ignatov Yu.D. الآليات المركزية للألم. - ل.: العلوم، 1976. 191.
- أمراض داخلية. في 10 كتب. الكتاب الأول مترجم من الإنجليزية. إد. E. Braunwald، K. J. Isselbacher، R. G. Petersdorf، إلخ - M.: الطب، 1993، 560.
- Ignatov Yu.، Zaitsev A. A. الجوانب الحديثة لعلاج الألم: المواد الأفيونية. جودة الممارسة السريرية. 2001، 2، 2-13.
- الآليات الفسيولوجية لتنظيم حساسية الألم. م.: الطب، 1984، 215.
- Kukushkin M.L.، Grafova V.N.، Smirnova V.I et al. دور أكسيد النيتريك في آليات تطور الألم // التخدير. والإنعاش، 2002، 4، 4-6.
- Kukushkin M. L.، Reshetnyak V. K. آليات خلل التنظيم للألم المرضي. في: أمراض الخلل التنظيمي. (تم تحريره بواسطة G. N. Kryzhanovsky) م.: الطب، 2002. 616 -634.
- ماشكوفسكي (دكتور في الطب) الأدوية. 1993، م. الطب، 763.
- ميلزاك ر. سر الألم. لكل. من الانجليزية م: الطب، 1981، 231 ص.
- Nasonov E. L. التأثيرات المسكنة للأدوية المضادة للالتهابات غير الستيرويدية في أمراض الجهاز العضلي الهيكلي: توازن الفعالية والسلامة. كونسيليوم ميديكيوم، 2001، 5، 209-215.
- Osipova N. A. المبادئ الحديثة للاستخدام السريري للمسكنات ذات التأثير المركزي. عش. والإنعاش. 1994, 4, 16-20.
- Reshetnyak V.K. القواعد الفيزيولوجية العصبية للألم والتسكين المنعكس. نتائج العلم والتكنولوجيا. فينيتي. فيزيول. الإنسان والحيوان، 1985. 29. 39-103.
- Reshetnyak V.K.، Kukushkin M.L. الألم: الجوانب الفسيولوجية والفيزيولوجية المرضية. في: المشاكل الحالية للفيزيولوجيا المرضية (محاضرات مختارة). إد. بي بي موروز. م: الطب، 2001، 354-389.
- Reshetnyak V.K.، Kukushkin M.L. اختلافات العمر والجنس في إدراك الألم // علم الشيخوخة السريري، 2003، T 9، رقم 6، 34-38.
- Filatova E. G.، Vein A. M. علم عقاقير الألم. المجلة الطبية الروسية، 1999، 9، 410-418.
- Chichasova N. V. الاستخدام المحلي للمسكنات لأمراض المفاصل والعمود الفقري. كونسيليوم ميديكيوم، 2001، 5، 215-217.
- Shumatov V. B.، Shumatova T. A.، Balashova T. V. تأثير التسكين فوق الجافية مع المورفين على نشاط عدم تشكيل الخلايا العصبية المسببة للألم في العقد الشوكية والحبل الشوكي. تخدير. أنا ريانيماتول.، 2002، 4، 6-8.
- Back L. N.، Finlay I. التأثير المسكن للمواد الأفيونية الموضعية على تقرحات الجلد المؤلمة. // J. إدارة أعراض الألم، 1995، 10، 493.
- Cabot P. J.، Cramond T.، Smith M. T. التصوير الشعاعي الذاتي الكمي لمواقع ربط المواد الأفيونية الطرفية في رئة الفئران. يورو. جي فارماكول، 1996، 310، 47-53.
- Calixto J. B.، Cabrini D. A.، Ferreria J.، Kinins في الألم والالتهاب. الألم، 2000، 87، 1-5
- Coderre T. J.، Katz J.، Vaccarino A. L.، Melzack R. مساهمة المرونة العصبية المركزية في الألم المرضي: مراجعة الأدلة السريرية والتجريبية. باين، 1993، 52، 259-285.
- ديكنسون أ.ه. أين وكيف تعمل المواد الأفيونية. وقائع المؤتمر العالمي السابع للألم، التقدم في أبحاث الألم وإدارته، تحرير G. F. Gebhart، D. L. Hammond و T. S. Jensen، مطبعة IASP، سياتل، 1994، 2، 525-552.
- ديكنسون إيه إتش علم الصيدلة لنقل الألم والسيطرة عليه. الألم، 1996. مراجعة محدثة لمنهج الدورة التنشيطية (المؤتمر العالمي الثامن للألم)، مطبعة الرابطة الدولية لأخصائيي العلاج، سياتل، واشنطن، 1996، 113-121.
- حسن A. H. S.، Ableitner A.، Stein C.، Herz A. التهاب مخلب الفئران يعزز النقل المحوري لمستقبلات المواد الأفيونية في العصب الوركي ويزيد من كثافتها في الأنسجة الملتهبة.// علم الأعصاب.., 1993, 55, ص185-195.
- Krainik M.، Zylicz Z. المورفين الموضعي للألم الجلدي الخبيث. مسكنة. ميد، 1997، 11، 325.
- كراجنيك إم، زيليكز زد، فينلي آي وآخرون. الاستخدامات المحتملة للمواد الأفيونية الموضعية في تقرير الرعاية التلطيفية لـ 6 حالات. الألم، 1999، 80، 121-125.
- Lawand N. B.، McNearney T.، Wtstlund N. إطلاق الأحماض الأمينية في مفصل الركبة: دور رئيسي في حس الألم والالتهاب، الألم، 2000، 86، 69-74.
- لورانس A. J.، جوشي G. P.، Michalkiewicz A. وآخرون. دليل على التسكين بوساطة مستقبلات المواد الأفيونية الطرفية في الأنسجة الزلالية الملتهبة .// يورو. جيه كلين. فارماكول.، 1992، 43، ص 351-355.
- ليكار ر.، سيتل ر.، جراجر ك. وآخرون. تسكين المورفين المحيطي في جراحة الأسنان. باين، 1998، 76، 145-150.
- ليكار ر.، سيتل ر.، جراجر ك. وآخرون. المستقبلات الأفيونية. مظاهرته في الأنسجة العصبية. العلوم، 1973، 179، 1011-1014.
- برزيولوكي ر.، حسن أ.س.، لاسون دبليو وآخرون. التعبير الجيني وتوطين الببتيدات الأفيونية في الخلايا المناعية للأنسجة الملتهبة: دور وظيفي في مضاد للألم. علم الأعصاب، 1992، 48، 491-500.
- Ren K.، Dubner R. التعديل التنازلي المحسن لحس الألم لدى الفئران المصابة بالتهاب مؤخر القدم المستمر. J. الفيزيولوجيا العصبية، 1996، 76، 3025-3037.
- Schafer M.، Imai Y.، Uhl G. R.، Stein C. Inflammation يعزز التسكين المحيطي بوساطة مستقبلات المواد الأفيونية، ولكن ليس نسخ مستقبلات المواد الأفيونية في العقد الجذرية الظهرية // يورو. جي فارماكول، 1995، 279، 165-169.
- ستاين سي، كوميسيل ك، هيميرل إي وآخرون. التأثير المسكن للمورفين داخل المفصل بعد جراحة الركبة بالمنظار. // ن. إنجل. ميد، 1991؛ 325: ص. 1123-1126.
- Torebjork E.، ديناميات مستقبلات الألم في البشر، في: G. F. Gebhart، D. L. Hammond and T. S. Jensen (Eds.)، وقائع المؤتمر العالمي السابع للألم. التقدم في أبحاث الألم وإدارته، مطبعة IASP، سياتل، واشنطن، 1994، 2، ص. 277-284.
- Wall P. D.، Melzack R. (Eds) كتاب الألم، الطبعة الثالثة، تشرشل ليفينغستون، إدنبرة، 1994.
- Wei F.، Dubner R.، Ren K. Nucleus retularis gigantocularis and nucleus Raphe magnus في جذع الدماغ يمارسان تأثيرات معاكسة على فرط التألم السلوكي وتعبير بروتين Fos الشوكي بعد الالتهاب المحيطي. الألم، 1999، 80، 127-141.
- Wei R.، Ren K.، Dubner R. تم تعزيز تعبير بروتين Fos الناجم عن الالتهاب في الحبل الشوكي للفئران بعد آفات الحويصلة الظهرية الجانبية أو البطنية الجانبية. دقة الدماغ.، 1998، 782، 116-141.
- دورات ويلكاكس جي إل IASP التنشيطية حول إدارة الألم، 1999، 573-591.
- آليات ويليس دبليو دي لنقل الإشارة. الألم 1996 – مراجعة محدثة. منهج الدورة التنشيطية (المؤتمر العالمي الثامن للألم)، مطبعة IASP، سياتل، واشنطن، 1996، 527-531.
- زيمليكمان ر.، جيفيل د.، إلياهو ه. وآخرون. التعبير عن مستقبلات المواد الأفيونية أثناء تكوين القلب في الفئران ذات الضغط الطبيعي وارتفاع ضغط الدم. // التداول، 1996؛ 93:ص. 1020-1025.
اشتعال- رد فعل موضعي معقد للجسم تجاه الضرر، يهدف إلى تدمير العامل المدمر واستعادة الأنسجة التالفة، والذي يتجلى في التغيرات المميزة في الأوعية الدموية الدقيقة والأنسجة الضامة.
علامات الالتهابكانت معروفة لدى الأطباء القدماء، الذين اعتقدوا أنها تتميز بخمسة أعراض: الاحمرار (rubor)، وتورم الأنسجة (الورم)، والحرارة (calor)، والألم (dolor)، والخلل الوظيفي (function laesa). للدلالة على الالتهاب، تتم إضافة النهاية "هو" إلى اسم العضو الذي يتطور فيه: التهاب القلب - التهاب القلب، التهاب الكلية - التهاب الكلى، التهاب الكبد - التهاب الكبد، إلخ.
المعنى البيولوجي للالتهابيتكون من تحديد وإزالة مصدر الضرر والعوامل المسببة للأمراض التي تسببت فيه، وكذلك استعادة التوازن.
يتميز الالتهاب بالميزات التالية.
اشتعال- هذا رد فعل وقائي تكيفي نشأ أثناء التطور. بفضل الالتهاب، يتم تحفيز العديد من أنظمة الجسم، والتخلص من العوامل المعدية أو غيرها من العوامل الضارة؛ عادة، نتيجة للالتهاب، تنشأ المناعة وتنشأ علاقات جديدة مع البيئة.
نتيجة لذلك، ليس فقط الأفراد، ولكن أيضا البشرية، كأنواع بيولوجية، تتكيف مع التغيرات في العالم الذي تعيش فيه - الغلاف الجوي، والبيئة، والعالم المصغر، وما إلى ذلك. ومع ذلك، في شخص معين، يمكن أن يؤدي الالتهاب في بعض الأحيان إلى مضاعفات خطيرة، حتى حتى وفاة المريض، حيث أن مسار العملية الالتهابية يتأثر بتفاعل جسم هذا الشخص - عمره، وحالة أنظمة الدفاع، وما إلى ذلك. لذلك، غالبا ما يتطلب الالتهاب تدخلا طبيا.
اشتعال- عملية مرضية عامة نموذجية يستجيب بها الجسم لمجموعة متنوعة من التأثيرات، لذلك تحدث في معظم الأمراض ويتم دمجها مع تفاعلات أخرى.
يمكن أن يكون الالتهاب مرضا مستقلا في الحالات التي يشكل فيها أساس المرض (على سبيل المثال، الالتهاب الرئوي الفصي، التهاب العظم والنقي، التهاب السحايا القيحي، وما إلى ذلك). في هذه الحالات، يكون للالتهاب جميع علامات المرض، أي سبب محدد وآلية فريدة للتقدم والمضاعفات والنتائج، الأمر الذي يتطلب علاجًا مستهدفًا.
الالتهاب والمناعة.
هناك علاقة مباشرة وعكسية بين الالتهاب والمناعة، حيث أن كلتا العمليتين تهدفان إلى "تطهير" البيئة الداخلية للجسم من العامل الغريب أو "الذات" المتغيرة، يليه رفض العامل الأجنبي والقضاء على العامل الأجنبي. عواقب الضرر. في عملية الالتهاب تتشكل ردود الفعل المناعية، وتتحقق الاستجابة المناعية نفسها من خلال الالتهاب، ويعتمد مسار الالتهاب على شدة الاستجابة المناعية للجسم. إذا كانت الدفاعات المناعية فعالة، فقد لا يتطور الالتهاب على الإطلاق. عندما تحدث تفاعلات مناعية لفرط الحساسية (انظر الفصل 8)، يصبح الالتهاب هو مظهرها المورفولوجي - يتطور الالتهاب المناعي (انظر أدناه).
لتطوير الالتهاب، بالإضافة إلى العامل المدمر، من الضروري الجمع بين مختلف المواد النشطة بيولوجيا، وخلايا معينة، والعلاقات بين الخلايا ومصفوفة الخلايا، وتطوير تغيرات الأنسجة المحلية والتغيرات العامة في الجسم.
اشتعالهي مجموعة معقدة من العمليات التي تتكون من ثلاثة ردود فعل مترابطة - التغيير (الضرر)، والنضح، والانتشار.
إن غياب واحد على الأقل من هذه التفاعلات المكونة الثلاثة لا يسمح لنا بالحديث عن الالتهاب.
التغيير هو تلف الأنسجة الذي تحدث فيه تغييرات مختلفة في المكونات الخلوية وخارج الخلية في موقع عمل العامل المدمر.
نضح- الدخول إلى مكان التهاب الإفرازات، أي سائل غني بالبروتين يحتوي على عناصر مكونة من الدم، حسب الكمية التي تتكون منها الإفرازات المختلفة.
الانتشار- تكاثر الخلايا وتكوين المصفوفة خارج الخلية بهدف استعادة الأنسجة التالفة.
الشرط الضروري لتطور هذه التفاعلات هو وجود وسطاء التهابات.
واجهة- المواد النشطة بيولوجيا التي توفر الروابط الكيميائية والجزيئية بين العمليات التي تحدث في موقع الالتهاب والتي بدونها يكون تطور العملية الالتهابية مستحيلا.
هناك مجموعتان من وسطاء الالتهابات:
وسطاء الالتهاب الخلوي (أو الأنسجة).، والتي يتم من خلالها تنشيط رد فعل الأوعية الدموية وضمان النضح. يتم إنتاج هذه الوسائط بواسطة الخلايا والأنسجة، وخاصة الخلايا البدينة (الخلايا البدينة)، والخلايا المحببة القاعدية واليوزينية، والخلايا الوحيدة، والبلاعم، والخلايا الليمفاوية، وخلايا نظام APUD، وما إلى ذلك. وأهم الوسائط الخلوية للالتهاب هي:
الأمينات حيوية المنشأ،وخاصة الهيستامين والسيروتونين، اللذين يسببان توسعًا حادًا (توسعًا) للأوعية الدموية الدقيقة، مما يزيد من نفاذية الأوعية الدموية، ويعزز وذمة الأنسجة، ويزيد من تكوين المخاط وتقلص العضلات الملساء:
- الدهون الحمضيةتتشكل عند تلف الخلايا والأنسجة وتكون في حد ذاتها مصدرًا لوسطاء التهابات الأنسجة.
- مادة تنظيم بطيئة من الحساسية المفرطةيزيد من نفاذية الأوعية الدموية.
- العامل الكيميائي اليوزيني أيزيد من نفاذية الأوعية الدموية ووصول الحمضات إلى موقع الالتهاب.
- عامل تنشيط الصفائح الدمويةيحفز الصفائح الدموية ووظائفها المتعددة الأوجه.
- البروستاجلاندانلها نطاق واسع من التأثير، بما في ذلك إتلاف الأوعية الدموية الدقيقة، وزيادة نفاذيتها، وتعزيز الانجذاب الكيميائي، وتعزيز تكاثر الخلايا الليفية.
وسطاء البلازما للالتهاباتتتشكل نتيجة التنشيط تحت تأثير العامل المدمر والوسطاء الخلويين لالتهاب ثلاثة أنظمة بلازما - أنظمة مكملة، أنظمة البلازمين(نظام كالكريين كينين) و نظام تخثر الدم. جميع مكونات هذه الأنظمة موجودة في الدم على شكل سلائف وتبدأ في العمل فقط تحت تأثير بعض المنشطات.
- وسطاء نظام القرينهما البراديكينين والكاليكرين. يزيد البراديكينين من نفاذية الأوعية الدموية، ويسبب الألم، وله خصائص خافضة للضغط. يقوم كاليكرين بتنفيذ التسمم الكيميائي للكريات البيض وينشط عامل هاجمان، وبالتالي يشمل نظام تخثر الدم وانحلال الفيبرين في العملية الالتهابية.
- عامل هاجمان، وهو مكون رئيسي في نظام تخثر الدم، ويبدأ تخثر الدم، وينشط وسطاء التهابات البلازما الأخرى، ويزيد من نفاذية الأوعية الدموية، ويعزز هجرة الكريات البيض المتعادلة وتراكم الصفائح الدموية.
- نظام كامليتكون من مجموعة من بروتينات بلازما الدم الخاصة التي تسبب تحلل البكتيريا والخلايا، وتزيد المكونات التكميلية C3b وC5b من نفاذية الأوعية الدموية، وتعزز حركة كريات الدم البيضاء متعددة الأشكال (PMN)، والخلايا الوحيدة والبلاعم إلى موقع الالتهاب.
متفاعلات المرحلة الحادة- مواد بروتينية نشطة بيولوجيًا، والتي بفضلها لا يشارك نظام دوران الأوعية الدقيقة والجهاز المناعي في الالتهاب فحسب، بل أيضًا أجهزة الجسم الأخرى، بما في ذلك الغدد الصماء والجهاز العصبي.
من بين المواد المتفاعلة في المرحلة الحادة، أهمها:
- بروتين سي التفاعلي،يزيد تركيزه في الدم بمقدار 100-1000 مرة أثناء الالتهاب، وينشط نشاط التحلل الخلوي للخلايا اللمفاوية التائية القاتلة. يبطئ تراكم الصفائح الدموية.
- إنترلوكين-1 (IL-1)، يؤثر على نشاط العديد من خلايا التركيز الالتهابي، وخاصة الخلايا اللمفاوية التائية، PMNs، ويحفز تخليق البروستاجلاندين والبروستاسيكلين في الخلايا البطانية، ويعزز الإرقاء في التركيز الالتهابي.
- تي كينينوجين هو مقدمة لوسطاء التهابات البلازما - الأقارب، ويمنع (بروتينات السيستين.
وهكذا، في موقع الالتهاب، تنشأ مجموعة من العمليات المعقدة للغاية التي لا يمكن أن تستمر بشكل مستقل لفترة طويلة، دون أن تكون إشارة لتنشيط أجهزة الجسم المختلفة. مثل هذه الإشارات هي تراكم وتداول المواد النشطة بيولوجيا، الأقارب، في الدم. المكونات التكميلية، البروستاجلاندين، الإنترفيرون، إلخ. ونتيجة لذلك، فإن نظام المكونة للدم، والمناعة، والغدد الصماء، والجهاز العصبي، أي الجسم ككل، متورط في الالتهاب. لذلك، بعبارات واسعة يجب اعتبار الالتهاب مظهرًا محليًا لرد الفعل العام للجسم.
عادة ما يصاحب الالتهاب تسمم. لا يرتبط فقط بالالتهاب نفسه، ولكن أيضًا بخصائص العامل المدمر، وفي المقام الأول العامل المعدي. مع زيادة مساحة الضرر وشدة التغيير، يزداد امتصاص المنتجات السامة ويزداد التسمم، مما يثبط أنظمة الحماية المختلفة للجسم - المختصة بالمناعة، المكونة للدم، البلاعم، إلخ. غالبًا ما يكون للتسمم تأثير حاسم على المسار وطبيعة الالتهاب . ويرجع ذلك في المقام الأول إلى عدم كفاية فعالية الالتهاب، على سبيل المثال، في التهاب الصفاق المعمم الحاد، وأمراض الحروق، والأمراض المؤلمة والعديد من الأمراض المعدية المزمنة.
الفيزيولوجيا المرضية ومورفولوجيا الالتهاب
في تطوره، يمر الالتهاب بثلاث مراحل، يحدد تسلسلها مسار العملية برمتها.
مرحلة التغيير
مرحلة التغيير (الضرر)- المرحلة الأولية للالتهاب، والتي تتميز بتلف الأنسجة. في هذه المرحلة، يتطور الجاذبية، أي. الانجذاب إلى موقع تلف الخلايا التي تنتج وسطاء التهابات ضروريًا لإدراجها في عملية تفاعل الأوعية الدموية.
الجاذبات الكيميائية- المواد التي تحدد اتجاه حركة الخلايا في الأنسجة. يتم إنتاجها بواسطة الميكروبات والخلايا والأنسجة وتوجد في الدم.
مباشرة بعد الضرر، يتم إطلاق الجاذبات الكيميائية مثل استريز البروسيرين والثرومبين والكينين من الأنسجة، وفي حالة تلف الأوعية الدموية، يتم إطلاق الفيبرينوجين والمكونات التكميلية المنشطة.
نتيجة للجذب الكيميائي التراكمي في منطقة الضرر، تعاون الخلية الأوليةإنتاج وسطاء التهابات - تراكم الخلايا البدينة، والخلايا المحببة القاعدية واليوزينية، والخلايا الوحيدة، وخلايا نظام APUD، وما إلى ذلك. فقط عندما تكون هذه الخلايا موجودة في موقع الضرر، توفر إطلاق وسطاء الأنسجة و بداية الالتهاب.
نتيجة لعمل وسطاء التهابات الأنسجة، تحدث العمليات التالية في المنطقة المتضررة:
- زيادة نفاذية الأوعية الدموية الدقيقة.
- تتطور التغيرات البيوكيميائية في النسيج الضام، مما يؤدي إلى احتباس الماء في الأنسجة وتورم المصفوفة خارج الخلية.
- التنشيط الأولي لوسطاء التهابات البلازما تحت تأثير العوامل الضارة ووسطاء الأنسجة.
- تطور التغيرات التصنعية والنخرية في الأنسجة في المنطقة المتضررة ؛
- تلعب هيدروليز (البروتياز، الليباز، الفسفوليباز، الإلاستاز، الكولاجيناز) والإنزيمات الأخرى المنطلقة من الليزوزومات الخلوية والتي يتم تنشيطها في موقع الالتهاب دورًا مهمًا في تطور تلف الخلايا والهياكل غير الخلوية:
- الاختلالات الوظيفية، سواء كانت محددة - في العضو الذي حدث فيه التغيير، أو غير محددة - التنظيم الحراري، أو المناعة المحلية، وما إلى ذلك.
مرحلة الإفراز
ب. تحدث مرحلة النضح في أوقات مختلفة بعد تلف الأنسجة استجابةً لعمل الوسائط الالتهابية الخلوية وخاصة البلازما التي تتشكل أثناء تنشيط نظام الكينين والجهاز التكميلي وجهاز تخثر الدم. في ديناميات مرحلة النضح، يتم التمييز بين مرحلتين: النضح البلازمي والتسلل الخلوي.
أرز. 22. الحالة الهامشية للكريات البيض المجزأة (Ls).
نضح البلازمايحدث بسبب التمدد الأولي لأوعية الأوعية الدموية الدقيقة، وزيادة تدفق الدم إلى موقع الالتهاب (النشط)، مما يؤدي إلى زيادة الضغط الهيدروستاتيكي في الأوعية. نشط يعزز تطوير الأوكسجين في موقع الالتهاب، مما يؤدي إلى العمليات التالية:
- تشكيل أنواع الأكسجين التفاعلية.
- تدفق عوامل الحماية الخلطية - المكمل، الفبرونكتين، الداين المناسب، وما إلى ذلك؛
- تدفق PMNs وحيدات والصفائح الدموية وخلايا الدم الأخرى.
تسلل الخلوية- دخول خلايا مختلفة إلى منطقة الالتهاب، وخاصة خلايا الدم، وهو ما يرتبط بتباطؤ تدفق الدم في الأوردة (السلبية) وعمل وسطاء الالتهابات.
في هذه الحالة، تتطور العمليات التالية:
- تنتقل الكريات البيض إلى محيط تدفق الدم المحوري.
- تقوم كاتيونات بلازما الدم Ca 2+ وMn وMg 2+ بإزالة الشحنة السالبة من الخلايا البطانية وتلتصق الكريات البيض والكريات البيض بجدار الوعاء الدموي (التصاق الكريات البيض)؛
- ينشأ الحالة الهامشية للكريات البيض ،أي إيقافهم عند جدار الأوعية (الشكل 22)؛

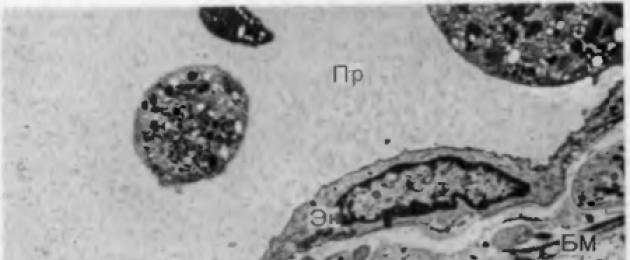
أرز. 23. هجرة كريات الدم البيضاء المجزأة من تجويف الجوف (L).
تقع الكريات البيض المجزأة (Ls) تحت الخلية البطانية (En) بالقرب من الغشاء القاعدي (BM) للسفينة.
- يمنع تدفق الإفرازات والسموم ومسببات الأمراض من مصدر الالتهاب والزيادة السريعة في التسمم وانتشار العدوى.
يتطور تجلط الدم في المنطقة الالتهابية بعد هجرة خلايا الدم إلى موقع الالتهاب.
تفاعل الخلايا في موقع الالتهاب.
- الكريات البيض متعددة النوى
عادة ما يكون أول من يصل إلى موقع الالتهاب. وظائفهم:
- تحديد مصدر الالتهاب.
- توطين وتدمير العامل الممرض ،
- خلق بيئة حمضية في موقع الالتهاب من خلال إطلاق (إخراج) الحبيبات التي تحتوي على هيدرولاز
- البلاعم،
تظهر بشكل خاص في موقع الضرر حتى قبل تطور الالتهاب. وظائفهم متنوعة للغاية. ماذا يفعل البلاعم وأحد الخلايا الرئيسية للاستجابة الالتهابية:
- يقومون ببلعمة العامل المدمر.
- تحديد الطبيعة المستضدية للعامل الممرض؛
- تحفيز ردود الفعل المناعية ومشاركة الجهاز المناعي في الالتهاب.
- توفير عصبية السموم في موقع الالتهاب.
- توفير تفاعلات متنوعة بين الخلايا، في المقام الأول مع PMNs، والخلايا الليمفاوية، وحيدات، والخلايا الليفية؛
- التفاعل مع PMNs، فإنها تضمن البلعمة للعامل المدمر؛
- يساهم تفاعل البلاعم والخلايا الليمفاوية في تطوير تفاعل فرط الحساسية المتأخر (DTH) في شكل انحلال الخلايا المناعي والورم الحبيبي.
- يهدف التفاعل بين البلاعم والخلايا الليفية إلى تحفيز تكوين الكولاجين والألياف المختلفة.
- حيدات إنها سلائف البلاعم، وتنتشر في الدم، وتدخل موقع الالتهاب، وتتحول إلى بلاعم.
- خلايا الجهاز المناعي - الخلايا اللمفاوية التائية والبائية وخلايا البلازما:
- مجموعات سكانية فرعية مختلفة من الخلايا الليمفاوية التائية تحدد نشاط الاستجابة المناعية؛
- تضمن الخلايا اللمفاوية التائية القاتلة موت العوامل البيولوجية المسببة للأمراض ولها خصائص تحلل الخلايا فيما يتعلق بخلايا الجسم نفسها؛
- وتشارك الخلايا الليمفاوية البائية وخلايا البلازما في إنتاج أجسام مضادة محددة (انظر الفصل 8)، والتي تضمن القضاء على العامل المدمر.
- الليفية هما المنتجان الرئيسيان للكولاجين والإيلاستين، اللذين يشكلان أساس النسيج الضام. تظهر بالفعل في المراحل الأولى من الالتهاب تحت تأثير السيتوكينات البلاعمية وتضمن إلى حد كبير استعادة الأنسجة التالفة.
- خلايا أخرى (الحمضات، خلايا الدم الحمراء) والتي يعتمد ظهورها على سبب الالتهاب.
تتفاعل كل هذه الخلايا، بالإضافة إلى المصفوفة خارج الخلية، ومكونات النسيج الضام مع بعضها البعض بفضل العديد من المواد الفعالة التي تحدد الاستقبال الخلوي وخارج الخلية - السيتوكينات وعوامل النمو. من خلال التفاعل مع مستقبلات الخلية والمصفوفة خارج الخلية، فإنها تنشط أو تمنع وظائف الخلايا المشاركة في الالتهاب.
نظام الأوعية الدموية الليمفاوية يشارك في الالتهاب بشكل متزامن مع قاع الدورة الدموية. مع التسلل الواضح للخلايا وتعرق بلازما الدم في منطقة الجزء الوريدي من الأوعية الدموية الدقيقة، سرعان ما تشارك جذور نظام "فائق الدورة الدموية" للأنسجة الخلالية في العملية - القنوات البينية.
ونتيجة لذلك يحدث في منطقة الالتهاب:
- انتهاك توازن أنسجة الدم.
- التغيرات في الدورة الدموية خارج الأوعية الدموية لسائل الأنسجة.
- حدوث وذمة وتورم الأنسجة.
- يتطور تضخم الغدد الليمفاوية. ونتيجة لذلك، تصبح الشعيرات الدموية اللمفاوية مملوءة باللمف. يتسرب إلى الأنسجة المحيطة ويحدث وذمة لمفية حادة.
نخر الأنسجة هو عنصر مهم في الالتهاب، حيث أن له عدة وظائف:
- في بؤرة النخر، يجب أن يموت العامل الممرض مع الأنسجة المحتضرة؛
- مع كتلة معينة من الأنسجة الميتة، تظهر المواد النشطة بيولوجيا، بما في ذلك الآليات التكاملية المختلفة لتنظيم الالتهاب، بما في ذلك متفاعلات المرحلة الحادة ونظام الخلايا الليفية.
- يعزز تنشيط الجهاز المناعي، الذي ينظم استخدام الأنسجة "الخاصة" المتغيرة.
المرحلة الإنتاجية (التكاثرية).
تنهي المرحلة الإنتاجية (التكاثرية) الالتهاب الحاد وتضمن إصلاح (ترميم) الأنسجة التالفة. خلال هذه المرحلة تحدث العمليات التالية:
- يقلل من الأنسجة الملتهبة.
- تقل شدة هجرة خلايا الدم.
- يتناقص عدد الكريات البيض في منطقة الالتهاب.
- يمتلئ بؤرة الالتهاب تدريجيًا بالبلاعم ذات الأصل الدموي، والتي تفرز الإنترلوكينات - الجاذبات الكيميائية للخلايا الليفية، بالإضافة إلى تحفيز تكوين أوعية دموية جديدة؛
- تتكاثر الخلايا الليفية في مكان الالتهاب:
- تراكم خلايا الجهاز المناعي في موقع الالتهاب - الخلايا الليمفاوية التائية والبائية وخلايا البلازما.
- تشكيل تسلل التهابي - تراكم هذه الخلايا مع انخفاض حاد في الجزء السائل من الإفرازات.
- تنشيط العمليات الابتنائية - كثافة تخليق الحمض النووي الريبي (DNA) والحمض النووي الريبي (RNA) والمواد الأساسية والهياكل الليفية للنسيج الضام:
- "تطهير" المجال الالتهابي بسبب تنشيط هيدروليز الليزوزوم للخلايا الوحيدة والبلاعم والخلايا المنسجات والخلايا الأخرى.
- تكاثر الخلايا البطانية للأوعية المحفوظة وتكوين أوعية جديدة:
- تشكيل الأنسجة الحبيبية بعد إزالة المخلفات النخرية.
الأنسجة الحبيبية - نسيج ضام غير ناضج، يتميز بتراكم خلايا الارتشاح الالتهابي والبنية الخاصة للأوعية المتكونة حديثا، تنمو عموديا إلى سطح الضرر، ثم تهبط مرة أخرى إلى الأعماق. تبدو المنطقة التي تدور فيها الأوعية الدموية وكأنها حبيبة، وهو ما يعطي الأنسجة اسمها. عندما يتم تنظيف موقع الالتهاب من الكتل النخرية، يملأ النسيج الحبيبي المنطقة المتضررة بأكملها. لديه قدرة امتصاص عالية، ولكن في نفس الوقت يمثل حاجزا أمام العوامل الالتهابية.
تنتهي العملية الالتهابية بنضوج التحبيب وتكوين النسيج الضام الناضج.
أشكال الالتهاب الحاد
يتم تحديد الأشكال السريرية والتشريحية للالتهاب من خلال هيمنة ديناميكيات النضح أو الانتشار على التفاعلات الأخرى التي تشكل الالتهاب. وعلى هذا الأساس يميزون:
- التهاب نضحي.
- التهاب منتج (أو تكاثري).
وفقا للتدفق هناك:
- التهاب حاد - لا يستمر أكثر من 4-6 أسابيع.
- التهاب مزمن - يستمر لأكثر من 6 أسابيع، وقد يصل إلى عدة أشهر وسنوات.
بواسطة خصوصية المسببة للأمراضتسليط الضوء:
- التهاب عادي (مبتذل) ؛
- الالتهاب المناعي.
التهاب نضحي
التهاب نضحيتتميز بتكوين الإفرازات، والتي يتم تحديد تكوينها بشكل رئيسي من خلال:
- سبب الالتهاب
- استجابة الجسم للعامل الضار وخصائصه؛
- يحدد الإفراز أيضًا اسم شكل الالتهاب النضحي.
1. التهاب خطيرتتميز بتكوين الإفرازات المصلية - سائل غائم يحتوي على ما يصل إلى 2-25٪ بروتين وكمية صغيرة من العناصر الخلوية - كريات الدم البيضاء والخلايا الليمفاوية والخلايا الظهارية المتقشرة.
أسباب الالتهاب المصلي هي:
- عمل العوامل الفيزيائية والكيميائية (على سبيل المثال، انفصال البشرة مع تكوين فقاعة أثناء الحرق)؛
- تأثير السموم والسموم التي تسبب نزفًا شديدًا (على سبيل المثال، بثور على الجلد أثناء مرض الجدري):
- التسمم الشديد المصحوب بفرط نشاط الجسم مما يسبب التهابًا مصليًا في سدى الأعضاء المتني - ما يسمى التهاب خلالي.
توطين الالتهابات المصلية - الأغشية المخاطية والمصلية والجلد والأنسجة الخلالية وكبيبات الكلى والمساحات المحيطة بالجيبية في الكبد.
عادة ما تكون النتيجة مواتية - حيث يتم امتصاص الإفرازات واستعادة بنية الأنسجة التالفة. وترتبط النتيجة غير المواتية بمضاعفات الالتهاب المصلي، على سبيل المثال، يمكن للإفرازات المصلية في السحايا الناعمة (التهاب السحايا النحيفة المصلي) أن تضغط على الدماغ، كما أن التغلغل المصلي للحاجز السنخي للرئتين هو أحد أسباب فشل الجهاز التنفسي الحاد. في بعض الأحيان، بعد التهاب مصلي في الأعضاء المتني، يتطور التصلب المنتشرسدى بهم.
2. الالتهاب الليفي تتميز بالتعليم الإفرازات الليفية، تحتوي، بالإضافة إلى الكريات البيض، وحيدات، الضامة، والخلايا المتحللة من الأنسجة الملتهبة، وكمية كبيرة من الفيبرينوجين، الذي يترسب في شكل جلطات الفيبرين. ولذلك، فإن محتوى البروتين في الإفرازات الليفية هو 2.5-5٪.
يمكن أن تكون أسباب الالتهاب الفبريني مجموعة متنوعة من النباتات الميكروبية: البكتيريا الوتدية السامة، الخناق، المكورات المختلفة، المتفطرة السلية، بعض الشيغيلا - العوامل المسببة للدوسنتاريا، والعوامل السامة الداخلية والخارجية، وما إلى ذلك.
توطين الالتهاب الليفي - الأغشية المخاطية والمصلية.
التشكل.
يسبق النضح نخر الأنسجة وتجمع الصفائح الدموية في موقع الالتهاب. تتخلل الإفرازات الليفية الأنسجة الميتة وتشكل طبقة رمادية فاتحة تفرز تحتها الميكروبات السموم. يتم تحديد سمك الفيلم من خلال عمق النخر، ويعتمد عمق النخر نفسه على بنية الأغطية الظهارية أو المصلية وخصائص النسيج الضام الأساسي. لذلك، اعتمادا على عمق النخر وسمك الفيلم الليفي، يتم تمييز نوعين من الالتهاب الليفي: الفصي والخناق.
التهاب كروبوسيعلى شكل فيلم ليفي رقيق يمكن إزالته بسهولة يتطور على غطاء ظهاري أحادي الطبقة من الأغشية المخاطية أو المصلية الموجودة على قاعدة نسيج ضام كثيفة ورقيقة.

أرز. 24. الالتهاب الليفي. التهاب اللوزتين الخناقي والتهاب الحنجرة الفصي والتهاب القصبات الهوائية.
بعد إزالة الغشاء الفبريني، لا يتشكل أي خلل في الأنسجة الأساسية. يتطور الالتهاب الخناقي على الغشاء المخاطي للقصبة الهوائية والشعب الهوائية، على البطانة الظهارية للحويصلات الهوائية، على سطح غشاء الجنب، الصفاق، التامور مع التهاب القصبة الهوائية الليفي والتهاب الشعب الهوائية، الالتهاب الرئوي الفصي، التهاب الصفاق، التهاب التامور، وما إلى ذلك (الشكل 24). ).
التهاب الخناق ، تتطور على الأسطح المبطنة بظهارة مسطحة أو انتقالية، بالإضافة إلى أنواع أخرى من الظهارة الموجودة على قاعدة نسيج ضام فضفاضة وواسعة. عادة ما يساهم هيكل الأنسجة هذا في تطور النخر العميق وتكوين طبقة ليفية سميكة يصعب إزالتها، وبعد إزالتها تبقى تقرحات. يتطور التهاب الخناق في البلعوم والأغشية المخاطية للمريء والمعدة والأمعاء والرحم والمهبل والمثانة وفي جروح الجلد والأغشية المخاطية.
الخروجيمكن أن يكون الالتهاب الليفي مفيدًا: في حالة الالتهاب الفصي للأغشية المخاطية، تذوب الأغشية الليفية تحت تأثير هيدرات الكريات البيض ويتم استعادة الأنسجة الأصلية في مكانها. وينتهي الالتهاب الخناقي بتكوين تقرحات، والتي يمكن أن تشفى أحيانًا بتكوين ندبات. النتيجة غير المواتية للالتهاب الليفي هي تنظيم الإفرازات الليفية، وتشكيل الالتصاقات والرسو بين طبقات التجاويف المصلية حتى طمسها، على سبيل المثال، تجويف التامور، التجاويف الجنبية.
3. التهاب قيحيتتميز بالتعليم الإفرازات قيحية ،وهي عبارة عن كتلة كريمية تتكون من مخلفات الأنسجة من موقع الالتهاب، وخلايا متغيرة التصنع، وميكروبات، وعدد كبير من خلايا الدم، الجزء الأكبر منها عبارة عن كريات الدم البيضاء الحية والميتة، بالإضافة إلى الخلايا الليمفاوية، والخلايا الوحيدة، والبلاعم، والخلايا المحببة اليوزينية في كثير من الأحيان. . محتوى البروتين في القيح هو 3-7٪. درجة حموضة القيح 5.6-6.9. القيح له رائحة محددة، لون أخضر مزرق مع ظلال مختلفة. الإفرازات القيحية لها عدد من الصفات التي تحدد الأهمية البيولوجية للالتهاب القيحي. يحتوي على إنزيمات مختلفة، بما في ذلك البروتياز، التي تحطم الهياكل الميتة، وبالتالي فإن تحلل الأنسجة مميز في موقع الالتهاب؛ يحتوي، إلى جانب الكريات البيض التي يمكنها البلعمة وقتل الميكروبات، على عوامل مختلفة للجراثيم - الغلوبولين المناعي، والمكونات التكميلية، والبروتينات، وما إلى ذلك. لذلك، يمنع القيح نمو البكتيريا ويدمرها. وبعد 8-12 ساعة تموت كريات الدم البيضاء القيحية وتتحول إلى “ أجسام قيحية".
سبب الالتهاب القيحي هي ميكروبات قيحية - المكورات العنقودية، العقديات، المكورات البنية، عصية التيفوئيد، الخ.
توطين التهاب قيحي - أي أنسجة الجسم وجميع الأعضاء.
أشكال الالتهاب القيحي.
خراج - التهاب قيحي محدود، يرافقه تكوين تجويف مملوء بالإفرازات القيحية. يقتصر التجويف على كبسولة قيحية - نسيج حبيبي، من خلال الأوعية التي تدخل الكريات البيض. في المسار المزمن للخراج، يتم تشكيل طبقتين في الغشاء القيحي: الطبقة الداخلية، التي تتكون من الأنسجة الحبيبية، والطبقة الخارجية، التي تشكلت نتيجة لنضج الأنسجة الحبيبية في النسيج الضام الناضج. ينتهي الخراج عادةً بإفراغ وإطلاق القيح على سطح الجسم، إلى الأعضاء المجوفة أو التجاويف من خلال الناسور - وهي قناة مبطنة بنسيج حبيبي أو ظهارة تربط الخراج بسطح الجسم أو تجاويفه. بعد خروج القيح، يصبح تجويف الخراج متندبًا. في بعض الأحيان، يخضع الخراج للتغليف.
فلغمون - التهاب قيحي منتشر غير محدد، حيث تتخلل الإفرازات القيحية الأنسجة وتقشرها. يتشكل الفلغمون عادة في الأنسجة الدهنية تحت الجلد، والطبقات العضلية، وما إلى ذلك. يمكن أن يكون الفلغمون ناعمًا إذا كان تحلل الأنسجة الميتة هو السائد، ويكون قاسيًا عندما يحدث نخر تجلط الدم للأنسجة في البلغم، والتي يتم رفضها تدريجيًا. في بعض الحالات، يمكن أن يتدفق القيح تحت تأثير الجاذبية إلى الأقسام الأساسية على طول أغلفة الأوتار العضلية، والحزم الوعائية العصبية، والطبقات الدهنية ويشكل ثانويًا، يسمى خراجات باردة,أو المتسربين. يمكن أن ينتشر الالتهاب البلغم إلى الأوعية الدموية، مما يسبب تجلط الدم في الشرايين والأوردة (التهاب الوريد الخثاري، التهاب الوريد الخثاري، التهاب الأوعية اللمفاوية). يبدأ شفاء البلغم بحدوده، يليه تكوين ندبة خشنة.
الدبيلة - التهاب قيحي في تجاويف الجسم أو الأعضاء المجوفة. سبب الدبيلة هو بؤر قيحية في الأعضاء المجاورة (على سبيل المثال، خراج الرئة والدبيلة في التجويف الجنبي)، وانتهاك تدفق القيح أثناء الالتهاب القيحي للأعضاء المجوفة - المرارة، الزائدة الدودية، قناة فالوب، إلخ. مع مسار طويل من الدبيلة، يحدث الطمس عضوًا مجوفًا أو تجويفًا.
جرح قيحي - شكل خاص من الالتهاب القيحي الذي يحدث إما نتيجة لتقيح الصدمة بما في ذلك الجراحة أو الجرح أو نتيجة فتح بؤرة الالتهاب القيحي في البيئة الخارجية وتشكيل سطح الجرح المغطى مع الافرازات قيحية.
4. التهاب متعفن أو متعفنيتطور عندما تدخل البكتيريا المتعفنة في بؤرة الالتهاب القيحي مع نخر الأنسجة الواضح. يحدث عادة عند المرضى الضعفاء الذين يعانون من جروح واسعة النطاق وغير قابلة للشفاء أو خراجات مزمنة. في هذه الحالة، يكتسب الإفرازات القيحية رائحة كريهة بشكل خاص من التعفن. ويهيمن نخر الأنسجة على الصورة المورفولوجية دون الميل إلى التحديد. تتحول الأنسجة النخرية إلى كتلة نتنة مصحوبة بزيادة التسمم.
5. الالتهاب النزفيهو شكل من أشكال الالتهاب المصلي أو الليفي أو القيحي ويتميز بنفاذية عالية بشكل خاص لأوعية دوران الأوعية الدقيقة ، وهبوط كريات الدم الحمراء واختلاطها بالإفرازات الموجودة (التهاب نزفي مصلي ، والتهاب نزفي قيحي). إن خليط خلايا الدم الحمراء نتيجة تحولات الهيموجلوبين يعطي الإفرازات لونًا أسود.
عادة ما يكون سبب الالتهاب النزفي تسممًا شديدًا للغاية، مصحوبًا بزيادة حادة في نفاذية الأوعية الدموية، والتي يتم ملاحظتها، على وجه الخصوص، في حالات العدوى مثل الطاعون والجمرة الخبيثة والعديد من الالتهابات الفيروسية والجدري والأشكال الحادة من الأنفلونزا، وما إلى ذلك.
عادة ما تعتمد نتيجة الالتهاب النزفي على مسبباته.
6. نزلةيتطور على الأغشية المخاطية ويتميز بمزيج من المخاط مع أي إفرازات، وبالتالي، مثل النزفية، فهو ليس شكلاً مستقلاً من الالتهابات.
يمكن أن يحدث الالتهاب النزلي بسبب حالات عدوى مختلفة. منتجات ضعف التمثيل الغذائي والمهيجات التحسسية والعوامل الحرارية والكيميائية. على سبيل المثال، مع التهاب الأنف التحسسي، يتم خلط المخاط مع الإفرازات المصلية (التهاب الأنف النزلي)، وغالبا ما يلاحظ نزلات قيحية من الغشاء المخاطي للقصبة الهوائية والشعب الهوائية (التهاب القصبة الهوائية النزلي أو التهاب الشعب الهوائية)، وما إلى ذلك.
الخروج.
يستمر الالتهاب النزلي الحاد لمدة 2-3 أسابيع، وعندما ينتهي لا يترك أي أثر. يمكن أن يؤدي الالتهاب النزلي المزمن إلى تغيرات ضامرة أو تضخمية في الغشاء المخاطي.
التهاب منتجالتهاب منتج (متكاثر).

تتميز بغلبة تكاثر العناصر الخلوية على النضح والتغيير. هناك 4 أشكال رئيسية للالتهاب المنتج: أرز. 25.
1. التيفوس الحبيبي بوبوف. تراكم المنسجات والخلايا الدبقية في موقع الوعاء المدمر.التهاب حبيبي
يمكن أن يحدث بشكل حاد ومزمن، ولكن المسار المزمن للعملية له أهمية قصوى.لوحظ، كقاعدة عامة، في الأمراض المعدية الحادة - التيفوس، حمى التيفوئيد، داء الكلب، التهاب الدماغ الوبائي، شلل الأطفال الأمامي الحاد، وما إلى ذلك (الشكل 25).
الأساس المرضيالالتهاب الحبيبي الحاد هو عادة التهاب في أوعية الدورة الدموية الدقيقة عند تعرضها للعوامل المعدية أو سمومها، والذي يصاحبه نقص تروية الأنسجة المحيطة بالأوعية الدموية.
مورفولوجيا الالتهاب الحبيبي الحاد. في الأنسجة العصبية، يتم تحديد تشكل الأورام الحبيبية عن طريق نخر مجموعة من الخلايا العصبية أو الخلايا العقدية، وكذلك نخر بؤري صغير لمادة الدماغ أو الحبل الشوكي، وتحيط به العناصر الدبقية التي تحمل وظيفة الخلايا البالعة.
في حمى التيفوئيد، يحدث تشكل الأورام الحبيبية بسبب تراكم الخلايا البلعمية المحولة من الخلايا الشبكية في بصيلات جماعية في الأمعاء الدقيقة. تتشكل هذه الخلايا الكبيرة البلعمية S. التيفية، وكذلك المخلفات في بصيلات انفرادية. الأورام الحبيبية التيفوئيدية تخضع للنخر.
يمكن أن تكون نتيجة الالتهاب الحبيبي الحاد مواتية عندما يختفي الورم الحبيبي دون أن يترك أثرا، كما هو الحال في حمى التيفوئيد، أو تبقى بعده ندبات دبقية صغيرة، كما هو الحال في التهابات الأعصاب. ترتبط النتيجة غير المواتية للالتهاب الحبيبي الحاد بشكل رئيسي بمضاعفاته - انثقاب الأمعاء في حمى التيفوئيد أو موت عدد كبير من الخلايا العصبية مع عواقب وخيمة.
2. منتشر خلالي,أو الالتهاب الخلالي موضعي في سدى الأعضاء المتني، حيث يحدث تراكم الخلايا وحيدة النواة - الخلايا الوحيدة والبلاعم والخلايا الليمفاوية. في هذه الحالة، تتطور التغيرات التصنعية والنخرية في الحمة.
يمكن أن يكون سبب الالتهاب إما عوامل معدية مختلفة، أو يمكن أن يحدث كرد فعل لللحمة المتوسطة للعضو على التأثيرات السامة أو التسمم الميكروبي. لوحظت الصورة الأكثر لفتًا للانتباه للالتهاب الخلالي في الالتهاب الرئوي الخلالي والتهاب عضلة القلب الخلالي والتهاب الكبد الخلالي والتهاب الكلية.
يمكن أن تكون نتيجة الالتهاب الخلالي مواتية عند حدوث استعادة كاملة للأنسجة الخلالية للأعضاء وغير مواتية عندما تصبح سدى العضو متصلبة، والذي يحدث عادة أثناء الالتهاب المزمن.
3. نمو مفرط التنسج (فرط التجدد).- التهاب إنتاجي في سدى الأغشية المخاطية، حيث يحدث تكاثر الخلايا اللحمية. يرافقه تراكم الحمضات والخلايا الليمفاوية وكذلك تضخم ظهارة الأغشية المخاطية. في هذه الحالة، الاورام الحميدة من أصل التهابي- التهاب الأنف السليلي، التهاب القولون السليلي، الخ.
تحدث زيادات مفرطة التنسج أيضًا على حدود الأغشية المخاطية ذات الظهارة المسطحة أو المنشورية نتيجة للتهيج المستمر لإفراز الأغشية المخاطية، على سبيل المثال، المستقيم أو الأعضاء التناسلية الأنثوية. في هذه الحالة، تتآكل الظهارة، ويحدث التهاب إنتاجي مزمن في السدى، مما يؤدي إلى تكوين الثآليل التناسلية.
الالتهاب المناعي - نوع من الالتهاب ينتج في البداية عن رد فعل الجهاز المناعي. تم تقديم هذا المفهوم بواسطة A.I. ستروكوف (1979)، الذي أظهر أن الأساس المورفولوجي للتفاعلات فرط الحساسية الفورية(الحساسية المفرطة، ظاهرة آرثوس، وما إلى ذلك)، وكذلك تأخر نوع فرط الحساسية(رد فعل السلين) هو التهاب. في هذا الصدد، فإن السبب وراء هذا الالتهاب هو تلف الأنسجة بواسطة المجمعات المناعية للأجسام المضادة للمستضد والمكونات التكميلية وعدد من الوسطاء المناعيين.
لرد فعل فرط الحساسية الفوري تتطور هذه التغييرات في تسلسل معين:
- تكوين المجمعات المناعية للأجسام المضادة في تجويف الأوردة:
- ربط هذه المجمعات بالتكملة؛
- التأثير الكيميائي للمجمعات المناعية على PMNs وتراكمها بالقرب من الأوردة والشعيرات الدموية.
- البلعمة وهضم المجمعات المناعية بواسطة الكريات البيض.
- تلف المجمعات المناعية والجسيمات الحالة للكريات البيض على جدران الأوعية الدموية، مع تطور نخر الفيبرينويد والنزيف حول الأوعية الدموية وذمة الأنسجة المحيطة.
ونتيجة لذلك، يتطور الالتهاب المناعي في المنطقة رد فعل نضحي نخري مع الإفرازات النزفية المصلية
في حالة تأخر رد الفعل التحسسي. الذي يتطور استجابة لمستضد موجود في الأنسجة، يختلف تسلسل العمليات إلى حد ما:
- تنتقل الخلايا اللمفاوية التائية والبلاعم إلى الأنسجة، وتجد المستضد وتدمره، بينما تدمر الأنسجة التي يوجد فيها المستضد؛
- في منطقة الالتهاب، يتراكم تسلل الخلايا اللمفاوية، غالبًا مع خلايا عملاقة وعدد صغير من الخلايا الليمفاوية.
- يتم التعبير بشكل ضعيف عن التغيرات في الأوعية الدموية الدقيقة.
- يحدث هذا الالتهاب المناعي كنوع منتج، غالبًا ما يكون ورمًا حبيبيًا، وأحيانًا خلاليًا، ويتميز بمسار طويل الأمد.
التهاب مزمن
التهاب مزمن- عملية مرضية تتميز باستمرار العامل المرضي، وتطور نقص المناعة فيما يتعلق بهذا، والذي يحدد تفرد التغيرات المورفولوجية في الأنسجة في منطقة الالتهاب، مسار العملية وفقا لمبدأ حلقة مفرغة، صعوبة إصلاح واستعادة التوازن.
في الأساس، الالتهاب المزمن هو مظهر من مظاهر الخلل في نظام الدفاع في الجسم بسبب الظروف المتغيرة لوجوده.
سبب الالتهاب المزمن هو، أولا وقبل كل شيء، العمل المستمر (استمرار) لعامل ضار، والذي يمكن ربطه بخصائص هذا العامل (على سبيل المثال، المقاومة ضد هيدروليز الكريات البيض) ومع عدم كفاية آليات التهاب الجسم نفسه (أمراض الكريات البيض، وتثبيط التسمم الكيميائي، وضعف أنسجة التعصيب أو المناعة الذاتية، وما إلى ذلك).
طريقة تطور المرض. إن استمرار المهيج يحفز الجهاز المناعي باستمرار، مما يؤدي إلى انهياره وظهوره في مرحلة معينة من التهاب مجموعة من العمليات المناعية المرضية، في المقام الأول ظهور وزيادة نقص المناعة، وأحيانًا أيضًا إلى المناعة الذاتية للأنسجة، وهذا المركب في حد ذاته يحدد مدة العملية الالتهابية.
يصاب المرضى باعتلال الخلايا اللمفاوية، بما في ذلك انخفاض مستوى مساعدي T ومثبطات T، وتتعطل نسبتهم، وفي نفس الوقت يزداد مستوى تكوين الأجسام المضادة، ويزداد تركيز المجمعات المناعية المنتشرة (CIC) في الدم، ويزداد المتمم. مما يؤدي إلى تلف أوعية الدورة الدموية الدقيقة وتطور التهاب الأوعية الدموية. وهذا يقلل من قدرة الجسم على التخلص من المجمعات المناعية. تتناقص أيضًا قدرة الكريات البيض على التسمم الكيميائي بسبب تراكم منتجات انهيار الخلايا والميكروبات والسموم والمجمعات المناعية في الدم، خاصة أثناء تفاقم الالتهاب.
التشكل. عادة ما تمتلئ منطقة الالتهاب المزمن بالأنسجة الحبيبية مع انخفاض عدد الشعيرات الدموية. يعتبر التهاب الأوعية الدموية المنتجة مميزًا، ومع تفاقم العملية، يكون التهاب الأوعية الدموية قيحيًا بطبيعته. يحتوي النسيج الحبيبي على بؤر نخر متعددة، وارتشاح لمفاوي، وكمية معتدلة من كريات الدم البيضاء المتعادلة، والبلاعم، والخلايا الليفية، ويحتوي أيضًا على جلوبيولين مناعي. غالبًا ما توجد الميكروبات في بؤر الالتهاب المزمن، لكن عدد كريات الدم البيضاء ونشاطها المبيد للجراثيم يظل منخفضًا. تتعطل أيضًا عمليات التجدد - حيث يوجد عدد قليل من الألياف المرنة، ويسود الكولاجين من النوع الثالث غير المستقر في النسيج الضام النامي، ويوجد القليل من الكولاجين من النوع الرابع الضروري لبناء الأغشية السفلية.
ميزة مشتركة الالتهاب المزمن هو انتهاك التدفق الدوري للعمليةفي شكل طبقات ثابتة من مرحلة إلى أخرى، في المقام الأول مراحل التغيير والنضح إلى مرحلة الانتشار. وهذا يؤدي إلى الانتكاسات المستمرة وتفاقم الالتهاب وعدم القدرة على إصلاح الأنسجة التالفة واستعادة التوازن.
مسببات العملية، وخصائص بنية ووظيفة العضو الذي يتطور فيه الالتهاب، والتفاعل وعوامل أخرى تترك بصمة على مسار وتشكل الالتهاب المزمن. ولذلك، فإن المظاهر السريرية والمورفولوجية للالتهاب المزمن متنوعة.
التهاب حبيبي مزمن يتطور في الحالات التي لا يستطيع فيها الجسم تدمير العامل الممرض، ولكن في الوقت نفسه لديه القدرة على الحد من انتشاره وتوطينه في مناطق معينة من الأعضاء والأنسجة. غالبًا ما يحدث في الأمراض المعدية مثل السل والزهري والجذام والرعام وبعض الأمراض الأخرى، والتي لها عدد من السمات السريرية والمورفولوجية والمناعية الشائعة. لذلك، يُطلق على هذا الالتهاب غالبًا اسم الالتهاب النوعي.
بناءً على المسببات، هناك 3 مجموعات من الأورام الحبيبية:
- المعدية، مثل الأورام الحبيبية في مرض السل، والزهري، وداء الشعيات، والرعام، وما إلى ذلك؛
- الأورام الحبيبية للأجسام الغريبة - النشا، التلك، الغرز، إلخ؛
- الأورام الحبيبية من أصل غير معروف، على سبيل المثال في الساركويد. اليوزيني ، حساسية ، الخ.
علم التشكل المورفولوجيا. الأورام الحبيبية عبارة عن تراكمات مدمجة من الخلايا البلعمية و/أو الخلايا الشبيهة بالظهارة، وعادةً ما تكون خلايا عملاقة متعددة النوى من نوع بيروجوف لانغانس أو نوع جسم غريب. استنادا إلى غلبة أنواع معينة من البلاعم، يتم تمييز الأورام الحبيبية البلاعم (الشكل 26) و خلية epipeluid(الشكل 27). يصاحب كلا النوعين من الأورام الحبيبية تسلل خلايا أخرى - الخلايا الليمفاوية وخلايا البلازما، وغالبًا ما تكون كريات الدم البيضاء العدلة أو اليوزينية. من المميزات أيضًا وجود الخلايا الليفية وتطور التصلب. غالبًا ما يحدث النخر الجبني في وسط الأورام الحبيبية.
يشارك الجهاز المناعي في تكوين الأورام الحبيبية المعدية المزمنة ومعظم الأورام الحبيبية ذات مسببات غير معروفة، لذلك عادة ما يكون هذا الالتهاب الحبيبي مصحوبًا بمناعة خلوية، وخاصة العلاج التعويضي بالهرمونات.

أرز. 27. العقيدات السلية (الأورام الحبيبية) في الرئتين. نخر جبني للجزء المركزي من الأورام الحبيبية (أ) ؛ على الحدود مع بؤر النخر، تكون الخلايا الظهارية (ب) وخلايا بيروجوف-لانجان العملاقة (ج) الموجودة في محيط الأورام الحبيبية عبارة عن تراكمات من الخلايا اللمفاوية.
نتائج الالتهاب الحبيبي، الذي يحدث بشكل دوري، مثل أي مرض آخر:
- ارتشاف الارتشاح الخلوي مع تكوين ندبة في موقع الارتشاح السابق؛
- تكلس الورم الحبيبي (على سبيل المثال، آفة غون في مرض السل)؛
- تطور النخر الجاف (الجبني) أو النخر الرطب مع تكوين خلل في الأنسجة - التجاويف؛
- نمو الورم الحبيبي حتى تشكيل ورم كاذب.
الالتهاب الحبيبي يكمن وراء الأمراض الحبيبية، أي: الأمراض التي يمثل فيها هذا الالتهاب الأساس البنيوي والوظيفي للمرض. ومن أمثلة الأمراض الحبيبية السل، والزهري، والجذام، والرعام، وما إلى ذلك.
وبالتالي، كل ما سبق يسمح لنا بالنظر في الالتهاب كرد فعل نموذجي وفي نفس الوقت فريد من نوعه للجسم، والذي له طبيعة تكيفية، ولكن اعتمادًا على الخصائص الفردية للمريض، فإنه يمكن أن يؤدي إلى تفاقم حالته، حتى تطور المضاعفات القاتلة. وفي هذا الصدد، فإن الالتهابات، وخاصة تلك التي تشكل أساس الأمراض المختلفة، تتطلب العلاج.