Allo stesso tempo, potrebbe effettivamente essere più elevato a causa della crescita asintomatica e lenta di questi tumori.
Localizzazione tipica dei carcinoidi: appendice, ileo e retto, stomaco e polmoni.
La classificazione dei carcinoidi si basa spesso sull'origine embrionale degli organi colpiti. Secondo questo approccio si distinguono i carcinoidi con localizzazione in derivati dell'intestino anteriore (bronchi e stomaco), medio (intestino tenue e appendice) e posteriore (retto).
Carcinoidi gastrici sono solitamente asintomatici e vengono scoperti incidentalmente. Tuttavia, i sintomi abbondanti possono essere caratteristici dei carcinoidi bronchiali: tosse, emottisi, polmonite ostruttiva, sindrome di Cushing e sindrome da carcinoide. I carcinoidi dell’intestino tenue possono causare ostruzione parziale o ischemia intestinale. I carcinoidi appendicolari sono più spesso reperti chirurgici incidentali. In presenza di metastasi si sviluppa una sindrome carcinoide.
carcinoidi rettali diagnosticati incidentalmente, sebbene possano essere accompagnati da stitichezza e sanguinamento rettale. La sindrome carcinoide si osserva raramente anche in presenza di metastasi.
Carcinoidi bronchiali rappresentano circa il 2% di tutti i tumori polmonari primitivi e si verificano più spesso all'età di 40-50 anni. La sindrome carcinoide è rara, ma la secrezione ectopica di ACTH è possibile con lo sviluppo della sindrome di Cushing. Ad un terzo dei pazienti, soprattutto fumatori, vengono diagnosticati i cosiddetti carcinoidi bronchiali atipici, caratterizzati da un decorso più aggressivo con frequenti metastasi ai linfonodi mediastinici. È indicato il trattamento chirurgico.
Carcinoidi gastrici rappresentano meno dell'1% di tutti i tumori di questa localizzazione. Sono divisi in tre gruppi.
Carcinoidi di tipo I si verificano sullo sfondo della gastrite atrofica cronica.
Carcinoidi di tipo II si presentano sullo sfondo della sindrome di Zollinger-Ellison e della secrezione ectopica di gastrina.
Carcinoidi III i tipi si verificano sporadicamente.
Carcinoidi gastrici di tipo I e II si sviluppano sullo sfondo di acloridria e ipergastrinemia, che si ritiene causino l'iperplasia delle cellule enterocromaffini e la formazione di piccoli tumori carcinoidi multipli. Questi tumori sono solitamente caratterizzati da una crescita lenta e non invasiva.
I tumori piccoli vengono solitamente rimossi per via endoscopica, i tumori grandi o ricorrenti vengono rimossi chirurgicamente. Per eliminare la fonte della secrezione di gastrina e causare la regressione del tumore, nei carcinoidi di tipo I viene eseguita l'antrumectomia. Nei pazienti con sindrome di Zollinger-Ellison, la regressione del tumore può essere indotta con gli analoghi della somatostatina.
Tra il 15 e il 25% dei carcinoidi gastrici si sviluppa sporadicamente, in assenza di ipergastrinemia. Questi tumori sono solitamente solitari, più grandi di 1 cm, inclini a un decorso aggressivo a causa della crescita invasiva e delle metastasi. Sono accompagnati da una sindrome carcinoide atipica, la cui manifestazione principale è il rossore, che si ritiene sia causato dall'istamina. Nella maggior parte dei casi, per tali carcinoidi viene eseguita la gastrectomia.
carcinoidi dell’intestino tenue costituiscono un terzo di tutti i tumori di questa localizzazione. Di solito si sviluppano tra i 50 e i 70 anni e si presentano con dolore addominale o ostruzione dell’intestino tenue. Al momento della visita dal medico, il 57% dei pazienti presenta sindrome carcinoide e metastasi epatiche. Tipicamente, i carcinoidi dell'intestino tenue sono multipli e caratterizzati da crescita endofitica. Spesso sono difficili da individuare con la TC e la fluoroscopia con bario, ma l'endoscopia con capsula può essere più efficace. La maggior parte dei carcinoidi dell'intestino tenue si trovano nell'intestino distale. La dimensione della neoplasia è un indicatore inaffidabile della prevalenza della malattia, poiché sono state descritte metastasi per tumori inferiori a 0,5 cm e spesso si osserva ischemia intestinale causata da fibrosi mesenterica. Quest'ultimo porta anche alla deformazione concentrica dell'intestino sotto forma di pieghe fisse. La resezione del tumore primario, insieme alle metastasi mesenteriche, elimina l'ostruzione intestinale e riduce significativamente il dolore, quindi il trattamento chirurgico è indicato anche in presenza di metastasi a distanza.
carcinoidi dell'appendice provengono, apparentemente, da cellule neuroendocrine subepiteliali. Questi tumori sono più comuni in giovane età e vengono diagnosticati principalmente durante l'appendicectomia. Al momento della diagnosi, circa il 95% di questi tumori ha dimensioni inferiori a 2 cm, le metastasi sono rare, quindi l'appendicectomia rimane il metodo di scelta per i carcinoidi dell'appendice piccola. I tumori più grandi di 2 cm spesso presentano metastasi regionali o a distanza ed è indicata l'emicolectomia destra. Tuttavia, negli anziani o in presenza di grave comorbilità, talvolta l'appendicectomia deve essere limitata.
carcinoidi rettali costituiscono solo il 12% di tutti i casi di questa localizzazione e si verificano all'età di 50-60 anni. Nella metà dei casi la malattia è asintomatica e la diagnosi viene posta durante la colonscopia. In altri casi, c'è dolore al retto, sanguinamento rettale, stitichezza.
I carcinoidi rettali di dimensioni inferiori a 1 cm metastatizzano raramente, quindi la loro escissione locale all'interno dei tessuti sani è efficace. La tattica per tumori più grandi di 12 cm non è così inequivocabile. L'ecografia endoscopica aiuta a determinare il grado di invasione della parete rettale: se non c'è germinazione della mucosa muscolare, è sufficiente l'escissione locale. Con tumori più grandi di 2 cm o con germinazione della mucosa muscolare è indicata una resezione anteriore bassa.
I carcinoidi sono tumori neuroendocrini caratterizzati dalla produzione, accumulo e secrezione di polipeptidi, ammine biogene e ormoni. La sindrome carcinoide comprende una varietà di manifestazioni quali diarrea, rossore (spesso al viso), ipotensione, dispnea, edema e aumento della sudorazione notturna.
Cause di carcinoide
I tumori carcinoidi originano da cellule neuroendocrine e sono classificati in base alla localizzazione.
L'incidenza dei carcinoidi è di 1-2 ogni 100.000 abitanti. I tumori dell'appendice sono i più comuni, seguiti dai tumori del retto e poi dell'ileo. Possono essere colpiti i polmoni, lo stomaco e l’intestino tenue.
Patogenesi. La sindrome carcinoide si basa sul rilascio di peptidi e ammine prodotti e accumulati dalle cellule carcinoidi. La maggior parte delle manifestazioni sono dovute alla produzione eccessiva di triptofano e dei suoi derivati (principalmente serotonina), al rilascio diretto di serotonina nel flusso sanguigno, evitando la sua degradazione nel fegato.
Diagnosi di carcinoide
I tumori carcinoidi sono caratterizzati da progressione lenta e decorso latente. Le piccole dimensioni della maggior parte dei tumori (meno di 2 cm) rendono difficile ottenere risultati utilizzando le principali metodiche diagnostiche. Se si sospetta un carcinoide, il metodo di scelta è determinare la concentrazione di acido 5-idrossiindolacetico nell'urina quotidiana e di serotonina nel plasma sanguigno. Si suggerisce una scintigrafia con octreotide. Questa tecnica consente di determinare la localizzazione di piccoli tumori, nonché di valutare la presenza di metastasi a distanza.
Se si sospettano metastasi epatiche, è indicata la TC addominale. Gli indicatori biochimici della funzionalità epatica non sono informativi e possono rientrare nei limiti normali. Le metastasi carcinoidi nel fegato sono caratterizzate da abbondante vascolarizzazione e praticamente non differiscono in densità dal tessuto normale; pertanto, potrebbero non essere rilevate alla TC con mezzo di contrasto. A questo proposito si consiglia di eseguire la TC con e senza mezzo di contrasto.
La scintigrafia marcata con octreotide è spesso utile per individuare il tumore primario e le metastasi, poiché oltre il 90% dei tumori carcinoidi neuroendocrini contiene un gran numero di recettori della somatostatina. Inoltre, il grado di assorbimento dell’octreotide marcato predice l’efficacia degli analoghi della somatostatina.
La cromogranina A è una proteina presente nelle vescicole secretorie delle cellule tumorali neuroendocrine. La sua concentrazione nel sangue riflette più accuratamente la prevalenza delle lesioni nei pazienti con carcinoidi rispetto al livello di acido 5-idrossiindolacetico nelle urine. Quando il contenuto di cromogranina è superiore a 5000 mg/ml la prognosi è sfavorevole.
Trattamento dei carcinoidi
Mostra la rimozione chirurgica del tumore e la terapia sintomatica. L'uso degli analoghi della somatostatina (sandostatina) ha aumentato l'aspettativa di vita dei pazienti. La co-somministrazione di somatostatina e interferone-α è più efficace dell'uso isolato della somatostatina.
Resezione segmentale del fegato con le metastasi, non solo può alleviare significativamente i sintomi della malattia, ma anche aumentare l'aspettativa di vita.
Trapianto di fegatoè indicato per metastasi isolate di carcinoidi nel fegato, ma il ruolo di questo metodo nel trattamento di tali pazienti non è stato studiato.
Embolizzazione delle arterie epatiche può servire come intervento palliativo quando un intervento radicale è impossibile. La durata dell'effetto terapeutico è breve: da 4 a 24 mesi. Gli effetti collaterali includono insufficienza renale, necrosi epatica, sepsi.
Distruzione o criodistruzione del catetere a radiofrequenza come metodo indipendente o in combinazione con la chirurgia può essere utilizzato come metodo di trattamento minimamente invasivo. Tuttavia, la loro efficacia, soprattutto nei pazienti con metastasi epatiche multiple, non è stata sufficientemente studiata.
Trattamento medico
- Analoghi della somatostatina. In circa il 90% dei pazienti, le manifestazioni della sindrome carcinoide vengono soppresse dall'octreotide alla dose di 150 mcg s/c 3 volte al giorno. L'octreotide a lunga durata d'azione viene somministrato alla dose di 20 mg IM una volta al mese con un aumento graduale (se necessario) della dose; per eliminare completamente i sintomi, puoi inoltre utilizzare un farmaco ad azione breve. Lanreotide ha un'efficacia simile. Entrambi i farmaci sono ben tollerati, sebbene presentino anche effetti collaterali come reazione locale nel sito di iniezione, steatorrea, iperglicemia.
- L'interferone è usato in monoterapia o in combinazione con analoghi della somatostatina. L'aggiunta di interferone aumenta l'efficacia della terapia, soprattutto nei tumori resistenti agli analoghi della somatostatina. Inoltre, nella maggior parte dei pazienti, la combinazione di questi farmaci riduce significativamente il tasso di crescita del tumore. Effetti collaterali dell'interferone: oppressione dell'ematopoiesi (soprattutto leucopoiesi), tiroidite linfocitica cronica, affaticamento, depressione.
- Chemioterapia. I risultati del trattamento dei carcinoidi con metastasi con una combinazione di streptozocina con fluorouracile, ciclofosfamide o doxorubicina sono deludenti. È stato dimostrato un leggero aumento della sopravvivenza quando si utilizza streptozocina con fluorouracile, ma l'uso di questi farmaci è limitato a causa della nefrotossicità, della soppressione dell'ematopoiesi, della nausea, del vomito e della debolezza.
- I nuovi farmaci includono analoghi radioattivi della somatostatina, inibitori del legame del fattore di crescita endoteliale ai suoi recettori, nonché anticorpi monoclinali (bevacizumab) e inibitori della tirosina chinasi (sunitinib).
S.L. Gutorov
Tenendo conto delle peculiarità delle caratteristiche morfologiche e del decorso clinico, nel concetto collettivo di "tumori neuroendocrini" si dovrebbero considerare separatamente i carcinoidi. Questa nosologia combina anche tumori piuttosto eterogenei, il che determina la necessità di diverse opzioni terapeutiche. I morfologi di solito descrivono un carcinoide tipico, un tumore neuroendocrino altamente differenziato, o un carcinoide atipico, o anaplastico, che è essenzialmente un cancro neuroendocrino, caratterizzato da atipia cellulare più pronunciata con elevata attività mitotica e presenza di focolai di necrosi. Basandosi solo su questo, è chiaro che la linea di demarcazione tra carcinoide e tumore neuroendocrino (cancro) non è ancora stata definita, il che spesso è la ragione di un trattamento inadeguato.
Negli ultimi anni si è registrato un aumento significativo dell’incidenza dei carcinoidi, le cui cause rimangono sconosciute. In generale, il carcinoide è un tumore attuale relativamente raro e piuttosto benigno. Il tumore primario nel 74% dei casi viene rilevato nel tratto gastrointestinale; più spesso nel piccolo (42%) e nel retto (27%), nello stomaco (9%).
Esistono carcinoidi superiori, medi e inferiori (terminali) in conformità con lo sviluppo di alcune parti del tubo intestinale embrionale. Quelli superiori comprendono tumori del polmone, del timo, dello stomaco, del pancreas. Questa localizzazione è caratterizzata da una bassa secrezione di serotonina, aumento della secrezione di istamina e di vari ormoni, che si manifesta clinicamente con un decorso atipico della sindrome carcinoide, spesso vengono rilevate metastasi ossee. I carcinoidi medi sono localizzati nel colon piccolo e destro, solitamente accompagnati da una sindrome carcinoide dovuta all'ipersecrezione di serotonina e di altre sostanze vasoattive. Nei carcinoidi inferiori, il tumore si trova nel colon sinistro o nel retto. Questa localizzazione non è caratterizzata dalla sindrome carcinoide, ma la frequenza di rilevamento di metastasi epatiche è molto alta.
Il tasso di sopravvivenza a cinque anni per il carcinoide è, in media, del 50-67%. La migliore sopravvivenza mediana si verifica quando il tumore è localizzato nel retto (88%), nei bronchi (74%) e nell'appendice (71%).
Tuttavia, al momento della diagnosi, circa il 13% dei pazienti presenta metastasi a distanza. In alcuni casi si osserva un decorso aggressivo del processo con resistenza primaria al trattamento. Forse questa situazione dovrebbe essere interpretata come un cancro neuroendocrino, che dovrebbe determinare ulteriori tattiche di trattamento.
Tenendo conto delle manifestazioni cliniche, delle caratteristiche del decorso e delle complicanze della malattia, si distinguono la struttura del tumore, un carcinoide funzionante e non funzionante. Il mancato funzionamento nella maggior parte dei casi è caratterizzato da una crescita lenta e poco sintomatica e dalla manifestazione della malattia da parte di una massa tumorale. Quest'ultima, a seconda della localizzazione, determina anche le prime manifestazioni cliniche (ostruzione o perforazione di un organo cavo, compressione delle strutture sottostanti, sanguinamento, polmonite perifocale ed emottisi se localizzate nei bronchi, ecc.). Di norma, la diagnosi viene stabilita dopo uno studio morfologico.
Un carcinoide funzionante produce una serie di sostanze biologicamente attive, tra cui serotonina, istamina, prostaglandine, ormone adrenocorticotropo, gastrina, calcitonina, ormoni della crescita e altri peptidi biogenici. La presenza nel sangue dell'una o dell'altra combinazione di neuropeptidi determina la clinica specifica della sindrome carcinoide. È generalmente accettato che la serotonina svolga un ruolo chiave nella clinica e nella patogenesi della sindrome carcinoide. La gravità delle manifestazioni della sindrome è direttamente correlata alla dimensione del tumore e alla presenza di metastasi (soprattutto quando sono localizzate nel fegato). Le principali manifestazioni della sindrome sono vampate di calore, diarrea, dolore addominale, broncospasmo e tremore. Caratteristico è lo sviluppo di una carenza proteica come conseguenza del consumo eccessivo di triptofano per la sintesi della serotonina.
Tra quelli funzionanti dovrebbero rientrare anche i carcinoidi con una “sindrome latente”, in cui l'aumento dei marcatori biochimici non è accompagnato da manifestazioni cliniche.
La conseguenza più pericolosa di un carcinoide funzionante sono le lesioni caratteristiche del cuore - sindrome cardiaca carcinoide (sindrome di Hedinger), che in alcuni casi ha conseguenze fatali. Il danno cardiaco nella sindrome da carcinoide viene diagnosticato in oltre il 50% dei casi. L'impatto di alte concentrazioni di sostanze biologicamente attive prodotte dal tumore sul muscolo e sul tessuto connettivo del cuore porta allo sviluppo di alterazioni fibrotiche nell'endo e nel miocardio del cuore destro, all'insufficienza delle sue valvole e alla successiva insufficienza cardiaca. Sono caratteristiche la stenosi e l'insufficienza della valvola tricuspide e della valvola polmonare. Tuttavia, la principale causa di morte nei pazienti è l’insufficienza ventricolare destra.
Va notato che il danno cardiaco si osserva nella sindrome latente nei pazienti con un aumento significativo del livello di acido 5-idrossiindolacetico (5-HIAA). La probabilità di danno cardiaco è elevata quando nelle urine vengono rilevati livelli significativamente elevati (più di 75 mg/giorno) di 5-HIAA per un lungo periodo ed è improbabile se l’escrezione giornaliera di 5-HIAA è bassa (meno di 50 mg /giorno).
Tutti i pazienti con sindrome carcinoide devono sottoporsi a un'ecocardiografia, che consentirà non solo di rilevare lo sviluppo del danno cardiaco nelle fasi iniziali, ma anche di iniziare in tempo un trattamento adeguato.
Circa la metà dei pazienti affetti da carcinoide, soprattutto in presenza della sindrome, presenta un'eccessiva formazione di tessuto fibroso con sviluppo di fibrosi intra-addominale e retroperitoneale, malattia di Peyronie, artropatie e trombosi dei vasi mesenterici. La malattia adesiva conseguente alla fibrosi intra-addominale è molto più probabile che sia la causa dell'ostruzione intestinale rispetto al tumore primario. Le complicanze della fibrosi retroperitoneale sono l'ischemia mesenterica, la stenosi adesiva degli ureteri. La fibrosi sviluppata può rendere difficile valutare oggettivamente la dimensione del tumore. Più raramente si sviluppa fibrosi polmonare. Non esistono farmaci efficaci per il trattamento di queste complicanze, quindi la somministrazione tempestiva di Octreotide, che potenzialmente riduce il tasso di fibrosi, gioca un ruolo significativo.
Una delle complicazioni potenzialmente letali di un carcinoide funzionante è una crisi carcinoide. Il quadro clinico comprende bruschi cambiamenti della pressione sanguigna, respirazione stridente, vampate di calore, confusione fino allo sviluppo del coma. La crisi può verificarsi spontaneamente, ma più spesso durante l'esecuzione di manipolazioni diagnostiche, interventi chirurgici e anestetici.
La diagnosi di carcinoide funzionante si basa sulla determinazione di marcatori biochimici specifici, che sono 5-HIAA e cromogranina A (CG-A).
Il livello di 5-HIAA nell'urina quotidiana può essere utilizzato per giudicare il livello di serotonina circolante nel sangue. Nella diagnosi del carcinoide, la sensibilità del metodo è del 73% e la specificità del 100%. Il livello di 5-HIAA è direttamente correlato alla gravità dei sintomi del carcinoide ed è un indicatore dell'efficacia del trattamento. Il rilevamento di un livello elevato di 5 HIAA in pazienti con sindrome carcinoide latente consente la prescrizione tempestiva del trattamento farmacologico e la prevenzione o l'arresto dello sviluppo di alterazioni cardiache e fibrotiche.
La determinazione del livello di 5-HIAA in tutti i pazienti con carcinoide è considerata obbligatoria. Con un decorso stabile della malattia, il livello di 5-HIAA viene determinato prima dell'inizio del trattamento, ogni 3-4 mesi durante il primo e ogni 6 mesi durante il secondo anno, con instabile, a seconda della situazione clinica. Se il paziente ha subito un'operazione radicale, è considerato sufficiente eseguire lo studio una volta all'anno.
La CG-A nel carcinoide è aumentata nell'85-100% dei casi e non dipende dallo stato funzionale del tumore. Il suo livello, di regola, è correlato alla dimensione del tumore e non è associato alla gravità dei sintomi della malattia. La sensibilità del metodo è del 63% e la specificità è del 98%. La determinazione del marcatore è particolarmente importante nei casi in cui il 5-HIAA non è espresso. Con un decorso stabile della malattia, lo studio CG-A viene eseguito ogni tre mesi durante il primo anno.
Va ricordato che l'espressione di CG-A non è specifica come quella del 5-HIAA e che un livello elevato di CG-A può essere rilevato in caso di alterazioni infiammatorie e/o insufficienza renale. Anche la gastrite di tipo A e l’uso di inibitori della pompa protonica possono influenzare l’aumento dei livelli di CG-A. Inoltre, sono possibili fluttuazioni temporanee difficili da spiegare nel livello di HCG-A.
In generale, basandosi solo sulla definizione di CG-A, l’interpretazione della situazione clinica non è competente. Per la pratica di routine, anche la disponibilità del test rappresenta un problema.
Ki-67, una proteina del nucleo cellulare espressa dalle cellule in proliferazione attiva, dovrebbe essere riferita a un altro marcatore che influenza sostanzialmente la tattica del trattamento. Viene determinato mediante esame immunoistochimico del tessuto tumorale ed è considerato un indice affidabile della proliferazione cellulare. Quando l'espressione del Ki 67 è superiore al 2%, il livello è considerato elevato e il tumore sta proliferando attivamente ed è potenzialmente sensibile alla chemioterapia. A basso livello di proliferazione (Ki 67 In definitiva, un ruolo decisivo nel determinare la tattica del trattamento è giocato da un'adeguata interpretazione morfologica del tumore, che consente di differenziare carcinoide, tumore neuroendocrino e cancro neuroendocrino; determinare il grado di differenziazione e malignità delle cellule tumorali, loro appartenenza al tipo, ecc.
L'obiettivo principale del trattamento del carcinoide è controllare i sintomi della malattia, il controllo biochimico (in particolare la serotonina), ottenere una risposta obiettiva dal tumore e preservare la qualità della vita del paziente. Ad oggi la chirurgia è l’unico metodo curativo. È stato dimostrato che nei pazienti operati radicalmente il tasso di sopravvivenza libera da recidiva a 10 anni è del 94%.
Tuttavia, a causa della prevalenza della malattia al momento della diagnosi, la frequenza degli interventi chirurgici radicali non supera il 20%. Quest'ultimo non riduce in alcun modo il ruolo guida del trattamento chirurgico.
È stato dimostrato che la resezione del tumore primitivo in caso di carcinoide dei tratti centrali del tubo intestinale, anche in presenza di metastasi ai linfonodi regionali o al fegato, migliora significativamente la sopravvivenza dei pazienti. Allo stesso tempo, posticipare la resezione del tumore primario a causa della presenza di metastasi complica l'operazione successiva.
Se la resezione non può essere radicale, dovrebbe essere eseguita a scopo palliativo. Le operazioni citoriduttive riducono il numero di recettori della serotonina, il che migliora la situazione clinica. Una meta-analisi delle resezioni citoriduttive del fegato in carcinoide ha mostrato che il 30-71% dei pazienti sopravvive a cinque anni, mentre nell'86-90% dei casi si è osservata una regressione completa delle manifestazioni della sindrome da carcinoide per un periodo da 4 a 120 mesi. Sono stati segnalati casi isolati di trapianto di fegato riuscito per carcinoide. Oltre a controllare i sintomi nella malattia disseminata, gli interventi citoriduttivi facilitano naturalmente il successivo trattamento farmacologico.
Se l'intervento chirurgico per le metastasi epatiche non è pratico, viene presa in considerazione l'embolizzazione (o chemioembolizzazione) dei vasi epatici con o senza chemioterapia. Come quest'ultimo si utilizzano 5-fluorouracile, doxorubicina, mitomicina C. L'effetto biochimico si ottiene nel 70-90% dei pazienti, il controllo dei sintomi della malattia è nel 50-75%, una riduzione significativa del tumore con un l'effetto sintomatico si ottiene nel 30-50% dei pazienti con una durata di 15-30 mesi.
Nonostante l'attrattiva del metodo, va ricordato che le complicanze sviluppate sono fatali in almeno il 7% dei casi.
Pertanto, tenendo conto dell’impatto significativo sulla sopravvivenza globale dei pazienti, la tattica chirurgica dovrebbe essere quanto più aggressiva possibile.
Attualmente, il trattamento farmacologico del carcinoide ha lo scopo di aumentare l'aspettativa di vita del paziente, ridurre la gravità delle manifestazioni della malattia, arrestare e prevenire lo sviluppo di condizioni potenzialmente letali associate alla crescita del tumore.
I primi farmaci che hanno avuto un effetto terapeutico significativo sui carcinoidi sono stati gli analoghi della somatostatina: l'octreotide e le sue forme prolungate. Il loro utilizzo controlla i sintomi della malattia nel 65-85% dei pazienti, riduce il rischio di sviluppare crisi carcinoidi, fibrosi specifica e altre complicanze.
L'introduzione di Octreotide riduce il tasso di crescita del tumore, soprattutto in caso di uso prolungato di dosi elevate. Pertanto, l'introduzione di Octreotide 500 mcg tre volte al giorno nel 43% dei pazienti ha portato alla stabilizzazione della malattia entro un anno.
L’octreotide è attualmente il farmaco di prima linea per la sindrome carcinoide. Nei pazienti affetti da insuloma e gastrinoma può essere utilizzato con successo anche nella seconda e terza linea di trattamento farmacologico. Inoltre, il suo utilizzo è indicato in pazienti affetti da carcinoide non funzionante durante la progressione della malattia. Per prevenire una crisi carcinoide, è necessario prescriverlo prima dell'intervento chirurgico o diagnostico.
In generale, l’efficacia della terapia con analoghi della somatostatina non può essere considerata soddisfacente. I dati riassunti di 14 studi che includevano 400 pazienti hanno mostrato una bassa efficacia diretta dell'octreotide: l'effetto oggettivo non ha superato il 9%, la risposta biochimica ha raggiunto il 37%. L'effetto migliore è stato quello di ridurre la gravità dei sintomi della malattia: diarrea e vampate di calore nel 71% dei pazienti (citato in ).
In caso di scarsa tollerabilità dell'octreotide, vengono prescritti i suoi analoghi prolungati, che hanno la stessa efficacia: octreotide-depot o sandostatina LAR, che è più comune in Russia, o lanreotide ogni 10-14 giorni in Europa.
In media, la frequenza dell'effetto biochimico del lanreotide raggiunge il 42% e l'effetto oggettivo è di circa il 9%. Rispetto all'octreotide, il lanreotide porta un po' più spesso alla stabilizzazione del tumore (46% contro 81%) e allo stesso modo (75% contro 80%) riduce la gravità della sindrome carcinoide: diarrea e vampate di calore.
I preparativi ad azione "breve" e prolungata non hanno resistenza incrociata e si sostituiscono con successo l'uno con l'altro. È stato inoltre dimostrato che la resistenza del tumore all'octreotide non determina resistenza ad altri tipi di trattamento farmacologico.
Lo sviluppo della resistenza agli analoghi della somatostatina si osserva, di regola, entro 12 mesi di trattamento. Forse questo effetto può essere superato sostituendolo con forme prolungate.
Per le cure di emergenza, l'octreotide viene prescritto 150 mcg 3 volte al giorno, per via sottocutanea. Con una buona tolleranza e la presenza di un effetto terapeutico, il farmaco viene somministrato per 3-7 giorni, quindi 20-30 mg (fino a 60 mg) del farmaco ad azione prolungata - una volta al mese.
L'esecuzione di un intervento chirurgico o di embolizzazione durante la terapia con una forma prolungata di Octreotide richiede l'introduzione di una dose aggiuntiva del farmaco una o due ore prima dell'intervento. In caso di situazione chirurgica di emergenza, una o due ore prima dell'intervento, viene somministrato per via sottocutanea un bolo di Octreotide 500-1000 mcg o 500 mcg, seguito (durante l'intervento) da un'infusione endovenosa di 50-200 mg/h.
Durante la rimozione di un tumore nella cavità addominale, l'esecuzione di una colecistectomia profilattica riduce il rischio di complicanze delle vie biliari con successivo utilizzo di analoghi della somatostatina.
In generale i farmaci sono ben tollerati. Gli effetti collaterali includono nausea, convulsioni, steatorrea, aritmie cardiache, disturbi endocrini e atonia gastrica. La formazione di calcoli nella cistifellea e un aumento della densità della bile si osservano in oltre il 50% dei casi, ma lo sviluppo di situazioni che richiedono un trattamento chirurgico non supera il 3%.
Data la significativa riduzione del rischio di sviluppare fibrosi specifica, l'octreotide deve essere prescritto a tutti i pazienti il cui contenuto giornaliero di 5-HIAA nelle urine supera i 50 mg.
Tipicamente, gli analoghi della somatostatina "ad azione breve" vengono somministrati ogni 6-12 ore: Octreotide (Sandostatina) 100-150 mcg 3 volte al giorno. Le forme ad azione prolungata (Octreotide-depot o Sandostatina-LAR) vengono utilizzate alla dose di 10-30 mg (fino a 60 mg) ogni 3-4 settimane.
Il regime standard è il seguente: durante le prime due settimane, l'octreotide viene somministrato alla dose di 100 mcg 3 volte al giorno. Con una tolleranza soddisfacente (e la presenza di un effetto), viene somministrato Octreotide-depot o Sandostatina-LAR 20 mg e l'octreotide viene continuato alla stessa dose nelle due settimane successive. Se l'effetto persiste, l'octreotide viene annullato e si continua il trattamento con una forma prolungata.
È necessario menzionare un nuovo metodo di trattamento con Octreotide radioattivo (111 In octreotide), che viene catturato selettivamente dalla cellula tumorale e ne sopprime l'attività proliferativa. Tale selettività consente di attribuire questo metodo a una terapia mirata o mirata. Vengono forniti i dati sulla sopravvivenza a cinque anni del 50% in 400 pazienti che hanno ricevuto Octreotide radioattivo. Lo svantaggio del metodo è la sua scarsa disponibilità. Attualmente, la società nazionale CJSC Pharm-sintez sta conducendo ricerche scientifiche sul rilascio dell'octreotide radioattivo (octreotide 111 In) sul mercato farmaceutico con il nome commerciale Octreotide-DTPA.
Un altro gruppo di farmaci che hanno efficacia clinica nei carcinoidi sono gli interferoni. A differenza dell'octreotide, gli interferoni inducono un po' più spesso un effetto antitumorale oggettivo, che si ottiene in circa il 15% dei casi. Allo stesso tempo, l'effetto sintomatico del trattamento si osserva nel 40-60% dei casi, biochimico - nel 30-60%, stabilizzazione della crescita del tumore (per un periodo superiore a 36 mesi) - nel 40-60% dei casi pazienti. La sopravvivenza mediana con interferone è di circa 20 mesi.
L'interferone alfa è indicato nel trattamento di prima linea per la bassa attività proliferativa dei carcinoidi delle sezioni centrali del tubo intestinale. Inoltre, ci sono segnalazioni di un'efficacia del 77% dell'interferone in seconda linea con l'inefficacia della chemioterapia citostatica.
Se usati insieme, gli analoghi della somatostatina e l'interferone hanno un effetto additivo e possibilmente un sinergismo. È stato dimostrato che l'interferone stimola l'espressione dei recettori della somatostatina, aumentando la probabilità di un effetto terapeutico dell'octreotide. Gli analoghi della somatostatina, a loro volta, riducono l'incidenza degli effetti collaterali dell'interferone alfa.
Tuttavia, un numero esiguo di studi e risultati piuttosto contrastanti non ci consentono di raccomandare l’uso combinato di farmaci nella pratica quotidiana. Forse la combinazione è appropriata per i tumori con bassa attività proliferativa con un carcinoide funzionante. La nomina standard accettata dell'interferone alfa alla dose di 3-5 UI da 3 a 5 volte a settimana. Dosi più elevate non hanno portato ad un aumento dell’efficacia.
Data la comodità per il paziente, sembra promettente l'utilizzo di forme pegelate di interferone (di solito 75-150 mg a settimana), da sole o in combinazione con forme prolungate di octreotide e/o derivati orali del 5-fluorouracile. Data l'assenza di resistenza crociata con gli analoghi della somatostatina, l'interferone è il farmaco di scelta nella seconda linea di terapia farmacologica.
Ad oggi non esiste consenso sul ruolo della chemioterapia nel trattamento dei carcinoidi. Di solito, la chemioterapia viene prescritta per un'elevata attività proliferativa (Ki 67 > 5-10%). La chemioterapia in prima linea nel trattamento conservativo migliora la prognosi ed è indicata per i carcinoidi del tubo intestinale superiore - timo, bronchi, stomaco e pancreas, se il Ki 67 supera il 10%. Nei carcinoidi del tratto centrale del tubo intestinale, invece, gli effetti terapeutici della chemioterapia sono trascurabili.
Nonostante il successo dell'introduzione di una nuova generazione di farmaci chemioterapici nella pratica oncologica, non ci sono cambiamenti significativi nella chemioterapia dei carcinoidi. La streptozotocina mantiene la sua posizione, che ha un effetto terapeutico se usata indipendentemente fino al 46%; doxorubicina, efficace nel 20% dei casi.
In generale, la chemioterapia monocomponente ha un'attività minima con una risposta obiettiva immediata inferiore al 30%.
La combinazione di streptozotocina e doxorubicina consente di ottenere un effetto oggettivo nel 69% dei casi, con 5-fluorouracile nel 45%.
Nei tumori del pancreas, l'efficacia della combinazione di streptozotocina, 5-fluorouracile e doxorubicina supera il 50%. Con la localizzazione del tumore primario nel polmone, nel retto e nel colon e nel classico carcinoide medio, questa combinazione è inattiva.
Nei carcinoidi scarsamente differenziati del tratto superiore dell'intestino (polmone, timo) e nelle forme a piccole cellule dei tumori neuroendocrini del colon e del retto ad elevata attività proliferativa (Ki 67 > 15%), la chemioterapia viene effettuata secondo regimi efficaci nei tumori a piccole cellule cancro ai polmoni. Buoni risultati terapeutici si ottengono con l'uso combinato di cisplatino (paraplatino) e Vepezid. L'introduzione di cisplatino alla dose di 75-100 mg/m2 il primo giorno e di Vepezid alla dose di 100-120 mg/m2 dal primo al quinto giorno di ogni ciclo di tre settimane è efficace nel 67% dei casi . Tuttavia, nonostante la frequenza degli effetti oggettivi, l’elevata aggressività di questi tumori predetermina una prognosi sfavorevole: un tasso di sopravvivenza a due anni è inferiore al 20%.
È anche possibile valutare la probabilità di ottenere un effetto terapeutico della chemioterapia sulla base dei risultati della determinazione dei radioisotopi dei recettori della somatostatina. È stato dimostrato che con un alto livello di accumulo del farmaco, l'efficacia della chemioterapia non supera il 10% e con valori negativi - 70%. Queste combinazioni sono basilari e consigliate per la pratica quotidiana.
Attualmente vengono studiati attivamente regimi che includono irinotecan, farmaci di un gruppo mirato, tra cui imatinib, farmaci antiangiogenici, inibitori della tirosina chinasi, ecc .. I risultati di questi studi clinici sono attesi nel prossimo futuro.
Per valutare l'effetto del trattamento dei carcinoidi, è necessario utilizzare un approccio integrato con lo studio dei marcatori tumorali, della secrezione ormonale, della dinamica dei sintomi associati al tumore e della valutazione della funzione degli organi coinvolti nel processo tumorale. L'utilizzo delle sole metodiche radiodiagnostiche non è sufficiente, poiché lo sviluppo della fibrosi può rendere difficile l'interpretazione dei dati.
Pertanto, la scelta di tattiche razionali per il trattamento farmacologico del carcinoide si basa principalmente sui moderni metodi di diagnosi morfologica del tumore e sulla determinazione dei suoi marcatori. L'applicazione tempestiva dei moderni metodi chirurgici e della terapia farmacologica può aumentare significativamente la durata e la qualità della vita dei pazienti.
Letteratura
1. Modlin IM, Lye KD, Kidd M. Un'analisi di 5 decadi di 13.715 tumori carcinoidi // Cancro. 2003;97:934-959.
2. Barakat M.T., Meeran K., Bloom S.R. Tumori neuroendocrini // Endocrino. Relativo. cancro. 2004 vol. 11. P. 1-18.
3. Kaltsas, G. A., Besser, G. M., Grossman, A. B. (2004). La diagnosi e la gestione medica dei tumori neuroendocrini avanzati. Endocr Ap 25: 458-511.
4. Kulke M.H. Tumori neuroendocrini: presentazione clinica e gestione della malattia localizzata // Cancer Treat. Rev. 2003 vol. 29. P. 363-370.
5. Modlin IM, Shapiro MD, Kidd M. Tumori carcinoidi e fibrosi: una relazione con poca spiegazione // Am J Gastroenterol 2004;99:1-13.
6. Norton J.A., Fraker D.L., Alexander H.R. et al. Intervento chirurgico per la cura della sindrome di Zollinger-Ellison // New Engl. J.Med. 1999 vol. 341. P. 635.
7. Modlin IM, Kidd M, Latich I. Stato attuale dei carcinoidi gastrointestinali // Gastroenterol-ogy. 2005;128:1717-1751.
8. Plockinger U, Rindi G, Arnold R, et al. Linee guida per la diagnosi e il trattamento dei tumori gastrointestinali neuroendocrini // Neuroendocrinology.2005;80:394-424.
9. Sarmiento JM, Heywood G, Rubin J, et al. Trattamento chirurgico delle metastasi neuroendocrine al fegato: un appello alla resezione per aumentare la sopravvivenza // J Am Coll Surg. 2003;197:29-37.
10. Jamil A, Taylor-Robinson S, Millson C, et al. Trapianto di fegato ortotopico per il trattamento dei tumori neuroendocrini metastatici – analisi di tutti i pazienti del Regno Unito. Gut 2001;49.
11. Drougas JG, Anthony LB, Blair TK et al. Chemioembolizzazione dell'arteria epatica per la gestione di pazienti con tumori carcinoidi metastatici avanzati // Am J Surg. 1998;175:408-412.
12. Saltz L., Trochanowski B., Buckley M. et al. Octreotide come agente antineoplastico nel trattamento dei tumori neuroendocrini funzionali e non funzionali // Cancro. 1993 vol. 72. R. 244-248.
13. Bajetta E., Carnagi C., Ferrari L. et al. Il ruolo degli analoghi della somatostatina nel trattamento dei tumori endocrini gastroenteropancreatici // Digest. 1996 vol. 57 (Suppl. 1). R.72-77.
14. Erikkson B., Renstrup J., Iman H. et al. Trattamento ad alte dosi con lanreotide di pazienti con tumori gastrointestinali neuroendocrini avanzati: effetti clinici e biologici // Ann. oncol. 1997 vol. 8. R. 1041-1044.
15. O'Toole D., Ducreux M., Bommelaer G. et al. Trattamento della sindrome carcinoide: una valutazione prospettica crossover di lanreotide rispetto a octreotide in termini di efficacia, accettabilità del paziente e tolleranza // Cancro. 2000 vol. 88(4). R.770-776.
16. Faiss S., Rath U., Mansmann U. et al. Trattamento con lanreotide a dosi ultra elevate in pazienti con tumori gastroenteropancreatici neuroendocrini metastatici // Digest. 1999 vol. 60. R. 469-476.
17 Bassi C, Falconi M, Lombardi D, et al. Profilassi delle complicanze dopo intervento chirurgico al pancreas: risultati di uno studio multicentrico in Italia. Gruppo di studio italiano. Digestione 1994; 55(suppl 1):41-47.
18. Sarmiento JM, Que FG. Chirurgia epatica per metastasi da tumori neuroendocrini // Surg Oncol Clin N Am 2003;12:231-42.
19. Lamberts SW, van der Lely AJ, Hofland LJ. Nuovi analoghi della somatostatina: manterranno le vecchie promesse? // Eur J Endocrinolo. 2002;146:701-705.
20. Krenning E. Radioterapia in NET. Una conferenza educativa della Rete europea dei tumori neuroendocrini "Stato attuale della diagnosi e del trattamento dei tumori neuroendocrini ereditari e sporadici del sistema gastroenteropancreatico", 2004.
21. Kaltsas G., Rockall A., Papadogias D. et al. Recenti progressi nell'imaging radiologico e con radionuclidi e nella terapia dei tumori neuroendocrini // Europ. J. Endocrinolo. 2004 vol. 151. P. 5-27.
22. Oberg K. Interferon nella gestione dei tumori GEP neuroendocrini // Digest. 2000 vol. 62 (Suppl. 1). R.92-97.
23 Bajetta E, Zilembo N, Di Bartolomeo M, et al. Trattamento dei carcinoidi metastatici e di altri tumori neuroendocrini con interferone alfa-2a ricombinante: uno studio dell'Italian Trials in Medical Oncology Group. // Cancro. 1993;72:3099-3105.
24. Eriksson V., Oberg K. Terapia con interferone dei tumori pancreatici endocrini maligni // Tumori endocrini del pancreas: Recent Advanced in Research and Management, 1995. P. 451-460.
25. Oberg K. Chemioterapia e bioterapia nel trattamento dei tumori neuroendocrini, Ann. oncol. 2001 vol. 12 (Suppl. 2). R.111-114.
26. Creutzfeldt W, Bartsch HH, Jacubaschke U, et al. Trattamento dei tumori endocrini gastrointestinali con interferone alfa e octreotide // Acta Oncol. 1991; 30:529-535.
27. Jensen R.T. e Doherty J.M. Tumori carcinoidi e sindrome carcinoide // Cancro: principi e pratica dell'oncologia su CD_ROM._6 edizione. 2000. Capitolo 38.6.
28. Wiedenmann B, Pape UF. Dalla ricerca di base a quella clinica nella malattia tumorale neuroendocrina gastroenteropancreatica – La prospettiva del medico-scienziato // Neuroendocrinologia. 2004;80(suppl 1):94-98.
29. Kvols L.K., Buck M. Chemioterapia dei carcinoidi metastatici e dei tumori delle cellule insulari: una revisione // Amer. J.Med. 1987 vol. 82. R.77.
30. Moertel C.G., Lavin P.T., Hahn R.G. Studio di fase II sulla doxorubicina per il carcinoma avanzato delle cellule insulari // Cancro. trattare. Rappresentante. 1982 vol. 66.R.1567.
31. Moertel C.G., Lefkopoulo M., Lipsitz S. et al. Streptozotocin_doxorubicina, streptozoto-cin_fluorouracile o clorozotocina nel trattamento del carcinoma avanzato delle cellule insulari // New Engl. J.Med. 1992 vol. 326. R.519.
32. Moertel CG, Kvols LK, O'Connell MJ, et al. Trattamento dei carcinomi neuroendocrini con etoposide e cisplatino combinati. Evidenza di una maggiore attività terapeutica nelle varianti anaplastiche di queste neoplasie // Cancer 1991;68:227-32.
carcinoide [gr. cancro karkinos (animale), ulcera cancerosa + specie eidos; sinonimo: argentaffinoma, tumore carcinoide, neurocarcinoma] - un tumore strutturalmente somigliante al cancro, in alcuni casi con attività biologica; appartiene al gruppo apudom. Il termine "carcinoide" fu proposto per la prima volta da S. Oberndorfer nel 1907 per riferirsi a tumori benigni dell'intestino tenue che somigliano al carcinoma. Successivamente si è scoperto che questi tumori, procedendo in modo relativamente benigno, hanno la capacità di metastatizzare e spesso portano a gravi complicazioni.
Questo tipo di tumore è più spesso localizzato nel retto distale. I carcinoidi rettali non superano 1 cm di diametro e non sono ormonalmente attivi. I carcinoidi più grandi sono spesso maligni nel loro decorso. Una caratteristica del carcinoide è la crescita lenta (il tumore è rimasto in uno stato latente per molto tempo). Le metastasi compaiono nelle fasi avanzate della malattia. Le metastasi tumorali si verificano in circa il 40% dei casi.
Clinicamente assegnare il cosiddetto carcinoide non funzionante e funzionante (con sindrome da carcinoide). Carcinoide non funzionante, può rimanere asintomatico per lungo tempo. Solo nelle fasi successive può comparire dolore, svilupparsi, a seconda della posizione del processo patologico, ostruzione intestinale, peritonite, sanguinamento, atelettasia polmonare. La sindrome carcinoide si verifica in circa il 25% dei pazienti, solitamente nei casi in cui sono presenti metastasi. È causato dal rilascio di sostanze biologicamente attive da parte delle cellule tumorali: serotonina, istamina, chinina. La sindrome carcinoide si manifesta con vampate di calore sotto forma di iperemia diffusa o irregolare della pelle del viso e della metà superiore del corpo, accompagnata da una sensazione di calore, talvolta tachicardia e calo della pressione sanguigna. Tali attacchi vasomotori si verificano spontaneamente o in connessione con l'assunzione di alcol, cibo, situazioni stressanti. Sono di breve durata o durano diversi giorni, possono manifestarsi con dolore spastico all'addome, diarrea, mancanza di respiro, agitazione psicomotoria. Con un lungo decorso del processo, nei pazienti compaiono telangiectasia e pigmentazione della pelle, si osservano danni all'endocardio delle valvole cardiache (tronco tricuspide e polmonare), broncospasmo ed ecterite.
Diagnosi di carcinoide particolarmente alle piccole dimensioni di un tumore, è difficile. Un carcinoide in stadio iniziale non funzionante è molto spesso un reperto accidentale durante un esame o un intervento chirurgico; nei casi di vasta portata, la diagnosi, come con altri tumori, si basa sui dati del quadro clinico, sugli studi di laboratorio e strumentali.
Il trattamento è chirurgico nello stesso volume di un tumore canceroso. Con una dimensione tumorale significativa e anche la presenza di metastasi estese, si raccomanda di rimuovere il focus primario e (se possibile) i nodi metastatici, il che consente di ridurre le manifestazioni cliniche. I farmaci chemioterapici solitamente non sono efficaci. La prognosi in assenza di metastasi è relativamente favorevole.
Tumori maligni non epiteliali del retto.
I tumori maligni del retto di natura mesenchimale negli stadi successivi non differiscono nel quadro clinico dal cancro del retto (vedi cancro del retto). Nelle fasi iniziali, di solito sono asintomatiche e sono reperti occasionali. Una caratteristica di tutti i tumori mesenchimali del retto è la crescita sottomucosa. Nei casi avanzati, sopra il tumore si verifica un'ulcerazione della mucosa rettale. Nelle fasi iniziali non si osserva danno alla mucosa. La diagnosi differenziale è difficile. È auspicabile la diagnostica morfologica nella fase preoperatoria. La natura maligna della crescita del tumore, di regola, viene stabilita dopo la sua rimozione totale e l'esame morfoistochimico. Il volume dell'operazione è lo stesso del cancro del retto. Dopo l'esame istologico del tumore asportato, in alcuni casi (GIST - tumori, leiosarcoma), il trattamento può essere integrato con la chemioterapia. La prognosi dei tumori mesenchimali maligni del retto dipende dallo stadio.
Tumori maligni della giunzione rettosigmoidea - C 19.
Secondo la classificazione internazionale secondo la struttura morfologica, i tumori maligni della giunzione rettosigmoidea sono uguali ai tumori del retto. (Vedi retto.)
I sintomi primari dei tumori del rettosigmoideo non sono diversi dai sintomi dei tumori del retto. Con le forme avanzate di cancro, i sintomi dell'ostruzione intestinale aumentano rapidamente. (vedi clinica per il cancro del retto). Il complesso delle misure diagnostiche, la classificazione clinica dei tumori, non differisce da quella del cancro del retto. vedere diagnosi e classificazione del cancro del retto. I principi di trattamento, prognosi e prevenzione delle neoplasie maligne della giunzione rettosigmoidea sono gli stessi delle neoplasie maligne dell'ampolla superiore del retto.
Tumori carcinoidi hanno un'origine neuroendocrina e sono i tumori endocrini più comuni del tratto gastrointestinale, tenendo conto< 1% от всех опухолей ЖКТ. гетерогенны по своим биологическим и морфологическим особенностям, часто обладают мультицентрическим ростом и потенциалом к метастазированию (печень, легкие, кости и т.д.), который зависит от размера опухоли.
Secondo moderno nomenclatura tumori carcinoidi sono neoplasie neuroendocrine. In precedenza, in connessione con l'origine dalle cellule neuroectodermiche e il meccanismo biochimico generale di cattura del precursore delle ammine (5-idrotriptofano), la sua decarbossilazione e la formazione di numerose ammine biologicamente attive (serotonina, bradichinina, istamina, peptide intestinale vasoattivo, ACTH , prostaglandine, sostanza P, ecc.) e.) erano chiamati APUDoms.
Circolante serotonina e altri peptidi attivi vengono metabolizzati di primo passaggio dal fegato (ad esempio la serotonina => metabolita dell'acido 5-idrossiindolacetico nelle urine), quindi la sindrome carcinoide di solito si presenta con metastasi epatiche o di altri organi.
Manifestazioni tumori variano a seconda della localizzazione. La definizione di malignità non si basa sul quadro istologico, ma sulla presenza di metastasi. Caratteristiche della crescita: progressione lenta con lo sviluppo di metastasi dopo 7-14 anni; il potenziale metastatico dipende dalla profondità dell’invasione e dalle dimensioni:
Meno di 1 cm: probabilità bassa.
1-2 cm: il comportamento del tumore non è chiaro (metastasi<3 % случаев).
Più di 2 cm: alta probabilità di metastasi (30-60%).
UN) Epidemiologia:
Prevalenza: negli Stati Uniti - 50.000 casi; l'incidenza negli Stati Uniti è stimata in 1,5-5,5 nuovi casi ogni 100.000 abitanti. Tra i malati si registra una leggera prevalenza delle donne, il picco di incidenza si verifica a 50-70 anni. I tumori carcinoidi rappresentano il 12-35% di tutti i tumori dell'intestino tenue e il 15-45% di tutti i tumori maligni dell'intestino tenue.
La distribuzione dei carcinoidi nel tratto gastrointestinale (attenzione: ci sono differenze tra manifestazioni cliniche e dati autoptici!): intestino tenue - 40-45% (ileo >> magro >> duodeno), retto - 12-20%, appendice - 15 -20%, intestino crasso - 7-10%, stomaco - 5-10%. Dati retrospettivi: appendice - 40% > retto - 12-15% > intestino tenue - 10-14%. Crescita multicentrica: ileo - 25-30% dei casi, intestino crasso - 3-5%.
B) Sintomi di carcinoide:
Precoce (più comune): reperti asintomatici accidentali durante la colonscopia o l'intervento chirurgico per altre malattie addominali.
Di medie dimensioni: dolore addominale vago e intermittente (ostruzione parziale/intermittente, ischemia intestinale dopo aver mangiato).
Metastasi:
- Sindrome carcinoide (< 10% среди органов, производных средней эмбриональной кишки): гиперемия (80-85%), гиперкинезия ЖКТ с поносами (около 70%), карциноидная болезнь сердца (30-40%, правые отделы сердца), бронхообструкция/хрипы (15-20%), миопатия (5-10%), пеллагроподобные изменения кожи (5%), потеря веса, артралгия, пептические язвы.
- Fibrosi peritumorale => ostruzione intestinale nel 50-75% dei casi.
Sintomi associati: tumori associati nella sindrome da neoplasie endocrine multiple di tipo I (MEN-I) - carcinoidi di organi derivati dall'intestino fetale anteriore.
b - passaggio del bario nell'intestino tenue. Tumore carcinoide al centro dell'ileo.
Si vede un polipo di 6 mm su una base ampia con una superficie liscia (indicata da una freccia) in combinazione con un restringimento focale del lume intestinale.
Questa piccola lesione presenta metastasi microscopiche ai linfonodi mesenterici.
c - sindrome carcinoide (tomogramma computerizzato). Nel mesentere dell'intestino tenue è stata trovata una massa di due centimetri con un centro calcificato (indicato da una freccia).
Bande spesse si irradiano dall'intestino tenue ad esso: infiltrazione tumorale di fasci vascolari con alterazioni intravascolari
d - passaggio del bario nell'intestino tenue. tumore carcinoide. Le pieghe di molte anse dell'intestino tenue sono fissate verso il centro del suo mesentere, le anse intestinali sono dilatate focalmente
V) Diagnosi differenziale:
IBS o spasmi.
Tumori non carcinoidi del tratto gastrointestinale: cancro del colon, cancro dell'intestino tenue (prossimale > distale), stomaco/pancreas, organi genitali femminili, carcinomatosi, GIST, linfoma, melanoma (pigmentato, senza pigmento), mesotelioma, ecc.
Tumori benigni: lipomi, leiomiomi, ecc.
G) Patomorfologia del carcinoide
Esame macroscopico di un carcinoide:
Nodulo/rigonfiamento sottomucoso o polipo (sessili/peduncolato) da grigio giallastro a marrone rosato; con aumento delle dimensioni => ulcerazione, forma anulare, ostruzione intestinale, fibrosi peritoneale/mesenterica.
Prevalenza del tumore al momento della scoperta: localmente avanzato/presenza di metastasi nel 3-5% dei casi di carcinoidi rettali, 13-38% di carcinoidi di organi derivati dall'intestino medio fetale => fegato, peritoneo, omento, polmoni, ossa, coinvolgimento dei linfonodi (80%), tumori satelliti simultanei > 25-30%.
Cambiamenti secondari: cardiopatia carcinoide (fibrosi a placche dell'endocardio e ispessimento delle valvole del cuore destro).
Tumori associati: cancro del colon nel 2-5% dei casi con carcinoide del colon e nel 30-60% con carcinoide dell'ileo; altri tumori associati: linfoma, cancro al seno.
Esame microscopico di un carcinoide:
Grappoli nidificati sottomucosi di cellule rotonde/poligonali con nucleoli prominenti e granuli eosinofili nel citoplasma.
Cinque varianti istologiche: insulare, trabecolare, ghiandolare, indifferenziata, mista.
Immunoistochimica. Positivi alla cromogranina A (CgA) e alla sinaptofisina, inoltre:
Carcinoidi di organi derivati dall'intestino embrionale anteriore: non-argent-taffin, argirofili, producono 5-idrotriptofano.
Carcinoidi di organi derivati dall'intestino medio-embrionale (dal duodeno alla metà del colon trasverso): argentaffini, argirofili, spesso multicentrici, producono numerose sostanze vasoattive -> sindrome carcinoide.
Carcinoidi di organi derivati dall'intestino posteriore (dal colon trasverso distale al retto): raramente argentafini o argirofili, solitamente solitari; la sindrome da carcinoide si sviluppa in meno del 5% dei casi di carcinoidi del colon e quasi mai nel retto (non produce serotonina).
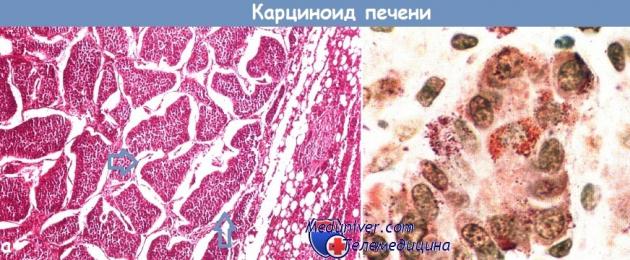
 Campione istologico di carcinoide epatico metastatico (a). Sono visibili tipiche isole di forma regolare. Colorazione ematossilina-eosina (x 150).
Campione istologico di carcinoide epatico metastatico (a). Sono visibili tipiche isole di forma regolare. Colorazione ematossilina-eosina (x 150). Dopo il trattamento con un reagente diazo alcalino, ad un ingrandimento maggiore, sono visibili granuli neurosecretori rosso-marroni (b) (x 480).
Frecce: isole di metastasi carcinoidi.
e) Esame per carcinoide
Standard minimo richiesto:
- Per sintomi sospetti => test di screening:
Cromogranina A (plasma): positiva nel 75-90% dei casi di carcinoidi di organi derivati dall'intestino anteriore, medio e posteriore.
Livello 5-HIAA (campione di urina casuale o urina raccolta entro 24 ore): positivo nel 70-85% dei casi di carcinoidi di organi derivati dall'intestino anteriore, medio, ma negativo nei carcinoidi di organi derivati dall'intestino posteriore.
Test di screening positivo, biopsia, dati di imaging medico:
Endoscopia: intestino tenue - endoscopia con capsula; colon - colonscopia; retto - colonscopia ed ecografia endorettale.
Metodi di imaging delle radiazioni:
TC/RM: metastasi epatiche e linfonodali => biopsia TC-guidata, segno della ruota a raggi - tumore desmoplastico del mesentere.
Scintigrafia con octreotide marcato (111 In): sensibilità - 80-90%.
In presenza di metastasi: ecocardiografia.
Studi aggiuntivi (facoltativi):
PET, PET-CT: il valore dello studio è dubbio a causa della lenta crescita del tumore e del basso potenziale di metastasi.
Esami di laboratorio: anemia, funzionalità epatica (albumina, PTI, APTT) e funzionalità renale.


e) Classificazione dei carcinoidi:
In base all'origine dell'organo: derivati dell'intestino anteriore, medio e posteriore.
In base alla localizzazione: intestino tenue, appendice, intestino crasso e retto.
In base allo stadio: localizzate, localmente avanzate (dimensioni, estensione ad altre strutture), metastasi regionali, metastasi a distanza.
In base all'attività secretoria: funzionante e non funzionante.
E) Trattamento del carcinoide senza intervento chirurgico. A scopo palliativo (paziente inoperabile o incurabile con tumore diffuso):
Sindrome carcinoide (iperemia, diarrea, respiro sibilante nei polmoni): analoghi della somatostatina (octreotide).
Controllo/riduzione del tumore: nessun beneficio dalla chemioterapia o radioterapia convenzionale => somministrazione intra-arteriosa di 5FU? Sterptozotocina? Somministrazione sistemica di fluorodeossiuridina (FUDR) + doxorubicina? Interferone? Analoghi della somatostatina marcati con isotopi radioattivi.
Octreotide come preparazione preoperatoria => prevenzione delle crisi carcinoidi.
Trattamento di supporto: ad esempio per la diarrea - loperamide, colestiramina, ecc.
H) Intervento chirurgico per carcinoide
Indicazioni:
Radicale: resezione oncologica standard = metodo di scelta in tutti i pazienti operabili con tumore resecabile => prevenzione delle complicanze locali, riduzione della secrezione ormonale, prevenzione delle alterazioni secondarie.
Palliativo: resezione palliativa, citoriduzione, resezione a cuneo => prevenzione dell'ostruzione intestinale, riduzione della gravità dei sintomi endocrini.
Approccio chirurgico:
carcinoide dell'appendice:
- < 1 см и не в основании (70-80%): аппендэктомия.
- 1-2 cm o estensione al mesentere dell'appendice, o invasione linfatica sottosierosa (=> metastasi nello 0-3% dei casi): emicolectomia destra.
- 2 cm, base dell'appendice, produzione di muco (metastasi nel 30% dei casi): emicolectomia destra.
Carcinoide dell'intestino tenue e crasso: resezione oncologica standard
carcinoide rettale:
- < 2 см без инвазии в мышечную пластинку слизистой: трансанальное иссечение.
-> 2 cm o invasione della mucosa muscolare: resezione oncologica.
Il carcinoide è una neoplasia tumorale che appartiene alla categoria dei potenzialmente maligni. Una delle caratteristiche di questo tumore è la capacità di secernere ormoni (serotonina) e altre sostanze biologiche (prostaglandine, bradichinina). Inoltre, le neoplasie sono caratterizzate da tassi di crescita relativamente bassi.
Varietà di sconfitta
I kartsionoidi differiscono nella localizzazione. Di tutte le formazioni tumorali del tratto digestivo, fino al 10% è rappresentato da questa particolare varietà. Il carcinoide più comunemente riscontrato è l'appendice. Il carcinoide maligno dell'appendice rappresenta fino alla metà dei casi clinici. Circa il 30% è colpito dall'intestino tenue.
Molto meno comuni sono tipi di tumori neuroendocrini come:
- carcinoide polmonare;
- neoplasia condizionatamente maligna dei bronchi;
- carcinoide gastrico;
- tumore del pancreas;
- danno ovarico;
- tumore della cistifellea.
Cause di carcinoide
I tumori di questo tipo, di regola, si sviluppano da cellule che producono ormoni. Qual è il "fattore scatenante" per lo sviluppo di una neoplasia maligna è attualmente sconosciuto.
segni e sintomi
La sintomatologia più pronunciata associata alla produzione dell'ormone si osserva nel carcinoide intestinale. La serotonina è prodotta prevalentemente da tumori localizzati nel digiuno e nell'ileo.
Il paziente può sviluppare la cosiddetta sindrome carcinoide, caratterizzata dai seguenti sintomi:
- forti vampate di calore con rossore o colorazione bluastra del viso e del collo;
- sensazione di bruciore locale e intorpidimento;
- tachicardia;
- gonfiore del viso;
- arrossamento degli occhi;
- aumento della lacrimazione;
- bassa pressione sanguigna;
- broncospasmo;
- dolore nella regione addominale;
- disturbi dispeptici pronunciati.
Sullo sfondo della diarrea, caratteristica delle metastasi epatiche, i pazienti sviluppano:
- ipovolemia;
- iponatriemia;
- ipokaliemia;
- ipocalcemia;
- ipoproteinemia;
- ipocloremia.
La disidratazione e la mancanza di elettroliti vitali possono a loro volta portare a ulteriori disturbi in numerosi organi e sistemi.
Gli attacchi possono essere scatenati da stress fisico o emotivo, nonché dall'assunzione di cibo e/o alcol. Nel periodo iniziale di sviluppo della patologia, gli attacchi possono verificarsi solo una volta ogni pochi mesi, ma nel tempo e in assenza di un trattamento adeguato, la frequenza delle vampate di calore può arrivare fino a 10-20 al giorno. Ogni attacco può durare fino a 10 minuti.
Tuttavia, nella maggior parte dei pazienti con localizzazione del carcinoide nell'intestino tenue o crasso, le manifestazioni cliniche si riducono a dolore spastico nella regione addominale e stitichezza, caratteristica anche di altre neoplasie maligne dell'intestino.
Il carcinoide rettale è caratterizzato dal rilascio di sangue scarlatto durante la defecazione.
Con il progredire della malattia, il paziente può sperimentare:
- perdita di peso (fino alla cachessia);
- epatomegalia (con metastasi epatiche);
- danno al cuore destro (insufficienza della valvola tricuspide, stenosi della bocca dell'arteria polmonare).
- fibrosi dell'endocardio.
Per un periodo piuttosto lungo, il danno gastrico può verificarsi quasi in modo asintomatico. Ciò è dovuto al fatto che le sostanze biologicamente attive sintetizzate dalla neoplasia vengono rapidamente distrutte dall'azione degli enzimi epatici.
Innanzitutto viene rilevato un carcinoide polmonare e un tumore ovarico, poiché in questo caso gli ormoni entrano nella circolazione sistemica, bypassando il fegato.
Diagnosi di carcinoide
La base per la diagnosi sono i dati dell'anamnesi, nonché i risultati ottenuti nel corso di ulteriori studi.
Metodi hardware per la diagnosi del carcinoide
Metodi hardware utilizzati nella diagnostica:
- tomografia computerizzata;
- Risonanza magnetica;
- angiografia;
- studio radiografico.
Il paziente è inoltre tenuto a sottoporsi ad un esame endoscopico (esofagoscopia, gastroduodenoscopia, colonscopia).
Analisi e campioni di iniezione
Molto istruttiva è l'analisi biochimica delle urine (viene rilevato il livello dell'acido 5-idrossiindolacetico, che è uno dei prodotti della biotrasformazione della serotonina). Viene studiata la quantità di questa sostanza nel volume giornaliero di urina.
In alcuni casi, vengono utilizzati test provocativi per chiarire la diagnosi. Le vampate di calore possono essere scatenate da iniezioni di sostanze come pentagastrina, catecolamine, gluconato di calcio o alcol.
Per chiarire la localizzazione e la prevalenza del processo patologico, spesso ricorrono all'intervento chirurgico diagnostico.
Diagnosi differenziale

In casi molto rari, la sindrome carcinoide può svilupparsi sullo sfondo dei tumori cellulari delle cosiddette "isole di Langerhans" del pancreas, così come nel carcinoma polmonare a piccole cellule e nel tumore midollare della tiroide.
Trattamento
Il trattamento del carcinoide prevede una serie di misure, inclusi metodi di esposizione sia conservativi che chirurgici.
Trattamento medico
Farmaci come il tamoxifene e l'interferone alfa aiutano a rallentare leggermente il tasso di crescita del carcinoide.
Trattamento chirurgico del carcinoide
Con una chiara localizzazione della neoplasia, l'unico metodo di trattamento affidabile è la chirurgia, durante la quale la neoplasia viene rimossa entro i confini dei tessuti sani, così come le metastasi.
L'operazione meno efficace per le metastasi epatiche, ma questo intervento consente di prolungare leggermente la vita del paziente.
Terapia chimica e radioterapia
La radioterapia e la chemioterapia sono riconosciute come inefficaci.
Trattamento sintomatico del carcinoide
Con un quadro clinico pronunciato, è indicato Prednisolone (10-20 mg al giorno). La diarrea viene trattata con codeina e ciproeptadina. Per ridurre la pressione sanguigna sono indicati i farmaci antipertensivi.
Possibili complicazioni
La principale complicazione di questo tumore potenzialmente maligno è la metastasi.
Importante: le metastasi si verificano nel 30-70% dei casi. T. n. La sopravvivenza a 5 anni dei pazienti con diagnosi di carcinoide è più della metà dei casi. Nonostante la prognosi sfavorevole, i pazienti, anche senza trattamento, possono vivere più di 10 anni.
Il recupero è possibile solo con il successo del trattamento chirurgico e l'assenza di metastasi tumorali ad altri organi e tessuti.
La causa della morte nella maggior parte dei casi è l'insufficienza cardiaca, metastasi multiple, ostruzione intestinale e malnutrizione estrema (cachessia).
Prevenzione
Poiché l’eziologia di questa grave malattia non è chiara, non sono state sviluppate raccomandazioni speciali per la prevenzione. Si può consigliare, se possibile, di ridurre al minimo l'impatto sul corpo di alcuni fattori esterni che possono agire come cancerogeni.
Dieta, nutrizione
Il rischio di sviluppare tumori maligni dell'intestino è significativamente ridotto nelle persone che non abusano di alcol e consumano la quantità minima del cosiddetto. "carne rossa".
- In contatto con 0
- Google+ 0
- OK 0
- Facebook 0