CARATTERISTICHE MOTIVAZIONALI DELL'ARGOMENTO
La nutrizione umana razionale richiede equilibrio non solo nel contenuto di proteine, grassi, carboidrati, ma anche nel contenuto di micronutrienti. I risultati dello studio dell'alimentazione reale di vari gruppi di popolazione indicano una significativa prevalenza di poliipovitaminosi, carenza di minerali essenziali e fibre alimentari. L’eliminazione delle carenze di micronutrienti non può essere raggiunta semplicemente aumentando l’assunzione di cibo. Le moderne condizioni di vita e di lavoro della maggior parte della popolazione portano ad una diminuzione dei costi energetici, che richiede una riduzione della quantità di cibo consumato e comporta un consumo insufficiente dei micronutrienti in esso contenuti. La conoscenza delle manifestazioni cliniche delle carenze di micronutrienti, delle fonti di vitamine, minerali e fibre alimentari nella dieta, dei metodi per preservare il valore vitaminico degli alimenti e dei metodi di arricchimento preventivo consentono al medico di ottimizzare lo stato nutrizionale dei pazienti.
OBIETTIVO DELLA LEZIONE: familiarizzare con il ruolo biologico, il razionamento e le fonti di micronutrienti e fibre alimentari nella nutrizione; insegnare come determinare la composizione chimica di una dieta in base al contenuto di vitamine, minerali, fibre alimentari utilizzando il metodo di calcolo (utilizzando l'esempio dell'analisi della disposizione del menu della dieta quotidiana di uno studente di medicina), metodi di conservazione e cottura per il risparmio di vitamine cibo e fortificazione preventiva.
LAVORO INDIPENDENTE DEGLI STUDENTI NELLE CLASSI
1. Determinazione della composizione qualitativa della dieta quotidiana di uno studente in base al contenuto di vitamine, minerali, fibre alimentari mediante metodo di calcolo (secondo il layout del menu compilato per l'argomento 3.2.) utilizzando “Tabelle della composizione chimica e valore energetico degli alimenti prodotti."
2. Risolvere problemi situazionali di due tipi orientati professionalmente, documentando la soluzione in un protocollo.
3. Lavoro di laboratorio per determinare il contenuto di vitamina C nelle verdure. 3.1. Determinazione del contenuto di vitamina C nelle patate crude e bollite; calcolo della percentuale di perdita di vitamina C durante la cottura.
3.2. Determinazione del contenuto di vitamina C nel cavolo; calcolo della percentuale di perdita di vitamina C durante la conservazione.
4. Ascolto e discussione degli abstract preparati dagli studenti
secondo le indicazioni individuali dell'insegnante.
COMPITO DI AUTOPREPARAZIONE
1. Ruolo biologico, razionamento, fonti di vitamine idrosolubili nell'alimentazione.
2. Ruolo biologico, razionamento, fonti di vitamine liposolubili nell'alimentazione.
3. Tipi di carenze vitaminiche.
4. Cause di ipovitaminosi, loro manifestazioni.
5. Tecniche per preservare ed incrementare il valore vitaminico delle diete, prevenendo l'ipovitaminosi.
6. Ruolo biologico, razionamento, fonti di minerali nella nutrizione.
7. Ruolo biologico, razionamento, fonti di fibra alimentare nell'alimentazione.
PROTOCOLLO DEL LAVORO INDIPENDENTE
"_____"_____________20___
Tabella 46
Composizione qualitativa della dieta quotidiana di uno studente
| Nomi dei piatti del menu, set di prodotti per porzione | Peso, g | vitamine | Minerali | Fibra alimentare, g | ||||||||
| Con mg | In mg | In mg | Un mg | Dμg | Camg | P mg | K mg | Fe mg | J µg | |||
| COLAZIONE: | ||||||||||||
| 2a COLAZIONE: | ||||||||||||
| CENA: | ||||||||||||
| CENA: | ||||||||||||
| IN GIORNATA TOTALE: |
2. Soluzione di un problema situazionale (tipo 1) No.____
__________________________________________________________________
______________________________________________________________________________________________________________________________________________________________________________________________________
__________________________________________________________________
__________________________________________________________________
Soluzione di un problema situazionale (tipo 2) N.___
__________________________________________________________________
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
__________________________________________________________________
__________________________________________________________________
3. Determinazione del contenuto di vitamina C nelle verdure:
tipo di prodotto _____________, peso del prodotto ____________g,
quantità 0,0001n. soluzione di acido iodico di potassio, utilizzata per il titanio
preparazione del campione _____ml;
Formula per il calcolo:
a) patate crude _______ m, patate bollite _______ mg,
perdita di vitamina C durante la cottura _________%
b) cavolo ______ mg, contenuto medio in cavolo _____ mg,
perdita di vitamina C durante la conservazione _____%.
__________________________________________________________________
__________________________________________________________________
__________________________________________________________________
Ho finito il lavoro __________________
Firma del docente _____________
MATERIALE DI RIFERIMENTO
Definizioni dell'argomento
AVITAMINOSI - completo esaurimento delle risorse vitaminiche del corpo.
ANTIVITAMINICI - composti che escludono parzialmente o completamente le vitamine dalle reazioni metaboliche dell'organismo distruggendole, inattivandole o impedendone l'assimilazione. Gli antivitaminici sono divisi in 2 gruppi:
a) composti simili a strutture (inibitori competitivi; entrano in relazioni competitive con vitamine o loro derivati nelle corrispondenti reazioni metaboliche biochimiche), tra cui sulfamidici, dicumarina, megafen, isoniazide, ecc.
b) composti strutturalmente diversi (antivitaminici naturali; sostanze
che, modificando la molecola o il composto complesso con metaboliti, privano parzialmente o completamente la vitamina della sua azione), tra cui la tiaminasi, l'ascorbinasi, l'avidina, ecc.
Le VITAMINE sono composti organici a basso peso molecolare con elevata attività biologica necessari per la vita normale, che non sono sintetizzati (o sintetizzati in quantità insufficienti) nel corpo ed entrano nel corpo con il cibo. Ruolo biologico vitamine idrosolubili determinato dalla loro partecipazione nella costruzione di vari coenzimi, vitamine liposolubili- nel controllo dello stato funzionale delle membrane cellulari e delle strutture subcellulari.
VITAMINE ANTAGONISTE: B 1 e B 2; A e D; acido nicotinico e colina; tiamina e colina (con la somministrazione a lungo termine di una vitamina per scopi terapeutici, vengono rilevati sintomi di carenza dell'altra).
VITAMINE SINERGISTICHE: C e P; R, S, K; B 12 e acido folico; S, K, B 2; A ed E; E e inositolo (se usati in combinazione in preparati multivitaminici, possono potenziare l’effetto biologico l’uno dell’altro). IPOVITAMINOSI: una forte diminuzione dell'apporto dell'una o dell'altra vitamina nel corpo.
LA FORMA NASCOSTA (LATENTE) DI CARENZA VITAMINICA non presenta manifestazioni o sintomi esterni, tuttavia ha un effetto negativo sulle prestazioni, sulla resistenza dell’organismo a vari fattori avversi e prolunga il recupero dopo una malattia.
FIBRA ALIMENTARE – carboidrati ad alto peso molecolare (cellulosa, emicellulosa, pectine, lignina, chitina, ecc.) prevalentemente di origine vegetale, resistenti alla digestione e all'assorbimento nell'intestino tenue, ma soggetti a fermentazione completa o parziale nell'intestino crasso.
LE CAUSE PIÙ IMPORTANTI DI IPOVITAMINOSI E AVITAMINOSI
1. Apporto insufficiente di vitamine dal cibo.
1.1. Basso contenuto di vitamine nella dieta.
1.2. Ridurre la quantità totale di cibo consumato a causa del basso dispendio energetico.
1.3. Perdita e distruzione di vitamine durante la lavorazione tecnologica dei prodotti alimentari, la loro conservazione e la cottura irrazionale
in lavorazione.
1.4. Deviazioni da una formula nutrizionale bilanciata (la nutrizione prevalentemente a base di carboidrati richiede quantità aggiuntive di tiamina;
con un'introduzione insufficiente di proteine complete, le vitamine C, PP, B1 vengono rapidamente escrete nelle urine, non partecipano ai processi metabolici e la conversione del carotene in vitamina A è ritardata).
1.5. Anoressia.
1.6. La presenza di vitamine in alcuni prodotti in forma non riciclabile (inositolo sotto forma di fitina nei prodotti a base di cereali).
2. Inibizione della microflora intestinale che produce alcune vitamine (B 6, K).
2.1. Malattie del tratto gastrointestinale.
2.2. Conseguenze della chemioterapia (disbiosi).
3. Violazione dell'assimilazione della vitamina.
3.1. Compromissione dell'assorbimento delle vitamine nel tratto gastrointestinale
per malattie dello stomaco, dell'intestino, lesioni del sistema epatobiliare, nonché in età avanzata (alterata secrezione biliare, necessaria per l'assorbimento delle vitamine liposolubili).
3.3. Violazione del metabolismo delle vitamine e formazione delle loro forme biologicamente attive (coenzima) in varie malattie, azione di agenti tossici e infettivi, chemioterapia e nella vecchiaia.
4. Aumento del fabbisogno di vitamine.
4.1. Condizioni fisiologiche speciali del corpo (crescita intensa, gravidanza, allattamento).
4.2. Condizioni climatiche speciali (il fabbisogno di vitamine aumenta del 30-60% a causa dell'aumento del consumo di energia alle basse temperature dell'aria nella zona climatica del Nord).
4.4. Carico neuropsichico significativo, condizioni di stress.
4.5. Esposizione a fattori di produzione dannosi (I lavoratori in negozi caldi esposti ad alte temperature /32 gradi/ con simultanea attività fisica richiedono il doppio di vitamine C, B1, B6, acido pantotenico rispetto a 18 gradi).
4.6. Malattie infettive e intossicazioni (nei processi settici gravi, il fabbisogno di vitamina C dell'organismo raggiunge i 300-500 mg al giorno).
4.7. Malattie degli organi interni e delle ghiandole endocrine.
4.8. Maggiore escrezione di vitamine.
5. Disturbi congeniti, geneticamente determinati, del metabolismo e delle funzioni delle vitamine.
5.1. Disturbi congeniti dell'assorbimento delle vitamine.
5.2. Disturbi congeniti del trasporto delle vitamine nel sangue e attraverso le membrane cellulari.
5.3. Disturbi congeniti della biosintesi delle vitamine (acido nicotinico da triptofano).
5.4. Disturbi congeniti della conversione delle vitamine in coenzimi
forme, gruppi prostetici e metaboliti attivi.
5.5. Violazione dell'inclusione di vitamine nel centro attivo dell'enzima.
5.6. Violazione della struttura dell'apoenzima, complicando la sua interazione con il coenzima.
5.7. Violazione della struttura dell'apoenzima, che porta alla perdita completa o parziale dell'attività enzimatica, indipendentemente dall'interazione con il coenzima.
5.8. Aumento del catabolismo delle vitamine.
5.9. Disturbi congeniti del riassorbimento delle vitamine nei reni.
Tabella 47
(per 100 g di parte edibile)
| Prodotti | IN 1 | ALLE 2 | RR | ALLE 6 | CON | E | UN | V-ka-ro-ting | D | ALLE 12 | Acido folico. | ||||
| mg/100 g | µg/100 g | ||||||||||||||
| pane di segale | 0,18 | 0,11 | 0,67 | 0,17 | - | 2,2 | - | - | - | - | |||||
| Pane di grano | 0,21 | 0,12 | 2,81 | 0,3 | - | 3,8 | - | - | - | - | |||||
| Fiocchi d'avena. | 0,49 | 0,11 | 1,1 | 0,27 | - | 3,4 | - | - | - | - | |||||
| Semolino | 0,14 | 0,07 | 1,0 | 0,17 | - | 2,5 | - | - | - | - | |||||
| Semole di riso | 0,08 | 0,04 | 1,6 | 0,18 | - | 0,4 | - | - | - | - | |||||
| Semole di grano saraceno. | 0,53 | 0,2 | 4,19 | 0,4 | - | 6,6 | - | - | - | - | |||||
| Miglio | 0,62 | 0,04 | 1,55 | 0,52 | - | 2,6 | - | 0,15 | - | - | |||||
| Pasta | 0,17 | 0,08 | 1,21 | 0,16 | - | 2,1 | - | - | - | - | |||||
| Manzo | 0,07 | 0,18 | 3,0 | 0,39 | Sl | - | - | - | - | 2,8 | 8,9 | ||||
| Maiale | 0,52 | 0,14 | 2,4 | 0,33 | Sl | - | - | - | - | - | 5,5 | ||||
| Fegato di manzo | 0,3 | 2,19 | 6,8 | 0,7 | 1,3 | 3,8 | 1,0 | - | |||||||
| La salsiccia è bollita. | 0,25 | 0,18 | 2,47 | 0,19 | - | - | - | - | - | - | |||||
| Polli | 0,07 | 0,15 | 3,6 | 0,61 | - | - | 0,1 | - | - | - | 5,8 | ||||
| Uova di gallina | 0,07 | 0,44 | 0,2 | 0,14 | - | 0,3 | - | 4,7 | 0,1 | 7,5 | |||||
| Merluzzo | 0,09 | 0,16 | 2,3 | 0,17 | Sl. | 0,9 | Sl. | - | - | 1,6 | 11,3 | ||||
| Caviale di storione. | 0,3 | 0,36 | 1,5 | 0,29 | 7,8 | - | 0,2 | - | - | ||||||
| Pastore del latte. | 0,03 | 0,13 | 0,1 | - | 1,0 | - | Sl. | 0,01 | - | - | - | ||||
| Kefir | 0,03 | 0,17 | 0,14 | 0,06 | 0,7 | 0,1 | Sl. | 0,01 | - | 0,4 | 7,8 | ||||
| Panna acida | 0,02 | 0,1 | 0,07 | 0,07 | 0,2 | 0,5 | 0,2 | 0,1 | 0,1 | 0,36 | 8,5 | ||||
| Fiocchi di latte | 0,04 | 0,27 | 0,4 | 0,11 | 0,5 | 0,4 | 0,1 | 0,03 | - | 1,0 | 35,0 | ||||
| Formaggi a pasta dura | 0,02 | 0,3 | 0,3 | 0,1 | 1,6 | 0,5 | 0,2 | 0,1 | - | 2,5 | 10-45 | ||||
| Burro | Sl | 0,01 | 0,1 | - | - | - | 0,5 | 0,34 | - | - | - | ||||
| L'olio di girasole è raffinato. | _ | - | - | - | - | - | - | - | - | - | |||||
| Piselli | 0,81 | 0,15 | 2,2 | 0,27 | - | 9,1 | - | 0,07 | - | - | |||||
| Patata | 0,12 | 0,05 | 0,9 | 0,3 | 0,1 | - | 0,02 | - | - | ||||||
| cavolo bianco | 0,06 | 0,05 | 0,4 | 0,14 | 0,1 | - | 0,02 | - | - | ||||||
| Cipolla verde | 0,02 | 0,1 | 0,3 | 0,15 | - | - | - | ||||||||
| Pomodori | 0,06 | 0,04 | 0,53 | 0,1 | 0,4 | - | 1,2 | - | - | ||||||
| cetrioli | 0,03 | 0,04 | 0,2 | 0,04 | 0,1 | - | 0,06 | - | - | ||||||
| Barbabietola | 0,02 | 0,04 | 0,2 | 0,07 | 0,1 | - | 0,01 | - | - | ||||||
| Carota | 0,06 | 0,07 | 0,13 | 0,6 | - | - | - | ||||||||
| Funghi porcini | 0,02 | 0,3 | 4,6 | 0,07 | 0,6 | - | - | - | - | ||||||
| Mele | 0,01 | 0,03 | 0,3 | 0,08 | 0,6 | - | 0,03 | - | - | 1,6 | |||||
| Albicocche | 0,03 | 0,06 | 0,07 | 0,05 | 0,9 | - | 1,6 | - | - | ||||||
| Ciliegie | 0,03 | 0,3 | 0,4 | 0,05 | 0,3 | - | 0,1 | - | - | ||||||
| Lamponi | 0,02 | 0,05 | 0,6 | 0,07 | 0,6 | - | 0,2 | - | - | ||||||
| Fragole | 0,03 | 0,05 | 0,3 | 0,06 | 0,5 | - | 0,03 | - | - | ||||||
| Ribes nero | 0,02 | 0,02 | 0,3 | 0,13 | 0,7 | - | 0,1 | - | - | ||||||
| Olivello spinoso | 0,1 | 0,05 | 0,6 | 0,11 | - | - | - | ||||||||
| La rosa canina è secca. | 0,15 | 0,84 | 1,5 | - | - | - | 6,7 | - | - | - | |||||
| Uva | 0,05 | 0,02 | 0,3 | 0,09 | - | - | Sl. | - | - | ||||||
| Limoni | 0,04 | 0,02 | 0,1 | 0,06 | - | - | 0,01 | - | - | ||||||
| Arance | 0,04 | 0,03 | 0,2 | 0,06 | 0,2 | - | 0,05 | - | - | ||||||
| Dolci, torte | 0,75 | 0,1 | 0,7 | - | - | - | 0,1 | 0,14 | - | - | - | ||||
| Il lievito viene pressato. | 0,6 | 0,68 | 11,4 | 0,58 | - | - | - | - | - | - | |||||
GOST R54635-2011
Gruppo H59
STANDARD NAZIONALE DELLA FEDERAZIONE RUSSA
PRODOTTI ALIMENTARI FUNZIONALI
Metodo di determinazione della vitamina A
Prodotti alimentari funzionali. Metodo di determinazione della vitamina A
OKS 67.050
OKSTU9109
Data di introduzione 2013-01-01
Prefazione
Gli obiettivi e i principi della standardizzazione nella Federazione Russa sono stabiliti dalla legge federale N 184-FZ "Sulla regolamentazione tecnica" del 27 dicembre 2002, e le regole per l'applicazione degli standard nazionali della Federazione Russa sono GOST R 1.0-2004 "Standardizzazione in Federazione Russa. Disposizioni fondamentali"
Informazioni standard
1 SVILUPPATO dall'Istituto di ricerca sulla nutrizione dell'Accademia russa delle scienze mediche
2 INTRODOTTO dal Comitato Tecnico per la Standardizzazione TC 36 “Prodotti Alimentari Funzionali”
3 APPROVATO ED ENTRATO IN EFFETTO con ordinanza dell'Agenzia federale per la regolamentazione tecnica e la metrologia del 12 dicembre 2011 N 784-st
4 INTRODOTTO PER LA PRIMA VOLTA
Le informazioni sulle modifiche a questo standard sono pubblicate nell'indice delle informazioni pubblicato annualmente "Norme nazionali" e il testo delle modifiche e degli emendamenti è pubblicato nell'indice delle informazioni pubblicate mensilmente "Norme nazionali". In caso di revisione (sostituzione) o cancellazione della presente norma, il corrispondente avviso sarà pubblicato nell'indice informativo pubblicato mensilmente "Norme nazionali". Informazioni, notifiche e testi rilevanti sono pubblicati anche nel sistema informativo pubblico - sul sito web ufficiale dell'Agenzia federale per la regolamentazione tecnica e la metrologia su Internet
1 zona di utilizzo
1 zona di utilizzo
Questo standard si applica agli alimenti funzionali e stabilisce un metodo per determinare la frazione di massa della vitamina A sotto forma di retinolo, retinolo acetato, retinolo palmitato mediante cromatografia liquida ad alte prestazioni (di seguito denominata HPLC).
L'intervallo di misurazione per la frazione di massa della vitamina A va da 0,5 a 10,0 milioni.
Nota - Questo standard può essere applicato ai prodotti alimentari a condizione che venga rispettato l'intervallo di misurazione.
2 Riferimenti normativi
Questo standard utilizza riferimenti normativi ai seguenti standard:
GOST R 8.563-2009 Sistema statale per garantire l'uniformità delle misurazioni. Tecniche di misurazione (metodi)
GOST R 12.1.019-2009 Sistema di standard di sicurezza sul lavoro. Sicurezza elettrica. Requisiti generali e nomenclatura dei tipi di protezione
GOST R ISO 5725-6-2002 Accuratezza (correttezza e precisione) dei metodi e dei risultati di misurazione. Parte 6: Utilizzo dei valori di precisione nella pratica
GOST R ISO/IEC 17025-2006 * Requisiti generali per la competenza dei laboratori di prova e taratura
________________
GOST ISO/IEC 17025-2009
GOST R 51652-2000 Alcool etilico rettificato da materie prime alimentari. Specifiche
GOST R 52062-2003 Oli vegetali. Regole di accettazione e metodi di campionamento
GOST R 52179-2003 Margarine, grassi per l'industria della cucina, dolciaria, della panificazione e lattiero-casearia. Regole di accettazione e metodi di controllo
GOST R 52349-2005 Prodotti alimentari. Prodotti alimentari funzionali. Termini e definizioni
GOST R 53228-2008 Bilance non automatiche. Parte 1. Requisiti metrologici e tecnici. Test
GOST 12.1.004-91 Sistema di standard di sicurezza sul lavoro. Sicurezza antincendio. Requisiti generali
GOST 12.1.005-88 Sistema di standard di sicurezza sul lavoro. Requisiti sanitari e igienici generali per l'aria nell'area di lavoro
GOST 12.1.007-76 Sistema di standard di sicurezza sul lavoro. Sostanze nocive. Classificazione e requisiti generali di sicurezza
GOST 427-75 Righelli di misurazione in metallo. Specifiche
GOST 1770-74 (ISO 1042-83, ISO 4788-80) Vetreria da laboratorio. Cilindri, bicchieri, beute, provette. Condizioni tecniche generali
Reagenti GOST 4166-76. Solfato di sodio. Specifiche
Reagenti GOST 4517-87. Metodi per preparare reagenti ausiliari e soluzioni utilizzati nelle analisi
GOST 6709-72 Acqua distillata. Specifiche
GOST 9293-74 Azoto, gassoso e liquido. Specifiche
GOST 12026-76 Carta da filtro da laboratorio. Specifiche
GOST 13496.0-80 * Mangimi composti, materie prime. Metodi di campionamento
________________
*Il documento non è valido sul territorio della Federazione Russa. È valida la norma GOST R ISO 6497-2011, di seguito nel testo. - Nota del produttore del database.
GOST 14919-83 Fornelli elettrici domestici, fornelli elettrici e friggitrici elettriche. Condizioni tecniche generali
GOST 16317-87 Apparecchi di refrigerazione elettrici domestici. Condizioni tecniche generali
GOST 18300-87 Alcool etilico tecnico rettificato. Specifiche
GOST 19627-74 Idrochinone (paradiossibenzene). Specifiche
Reagenti GOST 24363-80. Idrossido di potassio. Specifiche
GOST 25336-82 Vetreria e attrezzature da laboratorio. Tipi, parametri principali e dimensioni
GOST 26809-86 Latte e prodotti lattiero-caseari. Regole di accettazione, metodi di campionamento e preparazione dei campioni per le fognature
Reagenti GOST 27025-86. Istruzioni generali per il test
GOST 28498-90 Termometri in vetro liquido. Requisiti tecnici generali. Metodi di prova
GOST 29227-91 (ISO 835-1-81) Vetreria da laboratorio. Pipette graduate. Parte 1. Requisiti generali
Nota - Quando si utilizza questo standard, è consigliabile verificare la validità degli standard di riferimento nel sistema di informazione pubblica - sul sito web ufficiale dell'Agenzia federale per la regolamentazione tecnica e la metrologia su Internet o secondo l'indice informativo pubblicato annualmente "Nazionale Standards", pubblicata a partire dal 1° gennaio dell'anno in corso, e secondo i corrispondenti indici informativi mensili pubblicati nell'anno in corso. Se lo standard di riferimento viene sostituito (modificato), quando si utilizza questo standard dovresti essere guidato dallo standard sostitutivo (modificato). Se la norma di riferimento viene annullata senza sostituzione, la disposizione in cui ad essa è fatto rinvio si applica nella parte che non pregiudica tale rinvio.
3 Termini e definizioni
Questo standard utilizza termini secondo GOST R 52349, nonché il seguente termine con la definizione corrispondente:
4 Essenza del metodo
La determinazione della vitamina A nell'estratto ottenuto dal campione analizzato viene effettuata mediante separazione HPLC seguita da rilevazione fotometrica o fluorimetrica. Se necessario, l'estratto viene ottenuto dopo idrolisi alcalina del campione analizzato.
L'analisi quantitativa viene effettuata mediante il metodo dello standard esterno utilizzando l'area o l'altezza dei picchi di retinolo, retinolo acetato, retinolo palmitato.
5 Requisiti di sicurezza
5.1 Condizioni per un lavoro sicuro
Quando si eseguono i test, è necessario rispettare i requisiti di sicurezza antincendio stabiliti da GOST 12.1.004, sicurezza elettrica - GOST R 12.1.019, precauzioni di sicurezza quando si lavora con reagenti - GOST 12.1.007, nonché i requisiti stabiliti nel documentazione tecnica per uno spettrofotometro, un cromatografo e altri dispositivi e apparecchiature.
Il locale in cui vengono effettuate le prove deve essere dotato di ventilazione di mandata e di scarico. Il monitoraggio del contenuto di sostanze nocive nell'aria dell'area di lavoro deve essere effettuato in conformità con i requisiti di GOST 12.1.005.
Quando si lavora con le bombole di gas, è necessario seguire queste istruzioni:
5.2 Requisiti di qualificazione dell'operatore
Sono autorizzate a eseguire test ed elaborare i risultati persone con un'istruzione specialistica superiore o secondaria nelle seguenti professioni: chimico, ingegnere chimico, tecnico, assistente di laboratorio, con esperienza in un laboratorio chimico. Il primo utilizzo del metodo in laboratorio deve essere effettuato sotto la supervisione di un tecnico HPLC qualificato.
6 Condizioni di prova
6.1 Condizioni generali
I test vengono eseguiti in normali condizioni di laboratorio: temperatura ambiente - (25±5) °C; umidità relativa - (65±15)%; Frequenza CA - (50±5) Hz; tensione di rete - (220±10) V.
Durante la preparazione e la conservazione delle soluzioni, è necessario soddisfare i requisiti di GOST 27025, GOST 4517.
Per prevenire la distruzione della vitamina A, l'analisi del materiale di prova e degli standard viene effettuata in presenza di un antiossidante (acido ascorbico, idrochinone, pirogallolo), proteggendo i campioni dalla luce solare diretta.
6.2 Condizioni per le misurazioni fotometriche
Le condizioni di misurazione fotometrica sono riportate nella Tabella 1.
Tabella 1 - Condizioni di misurazione fotometrica
Vitamina A | Solvente | Lunghezza d'onda, nm | Tasso di assorbimento specifico |
Retinolo | |||
Acetato di retinolo | |||
Palmitato di retinolo | 2-propanolo |
6.3 Condizioni per l'analisi cromatografica
Temperatura della colonna cromatografica: 25 °C o temperatura ambiente.
Portata fase mobile: 0,7 cm/min (valore indicativo).
Volume del campione iniettato: 50·10 cm.
Fase mobile: miscela di acetonitrile, alcool metilico, cloruro di metilene in rapporto in volume 50:45:5.
L'ottimalità delle condizioni di separazione cromatografica viene verificata mediante analisi cromatografica di una soluzione mista di retinolo, retinolo acetato, retinolo palmitato con una concentrazione in massa di ciascuna sostanza di almeno 0,4 μg/cm. Questa soluzione mista viene preparata da soluzioni basiche di retinolo, retinolo acetato, retinolo palmitato per analogia con la procedura per la preparazione delle soluzioni di lavoro secondo 8.1.2. L'efficienza della separazione cromatografica è considerata soddisfacente se il coefficiente di separazione dei picchi adiacenti di retinolo, retinolo acetato e retinolo palmitato è almeno 1,3. Altrimenti, per ottenere l'efficienza di separazione richiesta, si seleziona sperimentalmente la portata della fase mobile o si testano altre colonne.
7 Strumenti di misura, dispositivi ausiliari, reagenti e materiali
7.1 Per determinare il contenuto della frazione di massa della vitamina A, vengono utilizzati i seguenti strumenti di misurazione, apparecchiature ausiliarie e materiali:
- bilance conformi a GOST R 53228, che garantiscono la precisione della pesatura entro l'errore assoluto consentito di ±0,1 mg;
- spettrofotometro con un intervallo spettrale di funzionamento da 190 a 1100 nm, l'errore principale nelle misurazioni della trasmittanza non è superiore all'1%;
- cuvette in quarzo con cammino ottico di 1 cm;
- cromatografo liquido ad alta prestazione, comprendente i seguenti elementi: pompa; dispositivo per l'iniezione del campione; rilevatore fluorimetrico (lunghezze d'onda, nm: eccitazione - 325 nm, emissione - 470 nm) o rilevatore spettrofotometrico (lunghezza d'onda di rilevamento - 325 nm) con un livello di rumore non superiore a 10 unità di densità ottica e un relativo errore di misurazione non superiore al 10% ; una colonna analitica per HPLC del diametro di 0,30-0,46 cm, della lunghezza di 10-25 cm, riempita con gel di ottadecilsilice con granulometria di 5 micron; dispositivo di registrazione - un integratore o registratore che consente di misurare l'area (o l'altezza) di un picco con un errore non superiore all'1%; Software per l'elaborazione dei risultati di misurazione ottenuti;
- filtri per filtrare la fase mobile e le soluzioni analizzate (ad esempio, con una dimensione dei pori di 0,45 micron);
- una microsiringa tipo Hamilton con capacità di 0,1 cm per l'introduzione dei campioni in un cromatografo liquido;
- pipette graduate 1(2,3)-1(2)-1-0,5(1,2,5,10,25) secondo GOST 29227 o dispensatori automatici con volumi di dose simili o variabili con un errore di dosaggio relativo non superiore a superiore a ± 1%;
- cilindri 1-50(100.250)-1(2) secondo GOST 1770;
- matracci tarati 2-50(100,250,500,1000)-2 secondo GOST 1770;
- tubi di misura con tappi rettificati P-2-5(10,15,20,25)-0,1(0,2)ХС secondo GOST 1770;
- vetri V(N)-1-50(100,150,250)ТХС secondo GOST 25336;
- palloni a fondo tondo K-1-100(250,500)-29/32TS secondo GOST 25336;
- imbuti V-36(56)-80ХС, В-75-110(140)ХС, В-100-150ХС secondo GOST 25336;
- righello in metallo con un valore di divisione di 1 mm secondo GOST 427;
- agitatore per matracci e provette con frequenza di vibrazione della piattaforma compresa tra 100 e 150 vibrazioni al minuto;
- centrifuga da 4-6mila giri al minuto;
- bagnomaria con regolatore di riscaldamento, mantenimento della temperatura da 40° a 100°C;
- bagno da laboratorio ad ultrasuoni con un volume di lavoro di almeno 2 dm;
- evaporatore rotante con un range di pressione di esercizio da 7 mm Hg. fino a 760 mmHg. (da 9·10 Pa a 10·10 Pa) o una pompa a getto d'acqua secondo GOST 25336;
- frigoriferi in vetro da laboratorio conformi a GOST 25336;
- termometro liquido da laboratorio con intervallo di temperatura da 0 °C a 100 °C, divisione scala 1 °C secondo GOST 28498;
- una bombola con gas di azoto conforme a GOST 9293, purezza speciale e secondo;
- carta da filtro da laboratorio secondo GOST 12026;
- piastrelle elettriche chiuse secondo GOST 14919;
- mulino elettrico da laboratorio;
- frigorifero domestico secondo GOST 16317.
7.2 Quando si eseguono misurazioni, vengono utilizzati i seguenti reagenti e materiali:
- alcol etilico assoluto () con una frazione di massa della sostanza principale pari ad almeno il 99,9%;
- alcol etilico rettificato (con una frazione in massa della sostanza principale pari ad almeno il 96% o secondo GOST R 51652, GOST 18300);
- la frazione di massa dell'alcol metilico () della sostanza principale non è inferiore al 99,9%;
- la frazione di massa dell'acetonitrile () della sostanza principale non è inferiore al 99,8%;
- la frazione di massa del cloruro di metilene () della sostanza principale non è inferiore al 99,8%;
- la frazione di massa n-esano () della sostanza principale non è inferiore al 99%;
- etil acetano () con una frazione di massa della sostanza principale pari ad almeno il 99% o secondo GOST 8981;
- la frazione di massa del propanolo-2 () della sostanza principale non è inferiore al 99%;
- etere di petrolio, distillato alla temperatura di (50±10) °C, purificato dai perossidi;
- etere etilico, purificato dai perossidi, contenente 0,1% pirogallolo, secondo;
- idrossido di potassio (KOH) secondo GOST 24363, grado chimico. o soluzione di KOH di grado analitico con una frazione in massa del 50%;
- solfato di sodio (anidro) con una frazione di massa della sostanza principale almeno del 99,5% o secondo GOST 4166, chimicamente puro;
- acqua distillata secondo GOST 6709;
- acido ascorbico () secondo il grado del reagente;
- idrochinone () con una frazione di massa della sostanza principale pari ad almeno il 99% o secondo GOST 19627;
- la frazione di massa del pirogallolo () della sostanza principale non è inferiore al 99%;
- butilidrossitoluene () con una frazione di massa della sostanza principale pari ad almeno il 99%;
- retinolo () = 286,5 g/mol, la frazione in massa della sostanza principale non è inferiore al 90%;
- retinolo acetato () = 328,5 g/mol, la frazione in massa della sostanza principale non è inferiore al 90% oppure;
- retinolo palmitato () = 524,9 g/mol, la frazione in massa della sostanza principale non è inferiore al 90% o .
7.3 È consentito utilizzare altri strumenti di misurazione, apparecchiature ausiliarie che non siano inferiori a quanto sopra in termini di caratteristiche metrologiche e tecniche e forniscano la necessaria precisione di misurazione, nonché reagenti e materiali di qualità non peggiore di quanto sopra.
8 Preparazione per effettuare le misurazioni
8.1 Preparazione delle soluzioni
8.1.1 Soluzioni standard di base
Sciogliere circa 50 mg di retinolo (o retinolo acetato, o retinolo palmitato) in 50 ml di alcool etilico assoluto. La concentrazione in massa di retinolo (o retinolo acetato o retinolo palmitato) nella soluzione è di circa 1,0 mg/cm. Successivamente, 2 cm di una soluzione di retinolo (o acetato di retinolo o palmitato di retinolo) vengono posti in un matraccio tarato da 50 cm utilizzando una pipetta e portati alla tacca con alcool etilico assoluto. La concentrazione in massa dei composti nelle soluzioni standard madre risultanti è di circa 40 μg/cm.
8.1.2 Soluzioni di calibrazione
Dalle soluzioni standard di base, vengono preparate almeno quattro soluzioni di calibrazione di retinolo (o acetato di retinolo o palmitato di retinolo) nell'intervallo di concentrazione in massa di 0,4-4,0 μg/cm diluendo accuratamente le soluzioni standard di base con alcol etilico assoluto in un recipiente da 50 ml. matraccio tarato.
La determinazione della concentrazione in massa di retinolo (o acetato di retinolo o palmitato di retinolo) (μg/cm) viene effettuata dopo aver misurato la densità ottica delle soluzioni di calibrazione in una cuvetta di quarzo con uno strato assorbente dello spessore di 1 cm su uno spettrofotometro alla lunghezza d'onda ottimale e viene calcolata utilizzando la formula
dov'è la densità ottica della soluzione di calibrazione;
- il valore di densità ottica della soluzione di calibrazione in alcol etilico assoluto o 2-propanolo con una concentrazione in massa di 1 g per 100 cm con uno spessore dello strato assorbente di 1 cm, riportato nella Tabella 1;
10 - fattore di conversione;
- coefficiente che tiene conto dell'assorbimento dei componenti associati durante la misurazione, calcolato dalla formula
dov'è l'area del picco della sostanza standard durante l'analisi HPLC, mAU·s (AU·s);
- la somma delle aree dei picchi dei componenti associati durante l'analisi HPLC della sostanza standard, mAU·s (AU·s).
Tutte le soluzioni sono accuratamente protette dalle radiazioni ultraviolette durante la preparazione e l'analisi. Le soluzioni di retinolo vengono conservate a temperature inferiori a 4 °C per 2 mesi. Per le misurazioni vengono utilizzate soluzioni appena preparate di retinolo acetato o retinolo palmitato per 2-3 ore a temperatura ambiente.
8.2 Campionamento e preparazione
8.2.1 Il campionamento viene effettuato in conformità con GOST 13496.0, GOST 26809, GOST R 52062, GOST R 52179.
8.2.2 Le particelle grossolane del campione medio, separate mediante quarti dal campione di laboratorio, vengono frantumate utilizzando un'attrezzatura adeguata (ad esempio un mulino da laboratorio) fino a quando l'intero prodotto passa attraverso un setaccio con aperture di 1 mm di diametro. Il campione macinato viene accuratamente miscelato.
I campioni analizzati vengono omogeneizzati, evitando l'esposizione a temperature elevate.
8.2.3 Prodotti alimentari a base di grassi e oli con un contenuto di acqua pari o inferiore all'1% in massa, arricchiti con retinolo acetato o retinolo palmitato
2-5 g del campione analizzato vengono trasferiti in un matraccio tarato da 25 cm, sciolti in 10-15 cm di n-esano, utilizzando un bagno ad ultrasuoni per accelerare la dissoluzione. La soluzione viene portata a volume con n-esano. Se necessario, la soluzione può essere utilizzata per la successiva diluizione con n-esano. Successivamente un'aliquota della soluzione esana viene evaporata in corrente di azoto ed il residuo secco viene ridisciolto nell'eluente.
8.2.4 Prodotti alimentari a base di oli e grassi con una frazione di acqua non superiore al 20%, arricchiti con retinolo acetato o retinolo palmitato
2-5 g del campione analizzato vengono sciolti sotto vigorosa agitazione in 10-15 cm di n-esano, utilizzando un bagno ad ultrasuoni per accelerare la dissoluzione. Rimuovere l'acqua in eccesso aggiungendo solfato di sodio anidro. Il contenuto del pallone viene filtrato attraverso un filtro di carta per separare i sedimenti non disciolti. Il pallone viene lavato due volte con 5 cm di n-esano. Si raccolgono i filtrati in un matraccio tarato da 25 cm e si porta a volume la soluzione con n-esano. Successivamente un'aliquota della soluzione esana viene evaporata in corrente di azoto ed il residuo secco viene ridisciolto nell'eluente.
8.2.5 Altri alimenti arricchiti con retinolo acetato o retinolo palmitato
Per effettuare l'idrolisi alcalina, 1-30 g del campione analizzato di materiale secco o liquido vengono posti in un pallone a fondo tondo con una capacità di 100-500 cm, al materiale secco vengono aggiunti 5-20 cm di acqua e riscaldato a bagnomaria ad una temperatura di 60°C - 70°C agitando per 5 minuti Aggiungere quindi 50-150 cm di alcool etilico rettificato (o alcool metilico), 0,2-1,0 g di antiossidante (acido ascorbico, idrochinone, butilidrossitoluene), 4-40 cm di una soluzione al 50% di idrossido di potassio e scaldare per 15-45 minuti a bagnomaria con riflusso ad una temperatura di 80°C-100°C.
I rapporti consigliati tra materiale di prova e reagenti sono riportati nella Tabella 2.
Tabella 2 – Rapporti consigliati tra materiale di prova e reagenti
Frazione di massa della vitamina A, milioni | Peso del materiale di prova, g | Volume di etanolo, cm | Volume della soluzione di KOH al 50%, cm |
Da 0,1-1,0 incl. | |||
St. 1.0-5.0 incl. | |||
St. 5.0-10.0 incl. |
Quando si effettua l'idrolisi alcalina a temperatura ambiente per almeno 16 ore, vengono utilizzati i rapporti di materiale e reagenti sopra indicati.
Se, dopo il raffreddamento, sulla superficie della miscela rimane uno strato di olio o grasso, il volume della soluzione KOH aggiunta e il tempo per l'idrolisi alcalina aumentano.
Una volta completata l'idrolisi, il contenuto del pallone viene rapidamente raffreddato a (20±5) °C e trasferito quantitativamente in un imbuto separatore. Il pallone viene risciacquato con acqua, il cui volume è pari al volume di alcol etilico (o alcol metilico) aggiunto, e l'acqua viene versata nello stesso imbuto. La vitamina A viene estratta con dietil (o petrolio) etere, n-esano, n-esano con l'aggiunta di dietil (o petrolio) etere in un rapporto in volume di 1:1 per due minuti. Per tenere conto della possibile estrazione incompleta della vitamina A, dovrebbe essere utilizzato il metodo di aggiunta standard.
L'estrazione viene ripetuta tre o quattro volte con porzioni di 50-100 cm di solvente. L'estratto combinato viene lavato dagli alcali tre o quattro volte con porzioni di 50-150 cm di acqua fino a scomparsa della reazione alcalina dell'acqua di lavaggio (utilizzando carta indicatrice universale ).
Per eliminare l'acqua, l'estratto viene filtrato su un filtro con 2-5 g di solfato di sodio anidro. Successivamente, l'estratto viene evaporato a secchezza utilizzando un evaporatore rotante ad una temperatura non superiore a 50 °C e quindi ridisciolto nell'eluente. Se necessario, la soluzione può essere utilizzata per la successiva diluizione.
La soluzione ottenuta secondo 8.2.3 (8.2.4, 8.2.5) viene analizzata mediante HPLC. La massa del campione analizzato e il volume del solvente sono selezionati in modo tale che la concentrazione degli analiti nella soluzione analizzata sia compresa tra 0,4 e 4,0 μg/cm.
8.3 Preparazione del cromatografo liquido
La preparazione del cromatografo liquido per il funzionamento viene eseguita in conformità con il manuale di istruzioni dell'apparecchiatura. Prima di iniziare il lavoro, la colonna viene lavata con l'eluente.
8.4 Costruzione della dipendenza dalla calibrazione
Le procedure per costruire la dipendenza dalla calibrazione vengono eseguite in conformità con il manuale operativo dell'apparecchiatura. Condurre l'analisi cromatografica di tutte le soluzioni di calibrazione preparate secondo 8.1.2.
Il grafico di calibrazione è costruito nelle coordinate "segnale analitico" - "concentrazione di massa di vitamina nella soluzione di calibrazione, µg/cm". Per ciascuna soluzione di calibrazione analizzata vengono effettuate due misurazioni parallele e viene ricavato il valore medio aritmetico. La differenza tra i valori del segnale analitico misurato e i valori del tempo di ritenzione non deve superare il 5% dei valori medi. Le sezioni lineari del grafico di calibrazione devono corrispondere all'intero intervallo di concentrazioni di massa determinate di vitamina A.
Il coefficiente della curva di calibrazione, μg/cm/(mAU s) o μg/cm/(AU s) è determinato come valore medio aritmetico dei coefficienti calcolati utilizzando la formula
dove è la concentrazione in massa delle sostanze standard nella esima soluzione di calibrazione, μg/cm;
- area (altezza) del segnale analitico durante l'analisi della soluzione di calibrazione, mAU·s (AU·s) o altezza del picco, mm.
La correttezza della costruzione della dipendenza dalla calibrazione è controllata dal valore dell'approssimazione attendibile di 0,997.
La calibrazione viene eseguita nei seguenti casi: nella fase di padronanza del metodo, quando si modificano le condizioni dell'analisi cromatografica o quando si identifica la non conformità ai requisiti metrologici con i risultati del controllo operativo o dell'audit interno.
9 Effettuare le misurazioni
Volumi uguali delle soluzioni di test e di calibrazione vengono introdotti in sequenza nella colonna del cromatografo. Come soluzione di calibrazione viene scelta la soluzione la cui altezza del picco differisce meno dall'altezza del picco della soluzione di prova. La concentrazione di vitamina A () nella soluzione utilizzata per la calibrazione viene determinata il giorno del suo utilizzo secondo 8.1.2.
Per identificare i picchi, confrontare il tempo di ritenzione del retinolo (o acetato di retinolo o palmitato di retinolo) della soluzione di prova e della soluzione standard e aggiungere anche una soluzione standard con un contenuto di vitamina A simile alla soluzione di prova.
10 Elaborazione e presentazione dei risultati
La frazione di massa della vitamina A, ppm, viene calcolata utilizzando le formule:
dove è il coefficiente della curva di calibrazione secondo 8.4;
- volume di diluizione, cm;
- massa del campione analizzato, g.
Utilizzando una soluzione di calibrazione
dove è la concentrazione in massa della soluzione di calibrazione, μg/cm;
- volume di diluizione, cm;
- valore medio aritmetico dei risultati delle misurazioni dell'area (altezza) del picco del componente analizzato per due analisi cromatografiche parallele della soluzione in esame, mAU·s (AU·s) o altezza del picco, mm;
- massa del campione analizzato, g;
- valore medio aritmetico dei risultati delle misurazioni dell'area (altezza) del picco del componente analizzato per due analisi cromatografiche parallele della soluzione di calibrazione, mAU·s (AU·s) o altezza del picco, mm.
Il risultato viene calcolato alla terza cifra decimale e arrotondato alla seconda cifra decimale.
Quando si analizza ciascun campione, vengono eseguite due determinazioni parallele, iniziando con il prelievo di una porzione del campione da analizzare.
La discrepanza tra i risultati di due misurazioni parallele (come percentuale del valore medio) eseguite da un operatore utilizzando reagenti e apparecchiature identiche e nel più breve periodo di tempo possibile non deve superare (il limite di ripetibilità è fornito nella Tabella 3) con un probabilità di confidenza del 95%.
Se questa condizione è soddisfatta, come risultato finale del test viene preso il valore della media aritmetica.
I limiti dell'errore relativo nel determinare la frazione di massa della vitamina A (), come percentuale del risultato del test e con una probabilità di confidenza del 95%, non devono superare i valori specificati nella Tabella 3.
Il risultato della determinazione della vitamina A è presentato come segue:
Milioni al 95%, (6)
dove è il valore medio aritmetico dei risultati di due determinazioni parallele, milioni;
- valore del limite di errore assoluto delle determinazioni, milioni, calcolato dalla formula
I risultati del test vengono registrati in un protocollo, che indica:
- riferimento a questa norma;
- tipologia, origine e nome del campione;
- modalità e data del campionamento;
- data di ricevimento e analisi del campione;
- risultati della ricerca;
- ragioni degli scostamenti nella procedura di determinazione dalle condizioni stabilite.
Introduzione………………………………2
1. Panoramica generale dei metodi per la determinazione delle vitamine…………………3
2. Metodi cromatografici per la determinazione delle vitamine…………5
3. Metodi elettrochimici per la determinazione delle vitamine…………10
4. Metodo di determinazione voltammetrico di stripping
vitamine idrosolubili B 1 B 2 nei prodotti alimentari………..13
Conclusione................................................................18
introduzione
Attualmente sul mercato è apparso un numero enorme di prodotti alimentari arricchiti per l'uomo e l'alimentazione animale, che sono miscele secche multicomponenti. La gamma di tali prodotti è piuttosto ampia. Si tratta innanzitutto di additivi alimentari biologicamente attivi, premiscele, mangimi per animali e uccelli e preparati multivitaminici. Un criterio per la qualità di tali prodotti può essere l'analisi del contenuto di vitamine e, in particolare, di quelle vitali come le vitamine idrosolubili e liposolubili, la cui quantità è regolata da documenti normativi e standard di qualità sanitaria.
Per determinare le vitamine vengono utilizzati vari metodi. I metodi ottici di analisi ampiamente utilizzati sono reagenti ad alta intensità di manodopera, tempo e costosi; l'uso dei metodi cromatografici è complicato dall'uso di apparecchiature costose. Ogni anno la gamma dei prodotti si amplia, la produzione alimentare aumenta e le ricette delle pappe vengono migliorate. Ciò, a sua volta, impone maggiori esigenze di monitoraggio della qualità dei prodotti e di miglioramento dei metodi per la determinazione delle vitamine. I requisiti medici e biologici e gli standard sanitari per la qualità delle materie prime alimentari e dei prodotti alimentari caratterizzano il valore nutrizionale della maggior parte dei tipi e gruppi di alimenti per l'infanzia per vari scopi.
1. Panoramica generale dei metodi per determinare le vitamine
Quasi tutte le vitamine sono facilmente soggette a ossidazione, isomerizzazione e vengono distrutte sotto l'influenza di alte temperature, luce, ossigeno atmosferico, umidità e altri fattori.
Tra i metodi esistenti per determinare la vitamina C (acido ascorbico), il metodo più utilizzato è la titolazione visiva e potenziometrica con una soluzione di 2,6-diclorofenolindofenolo secondo GOST 24556-81, basata sulle proprietà riducenti dell'acido ascorbico e sulla sua capacità ridurre il 2,6-DCPIP. Il colore blu scuro di questo indicatore diventa incolore quando viene aggiunto acido ascorbico. Importante è la preparazione di un estratto del prodotto in studio. Il miglior estraente è una soluzione al 6% di acido metafosforico, che inattiva l'ossidasi dell'acido ascorbico e fa precipitare le proteine.
Il carotene nei materiali vegetali, nei concentrati e nelle bevande analcoliche è controllato con il metodo fisico-chimico secondo GOST 8756.22-80. Il metodo si basa sulla determinazione fotometrica della frazione massica di carotene in una soluzione ottenuta durante l'estrazione da prodotti con un solvente organico. La soluzione viene prima purificata dalle sostanze coloranti associate mediante cromatografia su colonna. Il carotene si dissolve facilmente nei solventi organici (etere, benzina, ecc.) E conferisce loro un colore giallo. Per la determinazione quantitativa del carotene si utilizza la cromatografia ad adsorbimento su colonne con ossido di alluminio e ossido di magnesio. Questa determinazione dei pigmenti su una colonna dipende dall'attività dell'adsorbente, dalla quantità di pigmenti e dalla presenza di altri componenti nella miscela da separare. La miscela secca di ossido di alluminio trattiene il carotene e la miscela umida lascia entrare nella soluzione altre sostanze coloranti.
La tiamina si trova principalmente allo stato legato sotto forma di estere difosforico - cocarbossilasi, che è il gruppo attivo di numerosi enzimi. Con l'aiuto dell'idrolisi acida e sotto l'influenza degli enzimi, la tiamina viene rilasciata dal suo stato legato. Questo metodo determina la quantità di tiamina. Per calcolare il contenuto di vitamina B1 viene utilizzato il metodo fluorimetrico, utilizzato per determinare la tiamina nei prodotti alimentari. Si basa sulla capacità della tiamina di formarsi in ambiente alcalino con ferricanide calanio tiocromo, che conferisce un'intensa fluorescenza nell'alcol butilico. L'intensità del processo viene monitorata utilizzando un fluorimetro EF-ZM.
Negli alimenti e nelle bevande la riboflavina è presente allo stato legato, cioè sotto forma di esteri del fosforo legati alle proteine. Per determinare la quantità di riboflavina negli alimenti, è necessario liberarla dallo stato legato mediante idrolisi acida e trattamento con preparati enzimatici. La vitamina B1 nelle bevande analcoliche viene calcolata utilizzando un metodo chimico per determinare la quantità di forme di riboflavina facilmente idrolizzate e strettamente legate nei tessuti. Il metodo si basa sulla capacità della riboflavina di emettere fluorescenza prima e dopo la sua riduzione con iposolfito di sodio. Determinazione del contenuto totale di composti fenolici. Per questo viene utilizzato il metodo colorimetrico Folin-Denis, che si basa sulla formazione di complessi blu durante la riduzione dell'acido tungstico sotto l'azione dei polifenoli con un reagente in un mezzo alcalino. I composti fenolici vengono determinati mediante acido clorogenico mediante fotometria di fiamma su uno strumento EKF-2.
2. Metodi cromatografici per la determinazione delle vitamine
Recentemente, il metodo della cromatografia liquida ad alte prestazioni si è sviluppato rapidamente all'estero. Ciò è dovuto, innanzitutto, all'avvento dei cromatografi liquidi di precisione e al miglioramento delle tecniche di analisi. L'uso diffuso del metodo HPLC nella determinazione delle vitamine si riflette anche nel numero di pubblicazioni. Ad oggi, più della metà di tutti i lavori pubblicati sull'analisi delle vitamine idrosolubili e liposolubili sono dedicati all'uso di questo metodo e vari tipi di cromatografia si sono diffusi nella determinazione delle vitamine.
Per purificare il tocoferolo dalle impurità, viene utilizzata la cromatografia su strato sottile. In combinazione con metodi spettrofotometrici e fluorimetrici, questo metodo viene determinato quantitativamente anche la vitamina E. Durante la separazione, vengono utilizzate piastre con silufol, kieselgel
L'analisi degli isomeri del tocoferolo nell'olio di oliva viene effettuata mediante cromatografia gas-liquido. I metodi di analisi GC e GLC richiedono la preparazione di derivati volatili, cosa estremamente difficile nell'analisi delle vitamine liposolubili. Per questo motivo questi metodi di determinazione non sono ampiamente utilizzati. La determinazione della vitamina E in prodotti alimentari, prodotti farmaceutici e oggetti biologici viene effettuata in modalità gradiente e isocratica sia in condizioni di fase normale che di fase inversa. Come adsorbenti vengono utilizzati gel di silice (SG), farina fossile, silasorb, ODS-Hypersil e altri veicoli. Per il monitoraggio continuo della composizione dell'eluato nella cromatografia liquida durante l'analisi delle vitamine e l'aumento della sensibilità di determinazione, UV (A = 292 nm), spettrofotometrico (X = 295 nm), fluorescente (X = 280/325 nm), elettrochimico, I rilevatori utilizzati sono PMR e spettroscopico di massa.
La maggior parte dei ricercatori preferisce utilizzare la cromatografia ad adsorbimento per separare le miscele di tutti gli otto isomeri dei tocoferoli e dei loro acetati. In questi casi, la fase mobile è solitamente costituita da idrocarburi contenenti tracce di qualche etere. I metodi elencati per determinare la vitamina E, di norma, non prevedono la saponificazione preliminare dei campioni, il che riduce significativamente i tempi di analisi.
La separazione con contemporanea determinazione quantitativa del contenuto delle vitamine liposolubili (A, D, E, K) quando sono presenti insieme nei preparati multivitaminici viene effettuata sia in fase diretta che inversa. Tuttavia, la maggior parte dei ricercatori preferisce utilizzare la versione a fase inversa dell'HPLC. Il metodo HPLC consente di analizzare le vitamine idrosolubili B1 e B2 sia simultaneamente che separatamente. Per la separazione delle vitamine vengono utilizzate le versioni HPLC a fase inversa, a coppia ionica e a scambio ionico. Vengono utilizzate sia la modalità di cromatografia isocratica che quella a gradiente. La separazione preliminare degli analiti dalla matrice viene effettuata mediante idrolisi enzimatica e acida del campione.
Vantaggi del metodo della cromatografia liquida:
Rilevamento simultaneo di più componenti
Eliminazione dell'influenza dei componenti interferenti
Il complesso può essere rapidamente ricostruito per eseguire altre analisi.
Composizione e caratteristiche dell'attrezzatura e del software per il cromatografo liquido "Khromos ZH-301":
Tabella 1
Il termine “Vitamine” tradotto significa “ammine della vita”. Al giorno d'oggi esistono più di 30 sostanze di questo tipo e tutte sono di vitale importanza per il corpo umano, essendo parte di tutti i tessuti e le cellule, attivando e determinando il corso di molti processi.
Il fabbisogno di vitamine non è lo stesso e varia a seconda dell’età della vita, della malattia e delle condizioni meteorologiche di una persona. Il fabbisogno di vitamine aumenta durante la gravidanza, durante stress fisico e mentale, con iperfunzione della tiroide, insufficienza surrenalica e situazioni stressanti.
Va notato che anche l'ipervitaminizzazione, cioè un maggiore apporto di vitamine nel corpo umano, è sfavorevole per le funzioni metaboliche. Il sovradosaggio di vitamine si verifica principalmente quando si utilizzano preparati concentrati. La maggior parte delle vitamine entrano nel corpo umano dalle piante e una piccola parte dai prodotti animali. Più di 20 sostanze vitaminiche non possono essere sintetizzate nel corpo umano, mentre altre vengono sintetizzate negli organi interni, dove il fegato svolge un ruolo dominante.
Pertanto, scegliamo questo argomento per la nostra ricerca.
Infatti, ai nostri giorni, la salute umana e uno stile di vita sano stanno diventando sempre più una priorità. Oggigiorno vengono prodotti molti diversi additivi biologici (BAA), stimolanti e farmaci che aiutano a migliorare la salute.
Ma purtroppo dobbiamo ammettere che nelle catene di farmacie finiscono anche molti prodotti contraffatti e di bassa qualità. Dopo il traffico di armi e di droga, la falsificazione dei medicinali occupa un vergognoso terzo posto. Va notato che i preparati vitaminici e i complessi vitaminici non sono affatto prodotti economici, sono costosi. È stato interessante scoprire cosa si nasconde dietro le etichette dei farmaci venduti nelle farmacie della nostra città. Non possiamo condurre un’analisi qualitativa di tutti i farmaci; abbiamo bisogno di determinati reagenti, strumenti e tecniche. Come base per le nostre attività di ricerca, abbiamo utilizzato i metodi di analisi qualitativa di Kucherenko N. E., Severin S. E. per la determinazione delle vitamine.
Ipotesi: presumiamo che dietro le etichette dei preparati medicinali vitaminici non ci siano vitamine contraffatte, ma preparati naturali, poiché la salute dell'uomo e dei nostri abitanti dell'Amur ha il valore più alto.
Oggetto di studio: preparati vitaminici acquistati nelle farmacie cittadine.
Lo scopo del nostro lavoro: condurre un'analisi qualitativa delle vitamine acquistate nelle farmacie di Amursk e Komsomolsk-on-Amur.
In base all'argomento, sono stati impostati i seguenti compiti:
1. Conoscere le caratteristiche delle principali vitamine.
2. Condurre un'analisi qualitativa dei farmaci.
3. Confrontare i risultati ottenuti con l'avanzamento dello studio.
4. Trarre conclusioni.
Materiali e attrezzature: una serie di vitamine, reagenti chimici, metodi di analisi qualitativa Kucherenko N. E., Severina S. E. per determinare le vitamine.
1. Caratteristiche delle vitamine.
Affinché una persona sia forte e sana, ha bisogno di vitamine. Lo sappiamo tutti fin dalla prima infanzia. Ma raramente pensiamo a cosa siano queste sostanze: le vitamine. E quando ne parliamo immaginiamo semplicemente una scatola con confetti colorati o una ciotola di frutta. Una persona lontana dalla medicina ha bisogno di saperne di più sulle vitamine? Sì, è necessario, almeno per farlo
Riconosci ancora una volta quanto sia importante una dieta variata. Oggi anche i medici chiedono di scommettere non sui preparati vitaminici farmaceutici, ma su prodotti naturali ricchi di vitamine (frutta e verdura in primis, ma non solo). Quindi, cosa sono le vitamine e dove trovarle per le esigenze del corpo?
Le vitamine si formano attraverso la biosintesi nelle cellule e nei tessuti vegetali. La maggior parte di essi sono associati a trasportatori di proteine. Di solito nelle piante non si trovano in forma attiva, ma altamente organizzata e, secondo la ricerca, nella forma più adatta all'uso da parte dell'organismo, ovvero sotto forma di provitamine.
Le vitamine forniscono un uso economico e ottimale dei nutrienti essenziali da parte dell'organismo.
La mancanza di vitamine provoca gravi disturbi. Le forme latenti di carenza vitaminica non hanno manifestazioni e sintomi esterni luminosi. Spesso, tutto ciò di cui una persona si lamenta è stanchezza, riduzione delle prestazioni e debolezza generale. Anche per l'ipovitaminosi
Il corpo è meno resistente agli effetti di tutti i tipi di fattori avversi. Ci vuole più tempo per ripristinare le normali funzioni dopo una malattia ed è più soggetto a varie complicazioni.
Tutte le vitamine sono divise in due grandi gruppi: idrosolubili e liposolubili. Le vitamine idrosolubili comprendono tutte le vitamine del gruppo B, le vitamine PP, H, C, P e le vitamine liposolubili A, E, K, D.
Ora diamo uno sguardo più da vicino alle vitamine più famose.
Riboflavina (B2)
La riboflavina è una vitamina “della pelle”. È responsabile di mantenere la pelle sana, morbida e liscia. Inoltre, questa vitamina è necessaria per gli occhi (ad esempio, in caso di infiammazione degli occhi, si consiglia di assumere 3 mg di riboflavina 3 volte al giorno prima dei pasti).
La carenza di riboflavina provoca non solo malattie della pelle, ma anche disturbi digestivi, colite cronica e gastrite, malattie del sistema nervoso e debolezza generale e porta ad una diminuzione della resistenza dell'organismo alle infezioni.
Piridossina (B6)
Questa vitamina è molto importante per l'organismo, poiché contribuisce a un migliore assorbimento degli acidi grassi insaturi.
Inoltre, la piridossina è necessaria per la funzione muscolare: insieme al calcio, contribuisce al loro funzionamento efficace e al completo rilassamento. È stato stabilito che la carenza di piridossina può diventare un fattore che provoca lo sviluppo dell'otite media.
Acido ascorbico (vitamina C)
Questa vitamina svolge molte funzioni diverse nel corpo. I processi redox non possono verificarsi senza la sua partecipazione; aumenta l'elasticità e la forza dei vasi sanguigni, insieme alla vitamina A, protegge il corpo dalle infezioni, blocca le sostanze tossiche nel sangue ed è necessario per rafforzare denti e gengive.
Inoltre, per aumentare l’aspettativa di vita è necessario anche un apporto sufficiente di acido ascorbico, poiché è coinvolto nella creazione e nella guarigione del tessuto connettivo.
Non è difficile capire che la carenza di vitamina C è molto pericolosa. Nel frattempo, il corpo non ha la possibilità di immagazzinarlo per un uso futuro, quindi è necessario assumere regolarmente l'acido ascorbico (come parte del cibo e anche sotto forma di un farmaco). Non temere un sovradosaggio: la vitamina non è tossica e il suo eccesso viene facilmente escreto dagli organismi.
Acido nicotinico (PP)
Questa vitamina è coinvolta in molte reazioni ossidative. La sua carenza, spesso associata a una dieta monotona (ad esempio, quando si mangiano esclusivamente cereali), contribuisce allo sviluppo della pellagra.
Retinolo (vitamina A)
La vitamina A prolunga la giovinezza, normalizza il metabolismo, partecipa al processo di crescita e protegge la pelle e le mucose dai danni. Nel corpo degli animali e dell'uomo è formato dal carotene (la cosiddetta provitamina A).
Con una carenza di questa vitamina, la vista si deteriora, le condizioni della pelle cambiano (diventa secca, può apparire una piccola eruzione cutanea) e inizia un'intensa perdita di capelli.
Calciferolo (vitamina D)
I compiti principali della vitamina D nel corpo sono favorire l’assorbimento del calcio e regolare l’equilibrio fosforo-calcio. È attivamente coinvolto nel processo di formazione e crescita del tessuto osseo.
Inoltre, la vitamina D è necessaria per la normale coagulazione del sangue e la funzione cardiaca. È anche coinvolto nella regolazione dell'eccitabilità del sistema nervoso.
Anche se pochissimi alimenti contengono vitamina D, e anche in piccole quantità, la carenza di vitamina D non è molto comune. Il fatto è che il corpo può produrlo autonomamente sotto l’influenza dei raggi ultravioletti (ecco perché la vitamina D è anche chiamata “vitamina del sole”). Inoltre, per questo non è necessario prendere il sole per ore sotto i raggi cocenti del sole, è sufficiente uscire per qualche minuto al giorno durante le ore diurne.
A proposito, nel corpo delle persone dalla pelle chiara, la vitamina D si forma 2 volte più velocemente rispetto alle persone con la pelle scura.
Tocoferolo (vitamina E)
La vitamina E è conosciuta come la “vitamina della fertilità” perché è essenziale per la riproduzione. Inoltre, garantisce il normale funzionamento del muscolo cardiaco e previene la formazione di coaguli di sangue nei vasi sanguigni.
Recentemente, il tocoferolo è stato utilizzato efficacemente nel trattamento del diabete e dell’asma.
La vitamina E non è tossica, ma il suo contenuto in eccesso nel corpo porta ad un aumento della pressione sanguigna.
Il tocoferolo deve essere assunto solo in combinazione con il retinolo (vitamina A).
Rafforza la permeabilità delle pareti vascolari, riduce l'ossidazione dell'acido ascorbico e favorisce una migliore tolleranza alle situazioni di stress.
Ora che abbiamo imparato molto sul ruolo delle vitamine e sui loro benefici, sorge spontanea la domanda: “Dove puoi trovarle?” Questa domanda è tutt'altro che inattiva. Puoi consumare vitamine sintetiche farmaceutiche, ma gli esperti avvertono: tali vitamine non vengono sempre assorbite. E poi, perché ricorrere a mezzi artificiali se puoi ottenere vitamine direttamente dal cibo.
2. Descrizione dei farmaci.
Le vitamine sono sostanze essenziali per l'organismo, la cui presenza è di fondamentale importanza per il normale metabolismo e il mantenimento delle funzioni vitali in generale. Si tratta di composti a basso peso molecolare di natura organica. La maggior parte delle vitamine non vengono sintetizzate nel corpo umano e quindi il loro apporto tramite il cibo è estremamente importante. (L'eccezione è la vitamina D). Rispetto ai nutrienti essenziali, le vitamine devono essere fornite in dosi trascurabili. Allo stesso tempo, la carenza o l'assenza di una particolare vitamina provoca varie malattie e disturbi fisiologici.
1. Vitamina B 1 (tiamina)
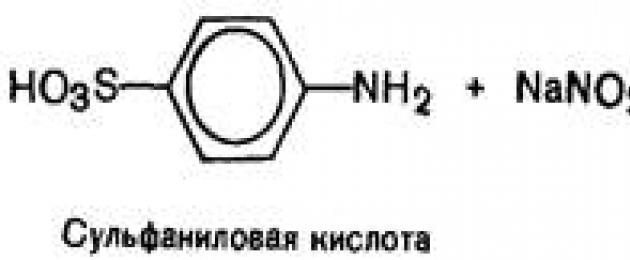
a) con diazo reagente
Principio del metodo. Innanzitutto si forma il diazobenzenesolfato (acido diazobenzenesolfonico):


Una soluzione di tiamina con l'aggiunta di diazobenzene solfato e alcali dà un composto colorato.
Progresso. Nella provetta vengono aggiunti in sequenza:
b) ossidazione a tiocromo
Principio del metodo. Quando esposta a K 3 Fe(CN) 6 in un mezzo alcalino, la tiamina viene ossidata in tiocromo giallo, che ha fluorescenza blu alla luce UV.

Progresso. 10 mg di bromuro di tiamina o cloruro di tiamina in polvere vengono sciolti in 5 ml di acqua, 1 ml di una soluzione al 5% di solfuro di ferro e potassio K 3 Fe(CN) 6 (ferriccianuro di potassio) e 1 ml di una soluzione al 10% di idrossido di sodio vengono aggiunti e mescolati. La metà del volume risultante viene riscaldata e si osserva un colore giallo come risultato della conversione della tiamina in tiocromo. Aggiungere all'altra metà 3 ml di alcool butilico o isoamilico, agitare bene e lasciare agire per qualche minuto. Lo strato superiore di alcol viene prelevato con un dispenser in un contenitore di vetro non fluorescente ed esaminato alla luce UV (o ai raggi di una lampada al quarzo al mercurio in una stanza buia). La fluorescenza blu è chiaramente visibile.
c) prendere lo spettro di assorbimento (modulo “spettrale”, range da 350 a 220 nm) e osservare il massimo a λ = 250-260 nm. Salvare il grafico, trasferirlo in Paint, quindi incollarlo nel file “Grafici” (documento Word), firmarlo e incollarlo nel report. ATTENZIONE! Prendi gli spettri di tutte le vitamine contemporaneamente per accendere e riscaldare lo spettrofotometro una sola volta. 
Spettro UV della tiamina cloridrato (8 μg/ml) in una soluzione di HCl allo 0,9%. Massimo a 246 nm.
2. Vitamina B2 (riboflavina)
a) con zinco metallico
Principio del metodo. La riboflavina viene ridotta dall'idrogeno liberato in leucoflavina incolore. C'è un cambiamento di colore dal giallo al verdastro, poi al cremisi, al rosa, e poi il colore scompare.

Progresso. 1 ml di una sospensione di riboflavina in acqua (soluzione 0,015 - 0,025%) viene versato in una provetta, vengono aggiunte 10 gocce di HCl concentrato e viene fatto cadere un pezzo di zinco metallico. Inizia il rapido rilascio di bolle di idrogeno e il liquido diventa gradualmente rosa o rosso, quindi il colore del liquido inizia a sbiadire e a scolorirsi (ossidazione inversa della leucoflavina in riboflavina).
b) con nitrato d'argento
Principio del metodo. Soluzioni neutre o leggermente acide di riboflavina (pH 6,5-7,2), reagendo con AgNO 3, danno un composto dai toni rosa-rossi. L'intensità del colore dipende dalla concentrazione della vitamina.
Progresso. A 1 ml di soluzione di riboflavina (0,015 - 0,025%) aggiungere 0,5 ml di soluzione AgNO 3 (0,1%). Appare un colore rosa.
c) fluorescenza negli UV + il suo spegnimento dopo l'aggiunta di SnCl 2 + Na 2 S 2 O 4, che attenuano la fluorescenza della vitamina stessa, ma non delle impurità. La fluorescenza della riboflavina è massima a pH 3,5-7,5. Registrare lo spettro in una soluzione di acetato di sodio.

Spettro UV della riboflavina (35 μg/ml) in soluzione di acetato di sodio CH 3 COONa
0,01%. Massimo a 266,5 nm. Picchi aggiuntivi a 223,0 nm, 373,5 nm e 444,5 nm.
3. Vitamina B5 (PP, acido nicotinico)

a) con acetato di rame
Principio del metodo. Quando l'acido nicotinico viene riscaldato con acetato di rame, si forma un precipitato di sale di rame dell'acido nicotinico.
Progresso. 5-10 mg di acido nicotinico vengono sciolti quando riscaldati in 10-20 gocce di una soluzione al 10% di acido acetico (o una soluzione allo 0,75% di acido nicotinico viene preparata in acqua calda, quindi 1 ml viene aggiunto a 2 ml di questo soluzione soluzione di aceto al 15%). A riscaldato fino al punto di ebollizione aggiungere alla soluzione un volume uguale di soluzione di acetato di rame al 5%. Il liquido diventa torbido bluastro e, dopo riposo e raffreddamento, precipita un precipitato blu di nicotinato di rame.

b) l'odore di piridina
Principio del metodo. Quando si riscalda l'acido nicotinico con Na 2 CO 3 anidro, si avverte un odore sgradevole di piridina.
Progresso. In un piccolo crogiolo di porcellana asciutto, mescolare 0,05 g di acido nicotina con 0,1-0,15 g di carbonato di sodio anidro e riscaldare. Appare un odore pungente di piridina.
4. Vitamina B6 (piridossina)

a) con cloruro ferrico
Principio del metodo. La vitamina B6 forma un complesso rosso sangue con cloruro ferrico.
Progresso. 4 ml di soluzione di piridossina allo 0,5-1% + 0,5 ml di FeCl 3 all'1% → agitare e osservare il colore rosso.
b) INOLTRE –

c) prendere uno spettro in NaOH 0,1 M (osservare i massimi a λ = 245 e 308 nm) o acqua (vedere figura).

Spettro UV della piridossina cloridrato (15 µg/ml) in acqua (pH≈6,0). Massimo a 291 nm.
5. Vitamina B12 – formalizziamolo in un report, ma in pratica non lo facciamo a causa dell'elevata tossicità del reagente attivo.
La vitamina B 12 reagisce con il cianuro a pH = 10 per formare dicianocobalamina viola, poiché il Co viene ossidato a 3-valente e la 5'-deossiadenosina viene sostituita dall'anione CN.
6. Vitamina P (usando la rutina come esempio)
Le sostanze con azione della vitamina P comprendono una serie di composti di natura fenolica, il cui principale effetto fisiologico è quello di ridurre la permeabilità e aumentare la forza dei capillari. Promuovono l'assorbimento della vitamina C nel corpo umano e animale, partecipano attivamente ai processi redox, hanno proprietà antiossidanti, inibendo, tra le altre cose, l'ossidazione dell'adrenalina. Inoltre inattivano l'enzima ialuronidasi, inibendo così la degradazione dell'acido ialuronico, un eteropolisaccaride nella sostanza fondamentale del tessuto connettivo. Vit. P inibisce l'attività della colinesterasi, della succinato deidrogenasi e di numerosi altri enzimi.

Numerosi flavonoli (rutina, quercetina), flavanoni, catechine, cumarine, acido gallico e suoi derivati, antociani (sostanze coloranti di frutti, bacche, fiori) hanno proprietà vitaminiche.
Molte sostanze della vitamina P sono glicosidi di flavonoli e flavanoni o agliconi (componenti non carboidrati dei glicosidi). Ad esempio, la rutina è un glicoside in cui il disaccaride rutinosi viene aggiunto un aglicone a struttura fenolica, il flavonolo quercetina.

a) con cloruro ferrico
b) con acido solforico
Principio: L'acido solforico concentrato forma sali di ossonio con flavoni (rutina), che sono gialli in soluzione. I flavanoni (ad esempio l'esperidina) conferiscono un colore cremisi con lo zolfo.
7. Vitamina C
a) qualitativamente - con K 3 Fe(CN) 6
Principio del metodo: riduzione del ferricianuro di potassio con vitamina C con viraggio al blu dovuto alla formazione del blu di Prussia.

Progresso. In due provette, mescolare 5 gocce di una soluzione al 5% di K 3 Fe(CN) 6 con 5 gocce di una soluzione all'1% di FeCl 3 . In una delle provette, aggiungere 20 gocce di una soluzione all'1% di acido ascorbico o succo di cavolo al liquido bruno-verdastro e all'altra la stessa quantità di acqua distillata. Il liquido nella prima provetta acquisisce un colore blu-verdastro e precipita un precipitato blu di blu di Prussia; nella seconda provetta (controllo) il colore bruno-verdastro del liquido rimane invariato.
- In contatto con 0
- Google+ 0
- OK 0
- Facebook 0