Lo shock è una forma di condizione critica del corpo, manifestata da disfunzione multiorgano, che si sviluppa a cascata sulla base di una crisi circolatoria generalizzata e, di regola, termina con la morte senza trattamento.
Il fattore shock è qualsiasi effetto sul corpo che supera in forza i meccanismi di adattamento. Durante lo shock, le funzioni della respirazione, del sistema cardiovascolare e dei reni cambiano, i processi di microcircolazione di organi e tessuti e i processi metabolici vengono interrotti.
Eziologia e patogenesi
Lo shock è una malattia di natura polietiologica. A seconda dell'eziologia dell'evento, i tipi di shock possono essere diversi.
1. Shock traumatico:
1) per lesioni meccaniche - fratture ossee, ferite, compressione dei tessuti molli, ecc.;
2) per ustioni (ustioni termiche e chimiche);
3) se esposto a basse temperature - shock da freddo;
4) in caso di lesioni elettriche – scossa elettrica.
2. Shock emorragico o ipovolemico:
1) si sviluppa a seguito di sanguinamento, perdita di sangue acuta;
2) a causa di un disturbo acuto dell'equilibrio idrico, si verifica la disidratazione del corpo.
3. Shock settico (batterico-tossico) (processi purulenti generalizzati causati da microflora gram-negativa o gram-positiva).
4. Shock anafilattico.
5. Shock cardiogeno (infarto del miocardio, arresto cordiaco acuto). Considerato nella sezione sulle condizioni di emergenza in cardiologia.
In tutti i tipi di shock, il principale meccanismo di sviluppo è la vasodilatazione e, di conseguenza, aumenta la capacità del letto vascolare, l'ipovolemia - il volume del sangue circolante (CBV) diminuisce, poiché ci sono vari fattori: perdita di sangue, ridistribuzione del fluido tra sangue e tessuti o discrepanza tra il volume normale del sangue e aumento della capacità del letto vascolare. La conseguente discrepanza tra il volume del sangue e la capacità del letto vascolare è alla base della diminuzione della gittata cardiaca e dei disturbi del microcircolo. Quest'ultimo porta a gravi cambiamenti nel corpo, poiché è qui che viene svolta la funzione principale della circolazione sanguigna: lo scambio di sostanze e ossigeno tra la cellula e il sangue. Si verifica un ispessimento del sangue, la sua viscosità aumenta e si verifica la microtrombosi intracapillare. Successivamente, le funzioni cellulari vengono interrotte fino alla morte. Nei tessuti, i processi anaerobici iniziano a prevalere su quelli aerobici, il che porta allo sviluppo di acidosi metabolica. L'accumulo di prodotti metabolici, principalmente acido lattico, aumenta l'acidosi.
Una caratteristica della patogenesi dello shock settico è una violazione della circolazione sanguigna sotto l'influenza di tossine batteriche, che contribuisce all'apertura degli shunt artero-venosi e il sangue inizia a bypassare il letto capillare e scorre dalle arteriole alle venule. A causa della diminuzione del flusso sanguigno capillare e dell'azione specifica delle tossine batteriche sulla cellula, la nutrizione cellulare viene interrotta, il che porta ad una diminuzione dell'apporto di ossigeno alle cellule.
Durante lo shock anafilattico, sotto l'influenza dell'istamina e di altre sostanze biologicamente attive, i capillari e le vene perdono il tono, mentre il letto vascolare periferico si espande, la sua capacità aumenta, il che porta alla ridistribuzione patologica del sangue. Il sangue inizia ad accumularsi nei capillari e nelle venule, causando disfunzione cardiaca. Il bcc risultante non corrisponde alla capacità del letto vascolare e la gittata cardiaca (gittata cardiaca) diminuisce di conseguenza. Il conseguente ristagno di sangue nel sistema microvascolare porta ad un disturbo del metabolismo e dell'ossigeno tra la cellula e il sangue a livello del letto capillare.
I processi di cui sopra portano all'ischemia del tessuto epatico e all'interruzione delle sue funzioni, che aggrava ulteriormente l'ipossia nelle fasi gravi dello sviluppo dello shock. La disintossicazione, la formazione di proteine, la formazione di glicogeno e altre funzioni del fegato vengono interrotte. Il disturbo del flusso sanguigno principale e regionale e della microcircolazione nel tessuto renale contribuisce all'interruzione delle funzioni di filtrazione e concentrazione dei reni con una diminuzione della diuresi dall'oliguria all'anuria, che porta all'accumulo di rifiuti azotati nel corpo del paziente , come urea, creatinina e altri prodotti metabolici tossici. Le funzioni della corteccia surrenale vengono interrotte, la sintesi dei corticosteroidi (glucocorticoidi, mineralcorticoidi, ormoni androgeni) è ridotta, il che aggrava i processi che si verificano. Un disturbo circolatorio nei polmoni spiega l'interruzione della respirazione esterna, la diminuzione dello scambio di gas alveolare, lo shunt del sangue, la formazione di microtrombosi e, di conseguenza, lo sviluppo di insufficienza respiratoria, che aggrava l'ipossia tissutale.
Clinica
Lo shock emorragico è la reazione del corpo alla conseguente perdita di sangue (la perdita del 25-30% del volume sanguigno porta a uno shock grave).
In caso di shock da ustione, il ruolo dominante è giocato dal fattore dolore e dalla massiccia perdita di plasma. Oliguria e anuria in rapido sviluppo. Lo sviluppo dello shock e la sua gravità sono caratterizzati dal volume e dalla velocità della perdita di sangue. In base a quest’ultimo si distingue lo shock emorragico compensato, lo shock reversibile scompensato e lo shock irreversibile scompensato.
Con shock compensato, si notano pelle pallida, sudore freddo e appiccicoso, il polso diventa piccolo e frequente, la pressione sanguigna rimane entro limiti normali o è leggermente ridotta, ma solo leggermente, e la minzione diminuisce.
Con shock reversibile non compensato, la pelle e le mucose diventano di colore cianotico, il paziente diventa letargico, il polso è piccolo e frequente, si osserva una significativa diminuzione della pressione arteriosa e venosa centrale, si sviluppa oliguria, l'indice di Algover aumenta e la L'ECG mostra un disturbo nell'apporto di ossigeno al miocardio. In caso di shock irreversibile, non c'è coscienza, la pressione sanguigna scende a livelli critici e potrebbe non essere rilevata, la pelle diventa color marmo e si sviluppa anuria (cessazione della minzione). L'indice Algover è alto.
Per valutare la gravità dello shock emorragico, è di grande importanza la determinazione del volume del sangue e del volume della perdita di sangue.
La mappa di analisi della gravità dello shock e la valutazione dei risultati ottenuti sono mostrati nella Tabella 4 e nella Tabella 5.
Tabella 4
Grafico di analisi della gravità dello shock
Tabella 5
Valutazione dei risultati in base al punteggio totale

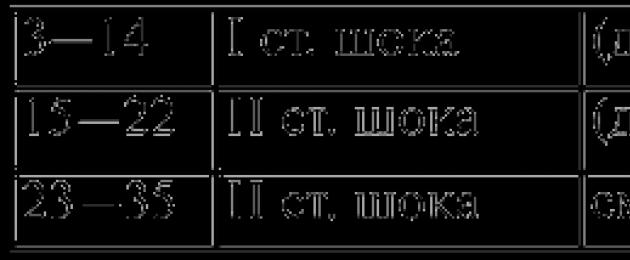
L'indice di shock, o indice Algover, rappresenta il rapporto tra la frequenza del polso e la pressione sistolica. In caso di shock di primo grado, l'indice Algover non supera 1. In caso di secondo grado - non più di 2; con un indice superiore a 2 la condizione è caratterizzata come incompatibile con la vita.
Tipi di shock
Shock anafilatticoè un complesso di varie reazioni allergiche di tipo immediato, che raggiungono un grado estremo di gravità.
Esistono le seguenti forme di shock anafilattico:
1) forma cardiovascolare, in cui si sviluppa insufficienza circolatoria acuta, manifestata da tachicardia, spesso con disturbi del ritmo cardiaco, fibrillazione ventricolare e atriale e diminuzione della pressione sanguigna;
2) forma respiratoria, accompagnata da insufficienza respiratoria acuta: mancanza di respiro, cianosi, respiro stridente e gorgogliante, rantoli umidi nei polmoni. Ciò è dovuto alla ridotta circolazione capillare, al gonfiore del tessuto polmonare, alla laringe, all'epiglottide;
3) forma cerebrale, causata da ipossia, alterata microcircolazione ed edema cerebrale.
In base alla gravità del decorso, ci sono 4 gradi di shock anafilattico.
Il grado I (lieve) è caratterizzato da prurito della pelle, comparsa di eruzioni cutanee, mal di testa, vertigini e sensazione di mal di testa.
II grado (moderato) – ai sintomi precedentemente menzionati si aggiungono l’edema di Quincke, la tachicardia, la diminuzione della pressione sanguigna e l’aumento dell’indice di Algover.
III grado (grave) si manifesta con perdita di coscienza, insufficienza respiratoria e cardiovascolare acuta (mancanza di respiro, cianosi, respiro sibilante, polso basso e rapido, forte diminuzione della pressione sanguigna, indice di Algover alto).
IV grado (estremamente grave) è accompagnato da perdita di coscienza, grave insufficienza cardiovascolare: il polso non è rilevabile, la pressione sanguigna è bassa.
Trattamento. Il trattamento viene effettuato secondo i principi generali del trattamento d'urto: ripristino dell'emodinamica, flusso sanguigno capillare, uso di vasocostrittori, normalizzazione del volume sanguigno e della microcircolazione.
Misure specifiche mirano a inattivare l'antigene nel corpo umano (ad esempio penicillinasi o b-lattamasi in stato di shock causato da antibiotici) o a prevenire l'effetto dell'antigene sul corpo - antistaminici e stabilizzatori di membrana.
1. Infusione endovenosa di adrenalina fino alla stabilizzazione emodinamica. È possibile utilizzare dopmin 10-15 mcg/kg/min e per i sintomi di broncospasmo e agonisti b-adrenergici: alupent, bricanil per via endovenosa.
2. Terapia per infusione in un volume di 2500–3000 ml con l'inclusione di poliglucina e reopoliglucina, a meno che la reazione non sia causata da questi farmaci. Bicarbonato di sodio 4% 400 ml, soluzioni di glucosio per ripristinare il volume sanguigno e l'emodinamica.
3. Stabilizzatori di membrana per via endovenosa: prednisolone fino a 600 mg, acido ascorbico 500 mg, troxevasina 5 ml, sodio etamilato 750 mg, citocromo C 30 mg (sono indicate le dosi giornaliere).
4. Broncodilatatori: aminofillina 240–480 mg, noshpa 2 ml, alupent (bricanil) 0,5 mg flebo.
5. Antistaminici: difenidramina 40 mg (suprastin 60 mg, tavegil 6 ml), cimetidina 200-400 mg per via endovenosa (sono indicate le dosi giornaliere).
6. Inibitori della proteasi: trasilolo 400mila unità, contrico 100mila unità.
Shock traumaticoè una condizione patologica e critica del corpo che si verifica in risposta a un infortunio, in cui le funzioni dei sistemi e degli organi vitali vengono interrotte e inibite. Durante lo shock traumatico si distinguono le fasi torpida ed erettile.
A seconda del momento in cui si verifica, lo shock può essere primario (1-2 ore) e secondario (più di 2 ore dopo l'infortunio).
Stadio erettile o fase di emergenza. La coscienza rimane, il paziente è pallido, irrequieto, euforico, inadeguato, può urlare, correre da qualche parte, scoppiare, ecc. In questa fase viene rilasciata l'adrenalina, grazie alla quale la pressione e il polso possono rimanere normali per un po '. La durata di questa fase varia da alcuni minuti e ore a diversi giorni. Ma nella maggior parte dei casi è di natura breve.
La fase torpida sostituisce la fase erettile, quando il paziente diventa letargico e adinamico, la pressione arteriosa diminuisce e compare la tachicardia. Le stime sulla gravità degli infortuni sono riportate nella Tabella 6.
Tabella 6
Valutazione del volume della gravità della lesione


Dopo aver calcolato i punti, il numero risultante viene moltiplicato per un coefficiente.
Appunti
1. Se ci sono infortuni non specificati nell'elenco del volume e della gravità dell'infortunio, viene assegnato un numero di punti a seconda del tipo di infortunio, la gravità corrispondente a uno di quelli elencati.
2. In presenza di malattie somatiche che riducono le funzioni adattative dell'organismo, la somma dei punti rilevata viene moltiplicata per un coefficiente da 1,2 a 2,0.
3. All'età di 50-60 anni, la somma dei punti viene moltiplicata per un fattore di 1,2, più vecchio - per 1,5.
Trattamento. Principali direzioni nel trattamento.
1. Eliminazione dell'azione dell'agente traumatico.
2. Eliminazione dell'ipovolemia.
3. Eliminazione dell'ipossia.
Il sollievo dal dolore viene effettuato somministrando analgesici e narcotici ed eseguendo blocchi. Ossigenoterapia, intubazione tracheale se necessaria. Rimborso perdite ematiche e bcc (plasma, sangue, reopoliglucina, poliglucina, eritromassa). Normalizzazione del metabolismo, quando si sviluppa acidosi metabolica, viene somministrato cloruro di calcio al 10% - 10 ml, cloruro di sodio al 10% - 20 ml, glucosio al 40% - 100 ml. Combattere la carenza vitaminica (vitamine del gruppo B, vitamina C).
Terapia ormonale con glucocorticosteroidi: prednisolone endovenoso 90 ml una volta e successivamente 60 ml ogni 10 ore.
Stimolazione del tono vascolare (mesaton, norepinefrina), ma solo quando il volume del sangue circolante viene reintegrato. Anche gli antistaminici (difenidramina, sibazon) sono coinvolti nella terapia antishock.
Shock emorragicoè una condizione di insufficienza cardiovascolare acuta che si sviluppa dopo la perdita di una quantità significativa di sangue e porta ad una diminuzione della perfusione degli organi vitali.
Eziologia: lesioni con danni ai grandi vasi, ulcere gastriche e duodenali acute, rottura di un aneurisma aortico, pancreatite emorragica, rottura della milza o del fegato, rottura di una tuba o gravidanza ectopica, presenza di lobuli placentari nell'utero, ecc.
In base ai dati clinici e all'entità del deficit di volume sanguigno, si distinguono i seguenti gradi di gravità.
1. Non espresso: nessun dato clinico, il livello di pressione sanguigna è normale. Il volume della perdita di sangue arriva fino al 10% (500 ml).
2. Debole - tachicardia minima, leggero calo della pressione sanguigna, alcuni segni di vasocostrizione periferica (mani e piedi freddi). Il volume della perdita di sangue varia dal 15 al 25% (750-1200 ml).
3. Moderato: tachicardia fino a 100-120 battiti al minuto, diminuzione della pressione del polso, pressione sistolica 90-100 mm Hg. Art., ansia, sudorazione, pallore, oliguria. Il volume della perdita di sangue varia dal 25 al 35% (1250-1750 ml).
4. Grave: tachicardia superiore a 120 battiti al minuto, pressione sistolica inferiore a 60 mm Hg. Art., spesso non rilevato dal tonometro, stupore, pallore estremo, estremità fredde, anuria. Il volume della perdita di sangue è superiore al 35% (più di 1750 ml). Gli esami di laboratorio hanno mostrato una diminuzione del livello di emoglobina, globuli rossi ed ematocrito in un esame del sangue generale. L'ECG rivela cambiamenti aspecifici nel segmento ST e nell'onda T, causati da un'insufficiente circolazione coronarica.
Trattamento lo shock emorragico prevede l'arresto del sanguinamento, l'uso della terapia infusionale per ripristinare il volume del sangue e l'uso di vasocostrittori o vasodilatatori, a seconda della situazione. La terapia infusionale prevede la somministrazione endovenosa di liquidi ed elettroliti in un volume di 4 litri (soluzione salina, glucosio, albumina, poliglucina). In caso di sanguinamento, è indicata la trasfusione di sangue e plasma dello stesso gruppo per un volume totale di almeno 4 dosi (1 dose corrisponde a 250 ml). È indicata la somministrazione di farmaci ormonali, come stabilizzatori di membrana (prednisolone 90-120 mg). A seconda dell'eziologia, viene effettuata una terapia specifica.
Shock settico– questa è la penetrazione di un agente infettivo dal suo focolaio originario nel sistema sanguigno e la sua diffusione in tutto il corpo. Gli agenti causali possono essere: batteri stafilococco, streptococco, pneumococco, meningococco ed enterococco, nonché Escherichia, Salmonella e Pseudomonas aeruginosa, ecc. Lo shock settico è accompagnato da disfunzione dei sistemi polmonare, epatico e renale, una violazione della coagulazione del sangue sistema, che porta alla comparsa della sindrome tromboemorragica (sindrome di Machabeli), che si sviluppa in tutti i casi di sepsi. Il decorso della sepsi è influenzato dal tipo di agente patogeno, questo è particolarmente importante con i moderni metodi di trattamento. I risultati di laboratorio indicano un'anemia progressiva (dovuta all'emolisi e all'inibizione dell'ematopoiesi). Leucocitosi fino a 12.109/l, tuttavia, nei casi più gravi, poiché si sviluppa una forte depressione degli organi emopoietici, si può osservare anche leucopenia.
Sintomi clinici dello shock batterico: brividi, febbre alta, ipotensione, pelle secca e calda - inizialmente, poi fredda e umida, pallore, cianosi, disturbi dello stato mentale, vomito, diarrea, oliguria. Caratteristica è la neutrofilia con uno spostamento della formula dei leucociti a sinistra fino ai mielociti; La VES aumenta a 30–60 mm/h o più. Il livello di bilirubina nel sangue aumenta (fino a 35–85 µmol/l), cosa che vale anche per il contenuto di azoto residuo nel sangue. La coagulazione del sangue e l'indice di protrombina sono ridotti (fino al 50-70%), i livelli di calcio e cloruro sono ridotti. Le proteine totali del sangue si riducono, il che avviene a causa dell'albumina, e il livello delle globuline (alfa-globuline e b-globuline) aumenta. L'urina contiene proteine, leucociti, globuli rossi e cilindri. Il livello di cloruro nelle urine diminuisce e il livello di urea e acido urico aumenta.
Trattamentoè principalmente di natura eziologica, pertanto, prima di prescrivere una terapia antibatterica, è necessario determinare l'agente patogeno e la sua sensibilità agli antibiotici. Gli agenti antimicrobici devono essere utilizzati alle dosi massime. Per trattare lo shock settico è necessario utilizzare antibiotici che coprano l'intero spettro dei microrganismi gram-negativi. La più razionale è l'associazione di ceftazidima e impinem, che si sono rivelate efficaci contro Pseudomonas aeruginosa. Farmaci come la clindamicina, il metronidazolo, la ticarcillina o l'imipinem vengono utilizzati come farmaci di scelta quando si verifica un agente patogeno resistente. Se gli stafilococchi vengono coltivati dal sangue, è imperativo iniziare il trattamento con farmaci a base di penicillina. Il trattamento dell'ipotensione consiste nella prima fase del trattamento nell'adeguatezza del volume del fluido intravascolare. Utilizzare soluzioni cristalloidi (soluzione isotonica di cloruro di sodio, lattato di Ringer) o colloidi (albumina, destrano, polivinilpirrolidone). Il vantaggio dei colloidi è che quando vengono introdotti, le pressioni di riempimento richieste vengono raggiunte più rapidamente e rimangono tali per lungo tempo. Se non vi è alcun effetto, vengono utilizzati il supporto inotropo e (o) i farmaci vasoattivi. La dopamina è il farmaco di scelta perché è un beta-agonista cardioselettivo. I corticosteroidi riducono la risposta complessiva alle endotossine, aiutano a ridurre la febbre e hanno un effetto emodinamico positivo. Prednisolone alla dose di 60k 90 mg al giorno.
Shock (inglese - colpo, spinta)- un processo patologico acuto e pericoloso per la vita che si verifica sotto l'influenza di un forte irritante per il corpo ed è caratterizzato da disturbi della circolazione centrale e periferica con una forte diminuzione dell'afflusso di sangue agli organi vitali. Ciò porta a gravi disturbi nel metabolismo cellulare, con conseguenti cambiamenti o perdita della normale funzione cellulare e, in casi estremi, la morte cellulare.
EZIOLOGIA E PATOGENESI
Molte malattie contribuiscono potenzialmente allo sviluppo dello shock e si possono distinguere i seguenti gruppi principali di cause della sua insorgenza:
1. Diminuzione primaria del volume sanguigno circolante (shock ipovolemico) - con sanguinamento, disidratazione, perdita di plasma dovuta a ustioni.
2. Compromissione dell'emodinamica periferica (ridistribuzione o shock vasogenico) - sepsi, anafilassi, intossicazione, insufficienza surrenalica acuta, shock neurogeno, shock traumatico.
3. Insufficienza cardiaca primaria (shock cardiogeno) - con aritmie, miocardite, insufficienza ventricolare sinistra acuta, infarto del miocardio.
4. Ostruzione del flusso sanguigno venoso o della gittata cardiaca (shock ostruttivo) - nelle malattie del pericardio, pneumotorace tensivo, embolia polmonare, embolia grassa e gassosa, ecc.
L'essenza dello shock è un'interruzione dello scambio di gas tra sangue e tessuti, seguita da ipossia e disturbi della microcircolazione. I principali collegamenti patogenetici dello shock sono causati da ipovolemia, insufficienza cardiovascolare, alterata circolazione tissutale a seguito di cambiamenti nella resistenza capillare e post-capillare, shunt del sangue, stasi capillare con aggregazione di elementi cellulari del sangue (sindrome del fango), aumento della permeabilità della parete vascolare e rigetto sanguigno. La compromissione della perfusione tissutale influisce negativamente su tutti gli organi e sistemi, ma il sistema nervoso centrale è particolarmente sensibile all'ipossia.
DIAGNOSTICA
Non esiste un’unica classificazione generalmente accettata dello shock in pediatria. Più spesso vengono presi in considerazione l'origine, la fase di sviluppo, il quadro clinico e la gravità dello shock.
Per origine si distinguono emorragico, disidratazione (anidremico), ustione, settico, tossico, anafilattico, traumatico, dolore endogeno, neurogeno, endocrino nell'insufficienza surrenalica acuta, cardiogeno, pleuropolmonare, shock post-trasfusionali, ecc.
Secondo le fasi di sviluppo dei disturbi circolatori periferici, sono indicati:
- fase precoce (compensata).
- fase di shock pronunciato c) fase tardiva (scompensata) di shock.
A seconda della gravità, lo shock può essere classificato come lieve, moderato o grave. Nella diagnosi dello shock di qualsiasi eziologia, vengono alla ribalta tecniche che consentono di valutare innanzitutto lo stato del sistema cardiovascolare e il tipo di emodinamica. All'aumentare del grado di shock, la frequenza cardiaca aumenta progressivamente (1° grado - del 20-40%, 2° grado - del 40-60%, 3° grado - del 60-100% o più rispetto alla norma) e diminuisce la pressione sanguigna ( 1o grado - diminuisce la pressione del polso, 2o grado - il valore della pressione arteriosa sistolica scende a 60-80 mmHg, è caratteristico il fenomeno del "tono continuo", 3o grado - la pressione arteriosa sistolica è inferiore a 60 mmHg o non determinata).
Lo shock di qualsiasi eziologia ha uno sviluppo graduale di disturbi circolatori periferici, allo stesso tempo, la loro gravità e durata possono essere molto diverse.
La fase precoce (compensata) dello shock si manifesta clinicamente in un bambino con tachicardia con pressione sanguigna normale o leggermente elevata, pelle pallida, estremità fredde, acrocianosi, lieve tachipnea e diuresi normale. Il bambino è cosciente, sono possibili stati di ansia ed eccitabilità psicomotoria, i riflessi sono rafforzati.
La fase di shock pronunciato (sottocompensato) è caratterizzata da una violazione della coscienza del bambino sotto forma di letargia, ovattamento, riflessi indeboliti, una significativa diminuzione della pressione sanguigna (60-80 mm Hg), grave tachicardia fino al 150% del norma di età, pallore grave e acrocianosi della pelle, polso filiforme, tachipnea superficiale più pronunciata, ipotermia, oliguria.
La fase tardiva (scompensata) dello shock è caratterizzata da una condizione estremamente grave, alterazione della coscienza fino allo sviluppo del coma, pallore della pelle con una tinta terrosa o cianosi diffusa della pelle e delle mucose, ipostasi, diminuzione critica del sangue pressione o sua incertezza (meno di 60 mm Hg), polso filiforme o sua assenza sui vasi periferici, respiro aritmico, anuria. Con l'ulteriore progressione del processo, si sviluppa il quadro clinico di uno stato atonale (fase terminale).
Talvolta la fase iniziale dello shock è di brevissima durata (forme gravi di shock anafilattico, forma fulminante di shock infettivo-tossico con infezione meningococcica, ecc.). E quindi la condizione viene diagnosticata nella fase di shock grave o scompensato. La fase precoce può manifestarsi in modo abbastanza completo e prolungato con l'origine vascolare dello shock, meno in presenza di ipovolemia primaria.
È sempre necessario prestare attenzione alla possibilità di scompenso circolatorio: pallore progressivo della pelle e delle mucose, sudore freddo e appiccicoso, estremità fredde, test di riempimento capillare positivo (dopo la pressione sull'unghia, il colore si ripristina normalmente dopo 2 s , e con un test positivo - più di 3 s, indica una circolazione periferica compromessa) o un sintomo positivo di una "macchia pallida" (più di 2 s), ipotensione arteriosa progressiva, un aumento dell'indice di shock Algover (il rapporto tra frequenza del polso alla pressione sistolica, che normalmente non supera 1 nei bambini di età superiore a 5 anni e 1,5 nei bambini di età inferiore a 5 anni), una progressiva diminuzione della diuresi.
Con grave insufficienza di perfusione, si può formare un'insufficienza multiorgano: danni simultanei o sequenziali ai sistemi vitali del corpo ("organi di shock" - sistema nervoso centrale, polmoni, reni, ghiandole surrenali, cuore, intestino, ecc.).
PRIMO SOCCORSO IN CASO DI SHOCK
1. Posizionare il paziente in posizione orizzontale con gli arti inferiori sollevati.
2. Garantire la pervietà del tratto respiratorio superiore: rimuovere i corpi estranei dall'orofaringe, gettare indietro la testa, rimuovere la mascella inferiore, aprire la bocca, stabilire una fornitura di ossigeno al 100% umidificato e riscaldato attraverso una maschera respiratoria o un catetere nasale.
3. Se possibile, ridurre o eliminare l’effetto di un fattore di shock significativo per lo sviluppo:
- per l'anafilassi: interrompere la somministrazione di farmaci; rimuovere la puntura dell'insetto; sopra il sito di iniezione o morso, applicare un laccio emostatico per un massimo di 25 minuti, iniettare nel sito di iniezione o nella lesione 0,3-0,5 ml di una soluzione di adrenalina allo 0,1% in 3-5 ml di soluzione salina, coprire il sito di iniezione con ghiaccio per 10 -15 minuti, quando se l'allergene entra attraverso la bocca, se le condizioni del paziente lo consentono, sciacquare lo stomaco, somministrare un lassativo, fare un clistere purificante, se gli allergeni entrano nel naso o negli occhi, sciacquare con acqua corrente;
- in caso di sanguinamento, interrompere l'emorragia esterna mediante tamponamento, bende, pinze emostatiche, bloccaggio di grandi arterie, un laccio emostatico con registrazione del tempo della sua applicazione;
- per la sindrome da dolore traumatico: immobilizzazione; analgesia per via endovenosa, intramuscolare con una soluzione di analgin al 50% alla dose di 0,1 ml/anno di vita o anche, se necessario, con una soluzione di promedolo all'1% alla dose di 0,1 ml/anno di vita, anestesia per inalazione - con ossido nitrico miscelato con ossigeno (2:1 o 1:1), oppure per via intramuscolare o endovenosa mediante somministrazione di 2-4 mg/kg Kalip-Sol;
- per pneumotorace tensivo - puntura pleurica.
4. Cateterizzazione delle vene centrali o periferiche per terapia infusionale intensiva, iniziando con l'introduzione di cristalloidi in un volume di 10-20 ml / kg (soluzioni di Ringer, cloruro di sodio allo 0,9%) e colloidi (reopoliglucina, poliglucina, albumina al 5%, Gecodez , gelatinolo , Gelofusin). La scelta dei farmaci, il loro rapporto, il volume di infusione e la velocità di somministrazione delle soluzioni è determinata dalla variante patogenetica dello shock e dalla natura della malattia di base. Per lo shock, le infusioni endovenose vengono effettuate finché il paziente non esce da questo stato o finché non compaiono segni minimi di congestione nella circolazione polmonare o sistemica. Per evitare un'eccessiva somministrazione di soluzioni, la pressione venosa centrale viene costantemente monitorata (normalmente il suo valore in mm H2O è pari a 30/35 + 5 x numero di anni di vita). Se è basso l'infusione continua, se è alto si interrompe. È obbligatorio anche il monitoraggio della pressione arteriosa e della diuresi.
5. In presenza di insufficienza surrenalica acuta, vengono prescritti ormoni:
Idrocortisone 10-40 mg/kg/giorno;
o prednisolone 2-10 mg/kg/die, con metà della dose giornaliera nella prima somministrazione e l'altra metà in modo uniforme durante la giornata.
6. In caso di ipoglicemia, somministrare per via endovenosa una soluzione di glucosio al 20-40% alla dose di 2 ml/kg.
7. In caso di ipotensione arteriosa refrattaria ed in presenza di acidosi metabolica, la sua correzione avviene con una soluzione di bicarbonato di sodio al 4% alla dose di 2 ml/kg sotto il controllo dello stato acido-base.
8. Terapia sintomatica (sedativi, anticonvulsivanti, antipiretici, antistaminici, emostatici, agenti antipiastrinici, ecc.).
9. Se necessario, supporto rianimatorio completo.
I pazienti con manifestazioni di shock devono essere ricoverati nel reparto di terapia intensiva, dove, tenendo conto dell'eziopatogenesi, la clinica effettuerà un ulteriore trattamento conservativo o chirurgico.
Shock anafilattico
Shock anafilattico- la manifestazione più grave di una reazione allergica immediata che si verifica all'introduzione di un allergene sullo sfondo della sensibilizzazione del corpo ed è caratterizzata da gravi disturbi della circolazione sanguigna, della respirazione e dell'attività del sistema nervoso centrale ed è veramente pericolosa per la vita.
Gli allergeni causalmente significativi per lo sviluppo dello shock arterioso nei bambini possono essere:
- farmaci (antibiotici, sulfamidici, anestetici locali, mezzi di contrasto radiopachi, antipiretici, eparina, streptochinasi, asparaginasi, espansori plasmatici - destrano, gelatina)
- proteine estranee (vaccini, sieri, sangue di donatori, plasma)
- estratti allergenici per diagnosi e trattamento;
- veleno di insetti, serpenti;
- alcuni prodotti alimentari (agrumi, frutta secca, ecc.);
- composti chimici;
- polline delle piante;
- raffreddando il corpo.
Sulla frequenza e sul tempo di sviluppo shock arterioso influenza la via di introduzione dell'allergene nel corpo. Nel caso della somministrazione parenterale dell'allergene, l'AS si osserva più spesso. La via di somministrazione endovenosa del farmaco è particolarmente pericolosa, sebbene lo sviluppo dell'AS sia del tutto possibile con qualsiasi possibilità che il farmaco entri nel corpo del bambino.
DIAGNOSTICA
Shock arterioso si sviluppa rapidamente, entro i primi 30 minuti (massimo fino a 4 ore) dal momento del contatto con l'allergene, e la gravità dello shock non dipende dalla dose dell'allergene. Nei casi più gravi, il collasso si sviluppa al momento del contatto con l'allergene.
Esistono cinque forme cliniche di shock arterioso:
1. Variante asfittica (asmatoide).- compaiono e aumentano debolezza, sensazione di costrizione al petto, mancanza d'aria, tosse persistente, mal di testa pulsante, dolore al cuore, paura. La pelle è nettamente pallida, poi cianotica. Schiuma alla bocca, soffocamento, mancanza di respiro espiratorio con respiro sibilante all'espirazione. Può svilupparsi angioedema del viso e di altre parti del corpo. In futuro, con la progressione dell'insufficienza respiratoria e l'aggiunta di sintomi di insufficienza surrenalica acuta, potrebbe verificarsi la morte.
2. Variante emodinamica (cardiovascolare).- compaiono e aumentano debolezza, tinnito, sudorazione abbondante, dolore anginoso nella zona del cuore. Aumentano il pallore della pelle e l'acrocianosi. La pressione sanguigna diminuisce progressivamente, il polso è filiforme, i suoni cardiaci sono nettamente indeboliti, in pochi minuti sono possibili aritmie cardiache, perdita di coscienza e convulsioni. Un esito letale può verificarsi con un aumento dell'insufficienza cardiovascolare.
3. Variante cerebrale- i sintomi neurologici e cerebrali focali aumentano rapidamente.
4. Opzione addominale- dolore addominale spastico diffuso, nausea, vomito, diarrea, sanguinamento gastrointestinale.
5. Opzione mista.
Il termine "shock", che significa colpo, shock, shock in inglese e francese, fu introdotto accidentalmente nel 1743 da un traduttore ora sconosciuto in inglese di un libro del consulente militare di Luigi XV Le Dran per descrivere la condizione dei pazienti dopo una ferita da arma da fuoco. . Fino ad ora questo termine è stato ampiamente utilizzato per descrivere lo stato emotivo di una persona esposta a fattori mentali inaspettati ed estremamente forti, senza implicare danni specifici agli organi o disturbi fisiologici. In relazione alla medicina clinica, significa shock una condizione critica caratterizzata da una forte diminuzione della perfusione degli organi, ipossia e disturbi metabolici. Questa sindrome si manifesta con ipotensione arteriosa, acidosi e deterioramento rapidamente progressivo delle funzioni dei sistemi vitali del corpo. Senza un trattamento adeguato, lo shock porta rapidamente alla morte.
I disturbi emodinamici acuti a breve termine possono essere un episodio transitorio quando si verifica una violazione del tono vascolare, causata di riflesso da dolore improvviso, paura, vista di sangue, senso di soffocamento o surriscaldamento, nonché aritmia cardiaca o ipotensione ortostatica dovuta ad anemia o ipotensione . Questo episodio si chiama crollo e nella maggior parte dei casi si risolve da solo senza trattamento. A causa di una diminuzione transitoria dell'afflusso di sangue al cervello, può svilupparsi svenimento- Perdita di coscienza di breve durata, spesso preceduta da sintomi neurovegetativi: debolezza muscolare, sudorazione, vertigini, nausea, oscuramento degli occhi e acufeni. Caratterizzato da pallore, bassa pressione sanguigna, bradicardia o tachicardia. La stessa cosa può verificarsi in persone sane a temperature ambiente elevate, poiché lo stress da calore porta ad una significativa dilatazione dei vasi cutanei e ad una diminuzione della pressione diastolica. I disturbi emodinamici più lunghi rappresentano sempre un pericolo per il corpo.
Causeshock
Lo shock si verifica quando il corpo è esposto a sostanze irritanti estremamente forti e può svilupparsi a seguito di varie malattie, lesioni e condizioni patologiche. A seconda della causa, si distinguono shock emorragico, traumatico, ustione, cardiogeno, settico, anafilattico, trasfusionale, neurogeno e altri tipi. Possono verificarsi anche forme miste di shock causate da una combinazione di diversi motivi. Tenendo conto della patogenesi dei cambiamenti che si verificano nel corpo e che richiedono determinate misure terapeutiche specifiche, si distinguono quattro tipi principali di shock
Shock ipovolemico si verifica con una significativa diminuzione del volume del sangue a causa di un sanguinamento massiccio o di una disidratazione e si manifesta con una forte diminuzione del ritorno venoso del sangue al cuore e una grave vasocostrizione periferica.
Shock cardiogenico si verifica con una forte diminuzione della gittata cardiaca a causa della ridotta contrattilità miocardica o di cambiamenti morfologici acuti nelle valvole cardiache e nel setto interventricolare. Si sviluppa con un bcc normale e si manifesta con un traboccamento del letto venoso e della circolazione polmonare.
Shock redistributivo manifestato con vasodilatazione, diminuzione della resistenza periferica totale, ritorno venoso del sangue al cuore e aumento della permeabilità della parete capillare.
Shock ostruttivo extracardiaco si verifica a causa di un'improvvisa ostruzione del flusso sanguigno. La gittata cardiaca diminuisce bruscamente nonostante il volume sanguigno, la contrattilità miocardica e il tono vascolare siano normali.
Patogenesi dello shock
Lo shock si basa su disturbi di perfusione generalizzati, che portano all'ipossia di organi e tessuti e disturbi del metabolismo cellulare ( riso. 15.2.). I disturbi circolatori sistemici sono una conseguenza della diminuzione della gittata cardiaca (CO) e dei cambiamenti nella resistenza vascolare.
I principali disturbi fisiologici che riducono l'efficace perfusione tissutale sono l'ipovolemia, l'insufficienza cardiaca, il tono vascolare compromesso e l'ostruzione dei grandi vasi. Con lo sviluppo acuto di queste condizioni, nell'organismo si sviluppa una “tempesta mediatrice” con l'attivazione dei sistemi neuro-umorali, il rilascio nella circolazione sistemica di grandi quantità di ormoni e citochine proinfiammatorie, che influenzano il tono vascolare, la permeabilità della parete vascolare. e CO. In questo caso, la perfusione di organi e tessuti viene bruscamente interrotta. I disturbi emodinamici acuti e gravi, indipendentemente dalle ragioni che li hanno causati, portano allo stesso tipo di quadro patologico. Si sviluppano gravi disturbi dell'emodinamica centrale, della circolazione capillare e un'interruzione critica della perfusione tissutale con ipossia tissutale, danno cellulare e disfunzione d'organo.
Disturbi emodinamici
Una bassa CO è una caratteristica precoce di molti tipi di shock, ad eccezione dello shock ridistributivo, in cui nelle fasi iniziali la gittata cardiaca può addirittura essere aumentata. La CO dipende dalla forza e dalla frequenza delle contrazioni miocardiche, dal ritorno del sangue venoso (precarico) e dalla resistenza vascolare periferica (postcarico). Le ragioni principali della diminuzione della CO durante lo shock sono l'ipovolemia, il deterioramento della funzione di pompaggio del cuore e l'aumento del tono arteriolare. Le caratteristiche fisiologiche dei vari tipi di shock sono presentate in tavolo 15.2.
In risposta ad una diminuzione della pressione sanguigna, aumenta l'attivazione dei sistemi adattivi. Innanzitutto, si verifica l'attivazione riflessa del sistema nervoso simpatico, quindi aumenta la sintesi delle catecolamine nelle ghiandole surrenali. Il contenuto di norepinefrina nel plasma aumenta di 5-10 volte e il livello di adrenalina aumenta di 50-100 volte. Ciò migliora la funzione contrattile del miocardio, aumenta l'attività cardiaca e provoca un restringimento selettivo dei letti venosi e arteriosi periferici e viscerali. La successiva attivazione del meccanismo renina-angiotensina porta ad una vasocostrizione ancora più pronunciata e al rilascio di aldosterone, che trattiene sale e acqua. Il rilascio dell'ormone antidiuretico riduce il volume dell'urina e ne aumenta la concentrazione.
In stato di shock, il vasospasmo periferico si sviluppa in modo non uniforme ed è particolarmente pronunciato nella pelle, negli organi addominali e nei reni, dove si verifica la diminuzione più pronunciata del flusso sanguigno. La pelle pallida e fresca osservata durante l'esame e il pallore dell'intestino con polso indebolito nei vasi mesenterici visibili durante l'intervento chirurgico sono chiari segni di vasospasmo periferico.
La costrizione dei vasi sanguigni del cuore e del cervello avviene in misura molto minore rispetto ad altre zone e questi organi ricevono sangue più a lungo di altri a causa della forte limitazione dell'afflusso di sangue ad altri organi e tessuti. I tassi metabolici del cuore e del cervello sono elevati e le loro riserve di substrati energetici sono estremamente basse, quindi questi organi non tollerano un'ischemia prolungata. La compensazione neuroendocrina di un paziente sotto shock è principalmente finalizzata a soddisfare i bisogni immediati degli organi vitali: cervello e cuore. Un flusso sanguigno sufficiente in questi organi è mantenuto da ulteriori meccanismi di autoregolazione finché la pressione sanguigna supera i 70 mmHg. Arte.
Centralizzazione della circolazione sanguigna- reazione compensatoria biologicamente appropriata. Nel periodo iniziale, salva la vita del paziente. È importante ricordare che le reazioni di shock iniziali sono reazioni di adattamento del corpo volte alla sopravvivenza in condizioni critiche, ma oltre un certo limite iniziano ad essere di natura patologica, portando a danni irreversibili ai tessuti e agli organi. La centralizzazione della circolazione sanguigna, che persiste per diverse ore, insieme alla protezione del cervello e del cuore, è irta di un pericolo mortale, sebbene più lontano. Questo pericolo risiede nel deterioramento della microcircolazione, nell'ipossia e nei disturbi metabolici negli organi e nei tessuti.
La correzione dei disturbi emodinamici centrali durante lo shock comprende una terapia infusionale intensiva mirata ad aumentare il volume del sangue, l'uso di farmaci che influenzano il tono vascolare e la contrattilità miocardica. Solo in caso di shock cardiogeno la terapia infusionale massiva è controindicata.
Violazioni mmicrocircolo e perfusione tissutale
Il sistema microvascolare (arteriole, capillari e venule) è l'anello più importante del sistema circolatorio nella fisiopatologia dello shock. È a questo livello che i nutrienti e l’ossigeno vengono forniti agli organi e ai tessuti e vengono rimossi anche i prodotti metabolici.
Lo spasmo in via di sviluppo delle arteriole e degli sfinteri precapillari durante lo shock porta ad una significativa diminuzione del numero di capillari funzionanti e ad un rallentamento della velocità del flusso sanguigno nei capillari perfusi, ischemia e ipossia tissutale. Un ulteriore deterioramento della perfusione tissutale può essere associato a patologia capillare secondaria. L'accumulo di ioni idrogeno, lattato e altri prodotti del metabolismo anaerobico porta ad una diminuzione del tono delle arteriole e degli sfinteri precapillari e ad una diminuzione ancora maggiore della pressione sanguigna sistemica. In questo caso le venule rimangono ristrette. In queste condizioni, i capillari si riempiono eccessivamente di sangue e l’albumina e la parte liquida del sangue lasciano intensamente il letto vascolare attraverso i pori nelle pareti dei capillari (“sindrome da perdita capillare”). L'ispessimento del sangue nel letto microcircolatorio porta ad un aumento della viscosità del sangue, mentre aumenta l'adesione dei leucociti attivati alle cellule endoteliali, i globuli rossi e altri elementi formati del sangue si uniscono e formano grandi aggregati, peculiari tappi, che peggiorano ulteriormente la microcircolazione fino a quando lo sviluppo della sindrome dei fanghi.
I vasi bloccati dall'accumulo di cellule del sangue vengono spenti dal flusso sanguigno. Si sviluppa la cosiddetta “deposizione patologica”, che riduce ulteriormente il bcc e la sua capacità di ossigeno e riduce il ritorno venoso del sangue al cuore e, di conseguenza, provoca un calo della CO e un ulteriore deterioramento della perfusione tissutale. L'acidosi, inoltre, riduce la sensibilità dei vasi sanguigni alle catecolamine, impedendone l'effetto vasocostrittore e porta all'atonia delle venule. Si chiude così un circolo vizioso. Un fattore decisivo nello sviluppo della fase irreversibile dello shock è considerato un cambiamento nel rapporto tra il tono degli sfinteri precapillari e delle venule.
Una conseguenza inevitabile del rallentamento del flusso sanguigno capillare è lo sviluppo della sindrome da ipercoagulazione. Ciò porta alla formazione di trombi intravascolari disseminati, che non solo aumentano i disturbi della circolazione capillare, ma causano anche lo sviluppo di necrosi focale e insufficienza multiorgano.
Il danno ischemico ai tessuti vitali porta costantemente a un danno secondario che mantiene e aggrava lo stato di shock. Il circolo vizioso che ne risulta può portare a un esito fatale.
Le manifestazioni cliniche di alterata perfusione tissutale sono pelle fredda, umida, pallida, cianotica o marmorizzata, prolungamento del tempo di riempimento capillare oltre 2 secondi, gradiente di temperatura superiore a 3 °C, oliguria (minzione inferiore a 25 ml/ora). Per determinare il tempo di riempimento capillare, spremere la punta della lamina ungueale o il cuscinetto del dito del piede o della mano per 2 secondi e misurare il tempo durante il quale l'area pallida riacquista il suo colore rosa. Nelle persone sane questo avviene immediatamente. Se la microcircolazione si deteriora, lo sbiancamento dura a lungo. Tali disturbi del microcircolo non sono specifici e sono una componente costante di qualsiasi tipo di shock e il grado della loro gravità determina la gravità e la prognosi dello shock. Anche i principi di trattamento dei disturbi del microcircolo non sono specifici e praticamente non differiscono per tutti i tipi di shock: eliminazione della vasocostrizione, emodiluizione, terapia anticoagulante, terapia disaggregante.
Disturbi metabolici
In condizioni di ridotta perfusione del letto capillare non è garantito un adeguato apporto di nutrienti ai tessuti, il che porta a disordini metabolici, disfunzione delle membrane cellulari e danni cellulari. Il metabolismo dei carboidrati, delle proteine e dei grassi viene interrotto e l'utilizzo delle normali fonti energetiche - glucosio e acidi grassi - viene fortemente inibito. In questo caso si verifica un catabolismo pronunciato delle proteine muscolari.
I disturbi metabolici più importanti durante lo shock sono la distruzione del glicogeno, una diminuzione della defosforilazione del glucosio nel citoplasma, una diminuzione della produzione di energia nei mitocondri, l'interruzione della pompa sodio-potassio della membrana cellulare con sviluppo di iperkaliemia, che può causare fibrillazione atriale e arresto cardiaco.
L'aumento dei livelli plasmatici di adrenalina, cortisolo e glucagone che si sviluppa durante lo shock e la soppressione della secrezione di insulina influenzano il metabolismo cellulare modificando l'uso dei substrati e la sintesi proteica. Questi effetti includono un aumento del tasso metabolico, un aumento della glicogenolisi e della gluconeogenesi. Una diminuzione dell’utilizzo del glucosio tissutale è quasi sempre accompagnata da iperglicemia. A sua volta, l'iperglicemia può portare ad una diminuzione del trasporto di ossigeno, all'interruzione dell'omeostasi acqua-elettrolita e alla glicosilazione delle molecole proteiche con una diminuzione della loro attività funzionale. Ulteriori effetti dannosi significativi dell’iperglicemia da stress durante lo shock contribuiscono all’approfondimento della disfunzione d’organo e richiedono una correzione tempestiva mantenendo la normoglicemia.
Sullo sfondo della crescente ipossia, i processi di ossidazione nei tessuti vengono interrotti, il loro metabolismo procede lungo il percorso anaerobico. Allo stesso tempo, i prodotti metabolici acidi si formano in quantità significative e si sviluppa l'acidosi metabolica. Il criterio per la disfunzione metabolica è un livello di pH nel sangue inferiore a 7,3, una carenza di basi superiore a 5,0 mEq/L e un aumento della concentrazione di acido lattico nel sangue superiore a 2 mEq/L.
Un ruolo importante nella patogenesi dello shock appartiene al disturbo del metabolismo del calcio, che penetra intensamente nel citoplasma delle cellule. Livelli elevati di calcio intracellulare aumentano la risposta infiammatoria, portando ad un’intensa sintesi di potenti mediatori della risposta infiammatoria sistemica (SIR). I mediatori dell'infiammazione svolgono un ruolo significativo nelle manifestazioni cliniche e nella progressione dello shock, nonché nello sviluppo delle complicanze successive. L’aumento della produzione e della distribuzione sistemica di questi mediatori può portare a danni cellulari irreversibili e ad un’elevata mortalità. L'uso dei calcioantagonisti migliora la sopravvivenza nei pazienti con vari tipi di shock.
L'azione delle citochine proinfiammatorie è accompagnata dal rilascio di enzimi lisosomiali e radicali liberi perossido, che causano ulteriori danni - la "sindrome delle cellule malate". L'iperglicemia e un aumento della concentrazione dei prodotti solubili di glicolisi, lipolisi e proteolisi portano allo sviluppo dell'iperosmolarità del liquido interstiziale, che provoca la transizione del fluido intracellulare nello spazio interstiziale, la disidratazione delle cellule e un ulteriore deterioramento del loro funzionamento. Pertanto, la disfunzione della membrana cellulare può rappresentare un percorso fisiopatologico comune per varie cause di shock. E sebbene gli esatti meccanismi della disfunzione della membrana cellulare non siano chiari, il modo migliore per eliminare i disturbi metabolici e prevenire l’irreversibilità dello shock è il rapido ripristino del bcc.
I mediatori infiammatori prodotti durante il danno cellulare contribuiscono a un’ulteriore interruzione della perfusione, che danneggia ulteriormente le cellule all’interno del sistema microvascolare. In questo modo si completa un circolo vizioso: una perfusione compromessa porta a un danno cellulare con lo sviluppo della sindrome da risposta infiammatoria sistemica, che a sua volta peggiora ulteriormente la perfusione tissutale e il metabolismo cellulare. Quando queste risposte sistemiche eccessive persistono per lungo tempo, diventano autonome e non possono essere invertite, si sviluppa la sindrome da insufficienza multiorgano.
Nello sviluppo di questi cambiamenti, il ruolo principale appartiene al fattore di necrosi tumorale (TNF), alle interlechine (IL-1, IL-6, IL-8), al fattore di attivazione piastrinica (PAF), ai leucotrieni (B4, C4, D4, E4 ), trombossano A2, prostaglandine (E2, E12), prostaciclina, interferone gamma. L'azione simultanea e multidirezionale dei fattori eziologici e dei mediatori attivati durante lo shock porta a danno endoteliale, interruzione del tono vascolare, permeabilità vascolare e disfunzione d'organo.
La persistenza o la progressione dello shock possono derivare da difetti di perfusione in corso, da danno cellulare o da una combinazione di entrambi. Poiché l’ossigeno è il substrato vitale più labile, il suo inadeguato apporto da parte del sistema circolatorio costituisce la base della patogenesi dello shock, e il ripristino tempestivo della perfusione e dell’ossigenazione dei tessuti spesso arresta completamente la progressione dello shock.
Pertanto, la patogenesi dello shock si basa su disturbi profondi e progressivi dell'emodinamica, del trasporto di ossigeno, della regolazione umorale e del metabolismo. L’interrelazione di questi disturbi può portare alla formazione di un circolo vizioso con il completo esaurimento delle capacità adattative del corpo. Prevenire lo sviluppo di questo circolo vizioso e ripristinare i meccanismi di autoregolazione dell'organismo è il compito principale della terapia intensiva per i pazienti con shock.
Fasi dello shock
Lo shock è un processo dinamico che inizia con l'azione del fattore aggressione, che porta a disturbi circolatori sistemici e, con il progredire dei disturbi, termina con danni irreversibili agli organi e morte del paziente. L'efficacia dei meccanismi compensatori, il grado delle manifestazioni cliniche e la reversibilità dei cambiamenti che si verificano consentono di distinguere una serie di fasi successive nello sviluppo dello shock.
Fase di preshock
Lo shock è solitamente preceduto da una moderata diminuzione della pressione arteriosa sistolica, non superiore a 20 mm Hg. Arte. dalla norma (o 40 mm Hg se il paziente soffre di ipertensione arteriosa), che stimola i barocettori del seno carotideo e dell'arco aortico e attiva i meccanismi compensatori del sistema circolatorio. La perfusione tissutale non è influenzata in modo significativo e il metabolismo cellulare rimane aerobico. Se cessa l'influenza del fattore aggressione, i meccanismi compensatori possono ripristinare l'omeostasi senza alcuna misura terapeutica.
Stadio iniziale (reversibile) dello shock
Questa fase di shock è caratterizzata da una diminuzione della pressione arteriosa sistolica al di sotto di 90 mmHg. Arte. , grave tachicardia, mancanza di respiro, oliguria e pelle fredda e umida. In questa fase, i meccanismi compensatori non sono in grado di mantenere un livello adeguato di CO e di soddisfare il fabbisogno di ossigeno di organi e tessuti. Il metabolismo diventa anaerobico, si sviluppa acidosi tissutale e compaiono segni di disfunzione d'organo. Un criterio importante per questa fase di shock è la reversibilità dei cambiamenti risultanti nell'emodinamica, nel metabolismo e nelle funzioni degli organi e una regressione abbastanza rapida dei disturbi sviluppati sotto l'influenza di una terapia adeguata.
Stadio intermedio (progressivo) dello shock
Questa è una situazione critica pericolosa per la vita con un livello di pressione sanguigna sistolica inferiore a 80 mmHg. Arte. e disfunzione d'organo pronunciata ma reversibile con trattamento intensivo immediato. Ciò richiede la ventilazione polmonare artificiale (ALV) e l'uso di farmaci adrenergici per correggere i disturbi emodinamici ed eliminare l'ipossia d'organo. L'ipotensione profonda prolungata porta ad un'ipossia cellulare generalizzata e ad un'interruzione critica dei processi biochimici, che diventano rapidamente irreversibili. Riguarda l'efficacia della terapia durante il primo cosiddetto "ora d'oro" dipende la vita del paziente.
Stadio refrattario (irreversibile) dello shock
Questo stadio è caratterizzato da gravi disturbi dell'emodinamica centrale e periferica, morte cellulare e insufficienza multiorgano. La terapia intensiva è inefficace, anche se le cause eziologiche vengono eliminate e la pressione arteriosa aumenta temporaneamente. La progressiva disfunzione multiorgano porta solitamente a danni irreversibili agli organi e morte.
Test diagnostici e monitoraggio dello shock
Lo shock non lascia tempo per una raccolta ordinata di informazioni e chiarimenti sulla diagnosi prima di iniziare il trattamento. La pressione arteriosa sistolica durante lo shock è molto spesso inferiore a 80 mmHg. Arte. , ma lo shock viene talvolta diagnosticato a pressione arteriosa sistolica più elevata se vi sono segni clinici di un netto deterioramento della perfusione degli organi: pelle fredda ricoperta di sudore viscido, cambiamenti dello stato mentale da confusione a coma, oligo- o anuria e insufficiente riempimento capillare cutaneo. La respirazione rapida durante lo shock di solito indica ipossia, acidosi metabolica e ipertermia, mentre l'ipoventilazione indica depressione del centro respiratorio o aumento della pressione intracranica.
I test diagnostici per lo shock comprendono anche un esame del sangue clinico, la determinazione di elettroliti, creatinina, parametri di coagulazione del sangue, gruppo sanguigno e fattore Rh, emogasanalisi, elettrocardiografia, ecocardiografia e radiografia del torace. Solo i dati raccolti con attenzione e interpretati correttamente aiutano a prendere le decisioni giuste.
Monitoring è un sistema per il monitoraggio delle funzioni vitali dell'organismo, in grado di avvisare rapidamente del verificarsi di situazioni minacciose. Ciò consente di iniziare il trattamento in tempo e prevenire lo sviluppo di complicanze. Per monitorare l'efficacia del trattamento d'urto è indicato il monitoraggio dei parametri emodinamici, dell'attività cardiaca, polmonare e renale. Il numero di parametri controllati deve essere ragionevole. Il monitoraggio dello shock deve necessariamente includere la registrazione dei seguenti indicatori:
- Pressione sanguigna, utilizzando la misurazione intraarteriosa se necessario;
- frequenza cardiaca (FC);
- intensità e profondità della respirazione;
- pressione venosa centrale (CVP);
- pressione di incuneamento dell'arteria polmonare (PAWP) in stato di shock grave e causa sconosciuta dello shock;
- diuresi;
- gas nel sangue ed elettroliti nel plasma.
Per approssimare la gravità dello shock, è possibile calcolare l'indice Algover-Burri o, come viene anche chiamato, l'indice di shock, il rapporto tra la frequenza cardiaca al minuto e il valore della pressione sanguigna sistolica. E più alto è questo indicatore, maggiore è il pericolo per la vita del paziente. L'incapacità di monitorare uno qualsiasi degli indicatori elencati rende difficile la corretta scelta della terapia e aumenta il rischio di sviluppare complicanze iatrogene.
Pressione venosa centrale
Una bassa pressione venosa centrale è un criterio indiretto di ipovolemia assoluta o indiretta e il suo aumento al di sopra di 12 cm di acqua. Arte. indica insufficienza cardiaca. Misurare la pressione venosa centrale e valutarne la risposta a un basso carico di liquidi aiuta a selezionare un regime di fluidoterapia e a determinare l’adeguatezza del supporto inotropo. Inizialmente, al paziente viene somministrata una dose di prova di liquido in 10 minuti: 200 ml con una CVP iniziale inferiore a 8 cm aq. Arte. ; 100 ml - con una pressione venosa centrale entro 8-10 cm aq. Arte. ; 50 ml - con pressione venosa centrale superiore a 10 cm aq. Arte. La reazione viene valutata in base alla regola “5 e 2 cm aq. Arte. ": se la pressione venosa centrale aumenta di oltre 5 cm, l'infusione viene interrotta e si decide la questione dell'opportunità di un supporto inotropo, poiché tale aumento indica una rottura del meccanismo di regolazione della contrattilità di Frank-Starling e indica insufficienza cardiaca. Se l'aumento della pressione venosa centrale è inferiore a 2 cm d'acqua. Arte. - ciò indica ipovolemia ed è un'indicazione per un'ulteriore rianimazione intensiva con liquidi senza la necessità di terapia inotropa. Aumento della pressione venosa centrale nell'intervallo tra 2 e 5 cm aq. Arte. richiede un'ulteriore terapia infusionale sotto il controllo dei parametri emodinamici.
Va sottolineato che la CVP è un indicatore inaffidabile della funzione ventricolare sinistra, poiché dipende principalmente dalla condizione del ventricolo destro, che può differire dalla condizione del sinistro. Informazioni più obiettive e più ampie sulle condizioni del cuore e dei polmoni vengono fornite monitorando l'emodinamica nella circolazione polmonare. Senza il suo utilizzo, il profilo emodinamico di un paziente in shock viene valutato in modo errato in più di un terzo dei casi. L'indicazione principale per la cateterizzazione dell'arteria polmonare in stato di shock è l'aumento della pressione venosa centrale durante la terapia infusionale. La risposta all'introduzione di un piccolo volume di fluido durante il monitoraggio dell'emodinamica nella circolazione polmonare viene valutata secondo la regola “7 e 3 mm Hg. Arte. "
Monitoraggio emodinamico nel circolo polmonare
Il monitoraggio invasivo della circolazione sanguigna nella circolazione polmonare viene eseguito utilizzando un catetere installato nell'arteria polmonare. A questo scopo viene solitamente utilizzato un catetere con un palloncino galleggiante all'estremità (Swan-Gans), che consente di misurare una serie di parametri:
- pressione nell'atrio destro, nel ventricolo destro, nell'arteria polmonare e nell'arteria polmonare, che riflette la pressione di riempimento del ventricolo sinistro;
- SV mediante metodo della termodiluizione;
- pressione parziale di ossigeno e saturazione di ossigeno dell'emoglobina nel sangue venoso misto.
La determinazione di questi parametri amplia significativamente le possibilità di monitoraggio e valutazione dell'efficacia della terapia emodinamica. Gli indicatori risultanti consentono:
- differenziare l'edema polmonare cardiogeno e non cardiogeno, identificare l'embolia polmonare e la rottura dei lembi della valvola mitrale;
- valutare il volume del sangue e lo stato del sistema cardiovascolare nei casi in cui il trattamento empirico è inefficace o è associato ad un aumento del rischio;
- regolare il volume e la velocità di infusione dei liquidi, le dosi di farmaci inotropi e vasodilatatori e il valore della pressione positiva di fine espirazione durante la ventilazione meccanica.
La ridotta saturazione di ossigeno del sangue venoso misto è sempre un indicatore precoce di gittata cardiaca inadeguata.
Diuresi
Una diminuzione della diuresi è il primo segno oggettivo di una diminuzione del volume sanguigno. Ai pazienti con shock deve essere installato un catetere urinario permanente per monitorare il volume e la velocità della minzione. Quando si effettua la terapia infusionale la diuresi deve essere di almeno 50 ml/ora. Durante l'intossicazione da alcol, lo shock può verificarsi senza oliguria, poiché l'etanolo inibisce la secrezione dell'ormone antidiuretico.
Lo shock è uno stato di estrema depressione del sistema circolatorio, a seguito del quale il flusso sanguigno diventa insufficiente per la normale ossigenazione, nutrizione e metabolismo dei tessuti.
5 tipi di shock:
1) shock ipovolemico
Cause: perdita di sangue e plasma; disturbi idrici ed elettrolitici
Se la perdita non supera i 500 ml non vi sono segni clinici, solo moderata tachicardia.
Perdite da 501 a 1200 ml – moderata tachicardia, moderata ipotensione, segno di vasocostrizione (pallore)
Perdite da 1201 a 1800 ml – polso fino a 120 battiti/min, ipotensione in aumento, pallore, paziente cosciente ma irrequieto
Perdite da 1801 a 3000 ml - tachicardia superiore a 170 battiti/min, pressione sistolica 60-70 mmHg, polso solo nei grandi vasi, il paziente è incosciente, pallido, freddo, bagnato, si osserva anuria.\
Per valutare la gravità dello stato di shock viene introdotto l’indice Algover (indice di shock):
HI = frequenza cardiaca\BP sist.
Normalmente, SI = 0,5 – 0,6 unità.
Gravità lieve – 0,8 unità
Grado medio – 0,9 – 1,2 unità
Grado grave – 1,3 o più unità
2) shock cardiogeno
Cause: infarto esteso, aneurisma ventricolare, rottura del setto interventricolare
Colpetto. meccanismi:
A) iposistolia – sindrome da bassa gittata cardiaca
B) deterioramento del metabolismo miocardico con necrosi estesa, forte diminuzione della gittata sistolica, significativa occlusione aterosclerotica dei vasi coronarici.
Clinicamente simile allo shock ipovolemico.
3) shock settico
Cause: infezioni generalizzate - aumento di lipopolisaccaridi e batteri estranei, il cui bersaglio è la microcircolazione. Inoltre, la comparsa di tossine batteriche porta alla sovrapproduzione delle proprie sostanze biologicamente attive e alla formazione di fase iperdinamica (1) shock settico: dilatazione dei vasi periferici, pressione sanguigna normale, polso rapido, ma buon riempimento.
Il paziente è roseo, la pelle è calda, la permeabilità vascolare aumenta nel tempo, quindi la parte liquida del sangue entra nei tessuti e il bcc diminuisce. Inizia la seconda fase - fase ipodinamica, clinicamente simile allo shock ipovolemico.
4) shock neurogeno (spinale).
Cause: lesione spinale, anestesia spinale, dilatazione acuta dello stomaco.
Patogenesi: si basa sulla perdita dell'innervazione simpatica del cuore e dei vasi sanguigni. Clinica: il paziente è sempre cosciente, bradicardia, pelle calda, ipotensione moderata.
5) shock traumatico
Cause: politraumi, ferite, sindrome compartimentale, ustioni, congelamento.
Meccanismi: dolore, tossiemia, perdita di sangue, ulteriore raffreddamento del corpo
Nella sindrome da schiacciamento e nelle lesioni massicce dei tessuti molli – tossiemia – insufficienza renale acuta
Per ustioni e congelamento – dolore, tossiemia e perdita di plasma – aumento della viscosità del sangue e insufficienza renale acuta
In caso di lesioni e ferite - ridistribuzione del sangue - diminuzione della gittata sistolica e del ritorno venoso
Fasi dello shock:
1) fase di eccitazione. Attivazione di tutte le funzioni del corpo, a breve termine: agitazione, tachicardia, ipertensione, mancanza di respiro
2) stadio torpido. A livello del sistema nervoso centrale si verifica un'inibizione diffusa. No: riflessi, coscienza, polso solo nei grandi vasi, pressione sanguigna inferiore a 60, il paziente è pallido, freddo, bagnato, anuria.
Qualsiasi shock è accompagnato da:
1) iperattivazione del legame endocrino
I recettori baro e volumetrici di tutti i vasi vengono attivati, il sistema ipotalamo-ipofisi-surrene viene attivato, SAS, vasopressina, aldosterone, RAAS lavorano a livello catabolico
Mirato a: mantenimento della resistenza periferica, ritenzione di liquidi per ricostituire il volume sanguigno, ridistribuzione del flusso sanguigno a favore degli organi vitali, iperglicemia per creare un pool energetico.
2) cambiamenti nel sistema circolatorio
Primario dal lato SSS:
Reazioni volte a compensare l'ipovolemia
Tachicardia, finalizzata al mantenimento del CIO
Spasmo dei vasi periferici e rilascio di sangue dal deposito
Centralizzazione della circolazione sanguigna
Idremia – ingresso di liquido interstiziale nel flusso sanguigno
Il tono arterioso cambia sotto l'influenza degli ormoni
Un aumento del tono arterioso porta ad un aumento della resistenza periferica e ad un aumento del carico pressorio sul FN - gradualmente la forza di contrazione inizia a diminuire
La gittata cardiaca dipende dalla forza e dalla velocità della contrazione, ma se la frequenza cardiaca è superiore a 170 battiti, ciò porta ad una forte diminuzione della gittata sistolica → praticamente nessun sangue entra nei vasi coronarici → disturbi metabolici nel miocardio → depressione tossica del miocardio (fattore di irreversibilità dello stato di shock)
3) disturbi microcircolatori
Associato ad un aumento del tono vascolare e alla centralizzazione della circolazione sanguigna. Verso la periferia, la velocità del flusso sanguigno inizia a diminuire → apertura delle anastomosi artero-venose, attraverso queste anastomosi il sangue arterioso, bypassando i capillari, viene scaricato nella parte venosa → devastazione della rete capillare → interruzione del metabolismo dei tessuti → aumento della formazione di sostanze biologicamente principi attivi → inizia la vasodilatazione e il flusso sanguigno, ma il flusso sanguigno sarà passivo e dipendente dalla pressione sanguigna.
Accumulo di BAS → paralisi vascolare, i capillari sono costantemente aperti, non rispondono agli stimoli, aumenta la permeabilità microvascolare, diminuisce la velocità del flusso sanguigno → sindrome DIC → formazione di trombi, il ritorno venoso diminuisce bruscamente, si verifica edema interstiziale, diminuisce BCC
4) disturbi metabolici
A causa dell'azione degli ormoni - iperglicemia. Sotto l'influenza di GCS e STH, l'esochinasi viene bloccata → il glucosio serve solo a nutrire gli organi vitali
Sotto l'influenza dell'ormone della crescita, dell'ACTH e dell'adrenalina, la lipolisi viene attivata con la formazione di acidi grassi liberi
Accumulo di endorfine ed encefaline → ipotensione e depressione tossica del miocardio. La riduzione del flusso sanguigno nel pancreas porta al rilascio di enzimi (tripsina e chemiotripsina), che coagulano le proteine endogene e danneggiano le membrane delle piccole cellule.
5) ipossia cellulare. Il flusso sanguigno nella ghiandola tiroidea diminuisce → diminuzione della secrezione di tiroxina → le cellule smettono di usare l'ossigeno → ipossia cellulare → aumento della permeabilità delle membrane cellulari → le cellule smettono di usare l'ossigeno → diminuzione dell'ATP → attivazione della glicolisi → aumento dell'osmolarità cellulare → edema cellulare e morte cellulare
6) endotossiemia. Accumulo di proprie sostanze biologicamente attive (lisosomi E) → spasmo dei vasi coronarici → ischemia → cambiamenti nella funzione cardiaca
Insufficienza multiorgano
1) stato funzionale iniziale
2) resistenza all'ipossia
Fegato. Promuove l'endotossiemia (il fegato stesso non è interessato)
Polmoni. Sviluppo della sindrome da distress respiratorio
Caratterizzato da:
A) attivazione delle proprietà adesive dell'endotelio dei vasi polmonari
B) aumentare la permeabilità dei vasi polmonari all'acqua e B
B) sviluppo della sindrome DIC
D) adesione dei neutrofili attivati all'endotelio vascolare, che porta allo sviluppo dell'infiammazione
Clinicamente: ipossiemia refrattaria, comparsa di scurimento a scaglie dei campi polmonari, diminuzione della compliance polmonare, ridotta elasticità del tessuto polmonare, ispessimento delle membrane alveolari → insufficienza respiratoria cronica
Stomaco: formazione di ulcere
Intestino – meno colpito (escl. shock settico)
VK Kulagin identifica le seguenti fasi:
1. Stadio nervoso: il nome sottolinea il ruolo principale del fattore nervoso nella fase iniziale dello shock.
2. Vascolare (i principali fattori patogenetici sono una diminuzione del volume del sangue circolante, la centralizzazione della circolazione sanguigna, i disturbi della microcircolazione con il successivo sviluppo dell'ipossia di molti tessuti).
3. Metabolico (i disturbi emodinamici sono accompagnati da disturbi metabolici che aggravano il corso del processo: acidosi metabolica, rilascio di vari enzimi dalle cellule, compresi gli enzimi lisosomiali, nei tessuti e nel sangue).
Le seguenti fasi di shock sono più comuni:
1) Stadio di shock compensato, eccitazione - erettile.
2) Stadio di shock scompensato, inibizione - torpido.
3) Stadio di shock termico, preagonale.
Durante la fase erettile si verifica un aumento della pressione sanguigna, un aumento della frequenza cardiaca e un flusso sanguigno accelerato. Il vasospasmo di molti organi periferici viene rilevato anche sullo sfondo dell'attivazione del flusso sanguigno negli organi vitali - centralizzazione della circolazione sanguigna. Lo stadio è più pronunciato nello shock traumatico e da ustione; nello shock anafilattico e trasfusionale è di breve durata.
Nello stadio torpido, la pressione sanguigna diminuisce e l’entità di questa diminuzione determina, insieme ad altri indicatori, la gravità dello shock. Una diminuzione della diuresi oraria a meno di 40 ml porta successivamente allo sviluppo di disturbi metabolici e quindi, al passaggio allo stadio successivo, disordini morfologici termici e irreversibili. Si basano su un'ipossia stagnante - anossia, che spesso diventa irreversibile.
2.1.1. Eziologia e patogenesi dello shock ipovolemico (HS)
Questo shock si sviluppa con un'estesa perdita di liquidi. La causa più comune di HS è la perdita acuta di sangue a seguito di lesioni o emorragie interne (da ulcera peptica, varici esofagee, aneurisma aortico). La perdita di sangue può essere evidente (ad esempio, con sangue nelle feci) o latente (ad esempio, con una gravidanza extrauterina).
Allo stesso tempo, l'HS può svilupparsi con grandi perdite non solo di sangue, ma anche di altri fluidi. In questi casi i sintomi non compaiono immediatamente, ma dopo alcune ore e sono accompagnati da un ispessimento del sangue. Il fluido può essere perso:
per ustioni termiche e chimiche massicce;
quando si accumula nella cavità addominale (peritonite).
con diarrea abbondante e vomito incontrollabile.
con l'urina in caso di diabete mellito e diabete insipido, insufficienza surrenalica e sovradosaggio di forti diuretici.
Oltre all'ipovolemia assoluta, esiste l'ipovolemia relativa, in cui può esserci abbastanza o anche molto sangue nei vasi, ma una parte minore di esso partecipa alla circolazione, e una parte maggiore si deposita (sequestrata) nel sangue. letti capillari e venosi. Questa situazione è tipica dello shock settico, anafilattico e, in una certa misura, cardiogeno, conferendo a tutti questi tipi di shock una certa somiglianza con lo shock ipovolemico, compreso lo shock emorragico.
Un adulto affronta facilmente la perdita del 10% del volume sanguigno circolante totale (TBV) utilizzando meccanismi per mantenere la pressione sanguigna, che includono principalmente la vasocostrizione sotto l'influenza delle catecolamine. Se, tuttavia, una persona perde rapidamente dal 20 al 25% del suo sangue circolante, i meccanismi di compensazione di solito non funzionano più completamente e si sviluppano sintomi di shock.
Nello shock emorragico si osservano i cambiamenti più sorprendenti nell'emodinamica.
Immediatamente dopo la perdita di sangue si attivano meccanismi compensatori volti al mantenimento della pressione arteriosa:
1) una diminuzione della gittata cardiaca (CO) è accompagnata da un aumento del tono arteriolare dovuto ad un aumento della sensibilità dei vasi periferici alle catecolamine e ad altri vasocostrittori;
2) i capillari si chiudono e il sangue comincia a defluire attraverso gli shunt arteriolo-venosi;
3) l'ischemia renale innesca la secrezione di renina, e attraverso di essa il sistema renina-angiotensina-aldosterone con ritenzione di sodio e acqua e aumento del BCC.
La vasocostrizione periferica (o spasmo delle arteriole), da un lato, mantiene la pressione sanguigna e, dall'altro, impedisce la perfusione dei tessuti. A questo proposito, l'ipossia si sviluppa nei tessuti e si accumulano sostanze che riducono il tono vascolare. Questi sono lattato, adenosina e molti altri prodotti intermedi. I microvasi, soprattutto quelli metabolici, sono pieni di sangue. Questo può essere considerato come una reazione compensatoria del corpo in risposta all'ipossia (per risolvere la carenza di ossigeno) nell'attuale situazione estrema. Di conseguenza, si sviluppa un ristagno venoso e molti liquidi lasciano la circolazione attiva e il flusso sanguigno si indebolisce. In questa fase tutti i microvasi muscolari perdono la sensibilità ai vasocostrittori.
La perfusione del cuore e del cervello viene mantenuta per il tempo più lungo, ma poi fallisce. Vasocostrizione. compensativo in sostanza, può causare necrosi ischemica dell'intestino o delle dita. Nel sangue appare un fattore di depressione miocardica, che indebolisce le contrazioni cardiache.
Oltre all'ipossia, l'endotossina dei batteri intestinali gram-negativi svolge un ruolo importante nella diminuzione del tono vascolare periferico in qualsiasi forma di shock. Se i disturbi della microcircolazione fossero associati solo all'acidosi metabolica, sarebbero eliminati relativamente facilmente dopo aver rimosso il corpo dall'ipossia. Ciò, tuttavia, non accade, perché oltre all'ipossia, una serie di mediatori "shockogenici" altamente attivi dei leucociti e dell'endotelio microvascolare, formati sotto l'influenza dell'endotossina, sono coinvolti nella dilatazione paralitica dei microvasi (vedi shock settico).
Il fatto è che qualsiasi shock è accompagnato da ischemia dell'intestino crasso. A sua volta, l’ischemia rende la parete intestinale permeabile alle endotossine, che entrano nel fegato attraverso il sistema della vena porta. In condizioni normali, quasi tutta l'endotossina viene depositata e neutralizzata nelle RES epatiche. Allo stesso tempo, durante lo shock, il fegato perde la capacità di catturare e neutralizzare l'endotossina. Quest'ultimo, bypassando il fegato, si riversa nella circolazione sistemica, collegandosi alla patogenesi dello shock.
- In contatto con 0
- Google+ 0
- OK 0
- Facebook 0