В организме человека она синтезируется в количестве, недостаточном для обеспечения нормальной жизнедеятельности, поэтому обязательно должна поступать с пищей. Для детей данная аминокислота является незаменимой.
Аминокислота гистидин входит в состав белков, поэтому называется протеиногенной. Она необходима для роста и развития всех органов и тканей, играет важную роль в синтезе гемоглобина – переносчика кислорода в крови, входит в активный центр многих ферментов, является предшественников важных соединений: гистамина, карнозина, ансерина.
Гистидин – гетероциклическая диаминомонокарбоновая аминокислота.
Молекула гистидина имеет один карбоксильный кислотный хвост, и две аминные головы, одна из которых включена в циклическое соединение. Имея две аминные головы, аминокислота обладает основными свойствами, т.е. в водном растворе сдвигает водородный показатель (рН) в щелочную сторону (>7). Аминокислота обладает высокогидрофильными свойствами, т.е. хорошо растворяется в воде. В глобулярных белках располагается преимущественно на поверхности.
Гистидин называют суперкатализатором по его значению в ферментативном катализе, т.к. он входит в активный центр многих ферментов.
Биологическая потребность .
Суточная потребность в гистидине составляет для взрослого человека 1,5-2 г., для грудных детей: 34 мг\кг. веса, т.е. 0,1 – 0,2 г.
Биосинтез гистидина
Биосинтез гистидина очень сложен, это каскад из 9 реакций, неудивительно, что организм предпочитает получить аминокислоту в готовом виде. Начальными соединениями для синтеза гистамина выступают: аденозин-трифосфорная кислота (АТФ) и 5-фосфорибозил-1-пирофосфат (ФРПФ).
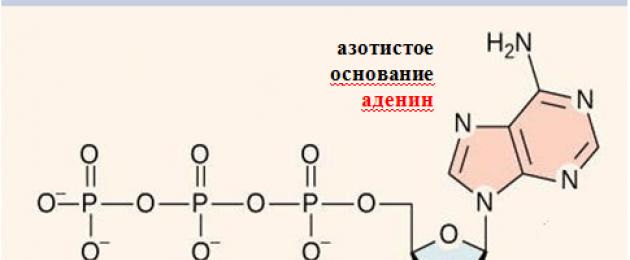
АТФ – это та горючка, на которой работает организм, соединение, поставляющее энергию. Она имеет сложное строение и состоит из пуринового основания аденина, пятичленного сахара рибозы и трех хвостов – остатков фосфорной кислоты.

5-фосфорибозил-1пирофосфат (ФРПФ) – соединение, образующееся из рибозо-5-фосфата, пятичленного сахара рибозы с присоединенным хвостом фосфорной кислоты. Рибоза-5-фосфат образуется, как конечный продукт пентозо-фосфатного цикла, каскада реакций превращения глюкозы – обычного сахара.

Рибозо-5-фосфат присоединяет к себе два фосфорных хвоста из молекулы АТФ и превращается в необходимый для синтеза гистидина 5-фосфорибозил-1-пирофосфат (ФРПФ). Таким образом, начальными продуктами синтеза являются: сахар глюкоза и 2 молекулы АТФ.
Синтез молекулы гистидина начался. Конвейер заработал. К молекуле 5-фосфорибозил -1- пирофосфата (ФРПФ) присоединяется молекула АТФ.

При этом от молекулы ФРПФ отрывается пирофосфатный хвост, а пуриновое ядро азотистого основания АТФ присоединяется к углероду пятичленного сахара рибозы в молекуле ФРПФ.
На втором этапе от образовавшегося монстра отщепляются еще два фосфорных остатка, которые на начальном этапе принадлежали АТФ.
Образуется соединение фосфорибозилАМФ.

Третий этап. Гидролиз, т.е. присоединение воды к пуриновому ядру, принадлежащему изначально молекуле АТФ. Углеродное кольцо разрывается, кислород воды присоединяется к углероду, а пара водородов отходит к соседним азотам, каждому по водороду, чтобы никому обидно не было.

Четвертый этап. Кольцо пятичленного сахара рибозы размыкается, колечко рибозы разворачивается, при этом отщепляется молекула воды.

На пятом этапе происходит метаморфоза. В реакцию вступает глутамин , который отдает азотистый остаток, а забирает гидроксильный остаток — ОН, превращаясь в глутаминовую кислоту (глутамат) .

Глутаминовая кислота и глутамин – два соединения, постоянно обменивающиеся азотными головами. Аммиак, образующийся при работе, захватывается глутаминовой кислотой, которая превращается в глутамин – транспортную форму переноса азотистой группы. Глутамин используется в разнообразных реакциях синтеза, вот и для образования имидазольного кольца гистидина пригодился.
Реакция обмена азотистой головой глутамина с глутаминовой кислотой выглядят так:

Соединение, идущее на синтез гистидина, перегруппировывается, от него отщепляется корона – рибонуклеотид — 5-аминоимидазол-4-карбоксамид – промежуточный продукт синтеза АТФ. На синтез АТФ оно и направится.

Другой продукт расщепления содержит пять атомов углерода из первоначального скелета сахара рибозы, один атом углерода и один атом азота, отщепленные от первоначально вступившей в реакцию молекулы АТФ, и один атом азота, принесенный глутамином. Одновременно замыкается имидазольное кольцо.
В результате получается заготовка для гистидина.
На шестом этапе отщепляется еще одна молекула воды
Седьмой этап: молекула глутаминовой кислоты жертвует свою аминную голову, превращаясь в α-кетоглутарат. Аминная голова глутаминовой кислоты (глутамата) приращивается к заготовке гистидина.
Соединение теряет фосфорный хвост, превращаясь в спирт
На заключительном этапе образовавшийся спирт окисляется молекулой НАД, и спирт превращается в аминокислоту.

Весь цикл превращения выглядит так:

Веществами – предшественниками для синтеза гистидина выступают:
- Глюкоза, которая в пентозо-фосфатном цикле превращается в фосфорибозил-пирофосфат (ФРПФ). Углеродный скелет сахара станет углеродным скелетом аминокислоты
- Две молекулы АТФ, одна жертвует фосфорным хвостом для синтеза ФРПФ, другая отдает пуриновое основание для синтеза имидазольного кольца гистидина
- Глутаминовая кислота, которая расходуется очень экономно: первоначально молекула глутаминовой кислоты захватывает аммиак, превращаясь в глутамин, необходимый для синтеза гистидина. В ходе реакции глутамин отдает азотную группу, вновь превращаясь в глутаминовую кислоту, которая может быть использована для дезаминирования, дабы отдать азотную группу заготовке гистидина.
- Две молекулы НАД для окисления спирта в аминокислоту.
Другая схема того же каскада реакций:

На всех этапах синтеза задействованы ферменты:
- АТФ-фосфорибозил трансфераза
- Пирофосфогидролаза
- Фосфорибозил АМФ циклогидролаза
- Фосфорибозил формимино-5-аминоимидазол-4-карбоксамид рибонуклеотид изомераза
- Глутамин амидо трансфераза
- Имидазолглицерол – 3 – фосфатдегидратаза
- Гистидинол фосфат амино трансфераза
- Гистидинол фосфат фосфатаза
- Гистидинол дегидрогеназа
Аминокислота гистидин является полузаменимой у взрослых и абсолютно незаменимой у детей, ибо выполняет в организме множество важных функций.
Биологическая потребность
Минимальная суточная потребность в гистидине для взрослого человека 12 мг\на 1 кг. массы тела, т.е. для человека, массой 60 кг. в сутки необходимо 0,7 г. Оптимальная суточная потребность для взрослого человека 1,5 — 2 г. Предельно-допустимая дозировка гистидина составляет 5-6 г.\сутки.
Для младенцев потребность в гистидине составляет 34 мг\кг. веса, т.е. 0,1 – 0,2 г.
Потребность в гистидине повышается при интенсивных физических нагрузках, в период восстановления после тяжелых травм, ранений, операций.
Содержание гистидина в продуктах питания
В тушеном мясе гистидина на 15-20% больше, чем в жареном и на 35-40% больше, чем в сыром
В приготовленной рыбе гистидина на 25-30% больше, чем в сырой
Белок растительных продуктов в среднем усваивается на 20% хуже, чем животного происхождения, а белок грибов лисичек усваивается лишь на 30%, в связи с чем были введены добавочные коэффициенты.
Для наилучшего сохранения аминокислоты в крупах и орехах, их следует хранить в герметично закрытых емкостях, защищенными от прямых солнечных лучей.
Крупы и бобовые потребляются не в сухом виде, а в виде каш, обычно соотношение зерна и воды в готовом блюде составляет 1:1 для бобовых и 1:2 для зерновых каш.
При обычном рационе достаточное количество гистидина можно получить из небольших порций мяса и рыбы – около 150 г. готового рыбного или мясного блюда содержат суточную норму аминокислоты. Сыра либо творога понадобится грамм 200-300, это вменяемая порция для ежесуточного потребления. Семечек, орехов потребуется 300 – 400 грамм, так что полным вегетарианцам следует задуматься: либо дефицит аминокислоты, либо серьезное превышение калоража, ибо эти продукты очень калорийны. Зерновые каши не могут рассматриваться в качестве основного источника гистидина, ибо 1,5 – 2 кг. каши под силу съесть лишь Гаргантюа либо человеку с серьезными физическими нагрузками. Так питались крестьяне в Средние века: большой объем зерновых с высоким калоражем компенсировался тяжелым трудом на земле.
Дефицит гистидина
В обычных условиях при нормальном питании дефицита гистидина у взрослых людей не наблюдается. Недостаточность гистидина возможна при экстремальных диетах или голодании, когда вынужденно или по своей воле люди отказываются от потребления белковых продуктов. Недостаток аминокислоты проявляется в мышечных болях, слабости. В костном мозгу перестают вырабатываться красные кровяные тельца (эритроциты), что ведет к анемии, а вот свертываемость крови повышается, что приводит к риску образованию тромбов. С дефицитом гистидина связано ухудшение слуха плоть до полного исчезновения. Резко снижается половое влечение, у мужчин может развиться эректильная дисфункция.
Развивается катаракта. Возможны заболевания желудка и двенадцатиперстной кишки. Снижается иммунитет, что приводит к бактериальным и вирусным инфекциям, повышается склонность к аллергиям, у детей возникает экзематозный дерматит: воспаление кожи с зудом, мокнутием, образованием корок.
Дети, лишенные грудного молока и при неадекватном вскармливании отстают в росте и развитии, вплоть до умственной отсталости.
Избыток гистидина
При обычном питании гистидин в организме не накапливается и симптомов избытка не наблюдается. Однако при употреблении фармакологических препаратов L-гистидина возможны побочные реакции,
Гистидин выводит из организма медь и цинк, избыток гистидина провоцирует аллергические реакции и приступы бронхиальной астмы, у мужчин он способен привести к преждевременной эякуляции.
Во избежание развития осложнений препараты гистидина можно применять лишь по клиническим показаниям под медицинским контролем.
Противопоказания
Препараты гистидина НЕ ПРИМЕНЯЮТ при наличии следующих состояний:
- Психические заболевания: биполярное расстройство, шизофрения, органические поражения головного мозга
- Аллергические заболевания, бронхиальная астма
- Артериальная гипотензия (низкое артериальное давление)
- Избыточный вес – гистидин способствует увеличению массы тела
- Беременность, лактация
- Хронические заболевания печени и почек
Побочные эффекты
При передозировке фармакологическими препаратами L-гистидина возможны следующие побочные эффекты:
- Аллергические реакции немедленного типа: отек Квинке, резкое падение артериального давления с потерей сознания (артериальный коллапс), анафилактический шок.
- Психические расстройства
Менее серьезные побочные эффекты, при которых следует снизить дозировку препарата:
- Со стороны желудочно-кишечного тракта: тошнота, рвота, диспепсия (нарушение переваривания в желудке)
- Со стороны центральной и периферической нервной системы: головная боль, головокружение, тремор (трясущиеся конечности), нарушения сознания, парестезии (ощущения «ползания мурашек», «покалывания иголок»)
- Со стороны вегетативной нервной системы: локальное повышение температуры (локальная гипертермия), жар, снижение артериального давления, спазм бронхов
- Аллергические реакции: кожная сыпь.
Заключение
Гистидин – важная и нужная аминокислота, потребность в которой удовлетворяется при обычном питании. Разнообразный рацион, включающий мясные, рыбные и молочные продукты даст необходимое и достаточное количество гистидина для полноценной жизни. Фармакологические препараты и биологические добавки L-гистидина могут употребляться для лечения заболеваний под контролем врачей, но не для общего оздоровления обычными людьми из-за рисков опасных осложнений и множества побочных эффектов.
Введение
| Тривиальное название | Гистидин / Histidine |
| Трехбуквенный код | His |
| Однобуквенный код | H |
| Название по IUPAC | L-α-амино-β-имидазолилпропионовая кислота |
| Структурная формула | |
| Брутто-формула | C₆H₉N₃O₂ |
| Молярная масса | 155,16 г/моль |
| Химические характеристики | гидрофильный, протонируемый, ароматический |
| PubChem CID | 6274 |
| Заменимость | Незаменимая |
| Кодируется | CAU и CAC |
 |
Гистидин представляет собой альфа-аминокислоту с имидазольной функциональной группой.
Гистидин был открыт немецким врачом Косселем Альбрехтом в 1896 году. Изначально полагалось,
что эта аминокислота незаменима только для младенцев, однако в ходе долгосрочных исследований
было установлено, что она также важна и для взрослых людей. Для человека суточная потребность
в гистидине 12 мг на кг веса.
Вместе с лизином и аргинином образует группу основных аминокислот. Входит в состав многих ферментов,
является предшественником в биосинтезе гистамина. В большом количестве содержится в гемоглобине.
Кольцо имидазола у гистидина является ароматическим при всех значениях рН. Оно содержит шесть
пи-электронов: четыре из двух двойных связей, и два из пары азота. Оно может формировать пи-связи,
однако это осложняется его положительным зарядом. При 280 нм оно не способно поглощать, однако в
нижней части УФ-диапазона оно поглощает даже больше, чем некоторые аминокислоты.
Гистидином богаты такие продукты как тунец, лосось, свиная вырезка, говяжье филе, куриные грудки,
соевые бобы, арахис, чечевица, сыр, рис, пшеница.
Было показано, что добавки гистидина вызывают быстрое выделение цинка у крыс при увеличении
скорости экскреции от 3 до 6 раз .
Биохимия
 |
Предшественником гистидина, как и триптофана, является фосфорибозилпирофосфат.
Путь синтеза гистидина пересекается с синтезом пуринов.
Имидазольная боковая цепь гистидина является общим координирующим лигандом в металлопротеинах и частью
каталитических центров у определенных ферментов. В каталитических триадах основный азот гистидина
используется для получения протона из серина, треонина или цистеина, и активации его в качестве нуклеофила.
Гистидин используется для быстрого трансфера протонов, абстрагируя протон с его основным азотом, и создавая
положительно заряженные промежуточные вещества, а затем используя другую молекулу, буфер, чтобы извлечь протон
из азотной кислоты. В карбоангидразе гистидинный протонный трансфер используется для быстрого транспортирования
протонов из цинк-связанной молекулы воды, чтобы быстро регенерировать активные формы фермента. Гистидин также
присутствует в гемоглобиновых спиралях Е и F. Гистидин помогает стабилизировать оксигемоглобин и дестабилизировать
CO-связанный гемоглобин. В результате, в гемоглобине связывание окиси углерода сильнее только лишь в 200 раз, по
сравнению с 20 000 раз в свободной геме.
Некоторые аминокислоты могут быть превращены в промежуточные соединения в цикле Кребса. Углероды из четырех
групп аминокислот образуют промежуточные вещества цикла – альфа-кетоглютарат (альфа-КТ), сукцинил-КоА, фумарат
и оксалоацетат. Аминокислоты, образующие альфа-КГ - глутамат, глутамин, пролин, аргинин и гистидин. Гистидин
преобразуется в формиминоглютамат (FIGLU).
Аминокислота является предшественником гистамина и биосинтеза карнозина.
 |
Гистидин входит в состав активных центров множества ферментов, является предшественником в биосинтезе гистамина (см. рис.2). Фермент гистидин аммиаклиазы преобразует гистидин в аммиак и уроканиновую кислоту. Недостаток этого фермента наблюдается при редком метаболическом расстройстве гистидинемии. В антинобактерии и нитчатых грибах, таких как Neurospora сrаssа, гистидин может быть преобразован в антиоксидант эрготионеин .
Основные функции
:
синтез белков;
поглощение ультрафиолетовых лучей и радиации;
производство красных и белых кровяных телец;
выработка гистамина;
выделение эпинефрина;
секреция желудочного сока;
антиатеросклеротическое,
гиполипидемическое действие;
выведение солей тяжелых металлов;
здоровье суставов.
Системы и органы
:
- органы ЖКТ;
- печень;
- надпочечники;
- костно-мышечная система;
- нервная система (миелиновые оболочки нервных клеток).
Последствия дефицита
:
- ослабление слуха;
- задержка умственного и физического развития;
- фибромиалгия.
Болезни
:
- гистидинемия.
Последствия избытка : Избыток гистидина может способствовать возникновению дефицита меди в организме.
 |
Имидазольная боковая цепь гистидина имеет рКа около 6,0.
Это означает, что при физиологически соответствующих значениях рН, относительно небольшие
изменения в рН могут изменять средний заряд цепи. При рН ниже 6 имидазольное кольцо является в
основном протонированным, как в уравнении Хендерсона-Хассельблаха. При протонировании кольцо
имидазола имеет две NH связи и положительный заряд. Положительный заряд равномерно распределяется
между двумя атомами азота.
На рис.3 представлена кривая титрования гистидина (файл Excel с вычислениями). Из кривой титрования следует, что остовная карбоксильная
группа имеет рК a1 =1,82, протонированная аминогруппа амидазола — рК a2 = 6,00, а
остовная протонированная аминогруппа — рК a3 =9,17. При рН = 7,58 гистидин
существует в виде биполярного иона (цвиттер-иона), когда суммарный электрический заряд молекулы равен 0. При
этом значении рН молекула гистидина электронейтральна. Такое значение рН называют изоэлектрической точкой
и обозначают рI. Изоэлектрическая точка рассчитывается как среднее арифметическое двух соседних значений рК a .
Для гистидина: рI= ½ *c(рК a2 + рК a3) = ½ * (6,00 + 9,17) = 7,58
.
На рис.4 показаны разные формы существования молекулы гистидина. Это стоит понимать так: при определенном рК a появляется соответствующая форма, и затем процент ее содержания постепенно увеличивается.
Белок-белковые контакты
Вы увидите (по порядку):
1) шаро-стержневая модель гистидина (до нажатия каких-либо кнопок)
2) общий вид пептидной связи на примере гистидина и глицина (PDB ID:1W4S, 198 и 199)(после нажатия "Запустить")
3) общий вид остовной водородной связи на примере гистидина и валина (PDB ID:1W4S, 974:A и 964:A) (после нажатия "Продолжить")
4) водородная связь с участием боковой цепи (PDB ID:5EC4, 119 и 100) (здесь и далее после следующих нажатий "Продолжить")
5) водородная связь с участием боковой цепи (PDB ID:5EC4, 93 и 72)
6) водородная связь с участием боковой цепи (PDB ID:5HBS, 48 и 63)
7) водородная связь с участием боковой цепи (PDB ID:5HBS, 137 и 135)
8) водородная связь с участием боковой цепи (PDB ID:5E9N, 219 и 284)
9) водородная связь с участием боковой цепи (PDB ID:3X2M, 112 и 14)
10) солевой мостик (PDB ID:1us0, 240 и 284)
11) солевой мостик (PDB ID:1US0, 187 и 185)
12) возможное стэкинг-взаимодействие (PDB ID:5E9N, 137 и 7)
13) возможное стэкинг-взаимодействие (PDB ID:5E9N, 10 и 50)
Гистидин способен образовывать не только водородные связи с участием остова, но и с участием боковой цепи. Кроме того, из-за
полярности молекулы возможно образование солевых мостиков с отрицательно заряженными аминокислотами (схематично
показаны желтым). Также ароматический гистидин может вступать в стэкинг-взаимодействия с другими ароматическими аминокислотами.
В гидрофобные взаимодействия гистидин не вступает из-за своей гидрофильности.
Белок–белковые взаимодействия лежат в основе многих физиологических процессов, связанных с ферментативной активностью и ее регуляцией,
электронным транспортом и др. Процесс образования комплекса двух белковых молекул в растворе можно условно разделить на несколько стадий:
1) свободная диффузия молекул в растворе на большом расстоянии от других макромолекул,
2) сближение макромолекул и их взаимная ориентация за счет дальнодействующих электростатических взаимодействий с образованием
предварительного (диффузионно-столкновительного) комплекса,
3) трансформация предварительного комплекса в финальный, т. е. в такую конфигурацию, в которой осуществляется биологическая
функция.
Альтернативно диффузионно-столкновительный комплекс может распасться без образования финального комплекса. При трансформации
предварительного комплекса в финальный происходят вытеснение молекул растворителя из белок-белкового интерфейса и конформационные
изменения самих макромолекул. Важную роль в этом процессе играют гидрофобные взаимодействия и образование водородных связей
и солевых мостиков .
Факторы, регулирующие белок-белковые взаимодействия:
ДНК-белковые контакты
 |
Устойчивость нуклеопротеидных комплексов обеспечивается нековалентным взаимодействием. У различных нуклеопротеидов
в обеспечение стабильности комплекса вносят вклад различные типы взаимодействий.
На рис. 5 показано взаимодействие гистидина и фосфатной группы остова ДНК. Это взаимодействие обусловленно
положительным зарядом гистидина. Было найдено множество подобных взаимодействий (все
образованы по единому принципу, поэтому смысла приводить их все нет).
Примечания и источники:
Работа выполнялась вместе с Тепловой Анастасией //
Гистидин // LifeBio.wiki.
Компьютерные исследования и моделирование, 2013, Т. 5 No 1 С. 47−64 // С.С.Хрущевa, А.М.Абатурова и другие // Моделирование белок-белковых взаимодействий с применением программного комплекса многочастичной броуновской динамики ProKSim.
Белок-белковые взаимодействия // Wikipedia.
Нуклеопротеиды //
Гистидин? Здоровое долголетие возможно только при условии правильного и сбалансированного питания. Чтобы все системы и органы работали правильно, в сутки мы должны получать большое количество полезных веществ. И в этом списке аминокислота гистидин занимает далеко не последнее место. Она необходима для протекания целого ряда биохимических процессов. Наверняка, многие не знают про огромную роль гистидина в жизнедеятельности организма. Поэтому предлагаем вам прочитать о полезных свойствах этого вещества. Также мы расскажем, как применяется эта аминокислота в спорте и медицине.
Гистидин в оптимальной природной форме и дозировке содержится в продуктах пчеловодства — таких как цветочная пыльца, маточное молочко и трутневый расплод, которые входят в состав многих натуральных витаминно-минеральных комплексов компании «Парафарм»: «Леветон П», «Элтон П», «Леветон Форте», «Апитонус П», «Остеомед», «Остео-Вит», «Эромакс», «Мемо-Вит» и «Кардиотон». Именно поэтому мы уделяем столько внимания каждому природному веществу, рассказывая о его важности и пользе для здорового организма.
Условно незаменимая аминокислота
гистидин: для печени и нервов
Гистидин – это аминокислота, о которой в научном мире до сих пор идут споры. Одни ученые утверждают, что в организме человека она не синтезируется, а потому должна регулярно поступать с пищей. Другие, напротив, приводят данные исследований, согласно которым, в небольших количествах это вещество может вырабатываться в теле. Поэтому все чаще гистидин вместе с аргинином относят в особую группу – «условно незаменимые аминокислоты» . Чуть реже встречается такое название как «полузаменимая аминокислота».
Так или иначе, но небольшие количества гистидина, которые организм вырабатывает самостоятельно, недостаточны для сохранения здоровья. Более того, у детей до года синтез этого вещества не происходит вообще. Поэтому нужно следить за своим питанием, стараясь разнообразить рацион.
Что собой представляет гистидин
В природе гистидин встречается часто – присутствует в большинстве живых организмов. Он является составляющей белка, а также находится и в свободном виде. В теле человека эта аминокислота также содержится в больших количествах. Это вещество относится к группе протеиногенных, а значит, необходимо для производства белка. В чистом виде гистидин представляет собой бесцветный порошок, который плавится при температуре 287 градусов (L-изомер). Данное соединение хорошо растворяется в воде, а плохо в этаноле. При декарбоксилировании в организме образуется гистамин. Для получения лекарств (латинское название — histidine) выделяют из гемоглобина и крови, а также синтезируют. Кстати, на сегодняшний день в мире производится более 200 тонн этого вещества в год.
Гистидин: история
важного научного открытия
История важного научного открытия произошла в конце 19 века, во время, когда в Европе химия развивалась очень активно. Известный немецкий физиолог и биохимик А. Коссель в 1896 году выделил из сернокислых гидролизатов стурина. В том же году швейцарский химик С. Хедин сумел получить L из других белков, причем он вел работу независимо от своего коллеги. Также большой вклад в изучение данного вещества внес В. Паули.
А. Коссель известен тем, что создал классический метод количественного выделения «гексоновых оснований», к которым помимо относятся такие аминокислоты как аргинин и лизин. Благодаря его достижениям позднее ученые выяснили, что белки имеют полипептидную природу. Также этот биохимик вел исследования клеточной биологии, изучал химический состав клеточного ядра, занимался выделением и описанием нуклеиновых кислот. За свою работу он был награжден Нобелевской премией по физиологии и медицине 10 декабря 1910 года.
Значение гистидина для организма.
«Кирпичик тела»
Несмотря на то что, это вещество мало известно широкому кругу людей, значение гистидина для организма велико. Не будет преувеличением назвать эту аминокислоту «кирпичиком тела». Во-первых, она участвует в синтезе белка, а, следовательно, помогает строить мышцы. Во-вторых, гистидин является частью многих ферментов, например, гастрина, который участвует в работе пищеварительной системы, улучшая усвоение ряда витаминов.
Также это соединение улучшает азотистый баланс в организме, помогает правильному функционированию печени. Немалую роль играет в работе иммунной системы — с его участием происходит формирование лейкоцитов и эритроцитов. Помимо этого в больших количествах он содержится в гемоглобине. Кроме того гистидин является компонентом для производства такого важного вещества как L-карнозин.
Еще организму гистидин нужен для синтеза гистамина, уникального гормона, который участвует в 23 основных физиологических функциях. К примеру, от его содержания в крови зависит сексуальное здоровье, как мужчин, так и женщин. Еще одна огромная заслуга гистамина – борьба с различными инфекциями. В последние годы ученые отмечают, что у многих людей в крови повышенное содержание гистамина, что вызвано такими заболеваниями как инфаркт, гипертония, ожирение, кариес и различные виды аллергии. Гистамин является медиатором аллергических реакций, расширяет мелкие кровеносные сосуды, сужает крупные. Медиаторы аллергии – это вещества, которые освобождаются из клеток или создаются в результате биохимических процессов в организме, необходимые для правильного протекания аллергической реакции.
При этом не стоит забывать и о других полезных свойствах :
- помогает расти маленьким детям;
- участвует в регуляции кислотности крови;
- избавляет от аллергии;
- помогает восстановиться после тяжелой болезни;
- способствует нормализации сна;
- необходим для формирования миелиновых оболочек нервных клеток;
- важен для нормальной работы сердечно-сосудистой системы.
Также он обладает адаптогенными свойствами, уменьшая воздействие на организм разрушительных факторов.
Что бывает при недостатке гистидина ?
Установлено, что при недостатке гистидина у детей замедляется рост и развитие. Для взрослых это состояние опасно тем, что может привести к ревматоидному артриту. Кроме того, при дефиците этой аминокислоты ухудшается восстановление травмированных участков тела, и поэтому восстановление после операций может затянуться. Помимо этого, проявляется еще один эффект – ухудшается состояние кожи и слизистой.
Врачи уверены, что недостаток в организме приводит болезням желудка и катаракте. Также ослабевает иммунная система , что особенно опасно для грудных детей. Зафиксированы случаи, когда малыши страдали от дерматита при недостатке в пище данной аминокислоты. Замечено, что при недостатке гистидина в организме люди жалуются на упадок сил. Помимо этого снижается либидо, ухудшается слух и развивается фибромиалгия. Можно назвать и другие симптомы дефицита :
- болезни Альцгеймера и Паркинсона;
- дефицит цинка;
- нарушения в речи;
- изменения походки;
- сниженная умственная активность;
- раздражительность;
- рассеянность;
- задержка полового созревания;
- атипичные аллергические реакции.
Нехватка в организме аминокислоты приводит к такому расстройству как гистединемия. Это редкое генетическое заболевание, в результате которого организм перестает вырабатывать фермент, расщепляющий гистидин. В этих случаях снижается умственное развитие, нарушаются речевая и двигательная функции.
Переизбыток аминокислоты
Побочные эффекты
Нужно сказать, что добиться переизбытка аминокислоты сложно, поскольку он хорошо усваивается организмом. Но запредельные дозы вещества могут привести к аллергическим реакциям, астматические проявлениям, а также сокращают время полового акта у мужчин. Здесь уместным будет сказать и про побочные эффекты , которые вызывают препараты :
- слабость;
- головная боль;
- нарушение сознания;
- диспепсия;
- тошнота;
- снижение артериального давления;
- дрожание рук;
- высыпания на коже.
При передозировке таким лекарством могут проявляться: коллапс, отек Квинке, анафилактический шок. Не рекомендуется употреблять эту аминокислоту больным бронхиальной астмой, артериальной гипертензией и органическими заболеваниями ЦНС.
Гистидин : вещество в спорте
Доказано, что гистидин принимает участие в синтезе белков. Поэтому мышцы растут и становятся крепкими, что немаловажно для спортсменов. Кроме того вызывает увеличение секреции соматотропина, который стимулирует рост хрящей, костей и мышц.
Также гистидин как вещество в спорте ценится, поскольку из него в организме синтезируется L-карнозин. Как известно, это сильный антиоксидант, который содержится в мозге и мышцах. Он повышает выносливость, предотвращая накопление продуктов распада. В частности, нейтрализует кислоту, которая вырабатывается во время интенсивного мышечного напряжения.
Помимо этого включают в различные спортивные пищевые добавки , которые применяются для роста мышц и восстановления после травм. Замечено, что он особенно эффективен при совместном приеме с бета-аланином, так усиливается взаимное действие аминокислот. Если употреблять в таком виде, можно улучшить результаты, как в силовых видах спорта, так и в легкой атлетике.
Данное вещество входит в состав витаминного комплекса «Леветон Форте». Этот препарат создан на основе трав и продуктов пчеловодства, помогает повысить выносливость и работоспособность.
Гистидин в медицине:
огромные перспективы
Благодаря своим многочисленным свойствам гистидин в медицине сегодня применяется повсеместно. Поскольку он входит в состав многих ферментов, то благотворно воздействует на печень. Также считается хорошим средством для лечения гепатита, помогает при артрите, крапивнице. Вот почему данное вещество является компонентом многих лекарств. В частности, гидрохлорид гистидина назначают как средство против язвенной болезни желудка и гепатита. Нередко аминокислота применяется как один из компонентов комплексного лечения атеросклероза.
В 1976 году советские ученые В.С. Якушев и Р. И. Лившиц провели ряд экспериментов на животных, в ходе которых установили, что ограничивает образование малонового диальдегида в тканях при экспериментальном инфаркте миокарда. Все это делает его перспективным для лечения сердечно-сосудистых заболеваний.
Стоит сказать, что перспективы у гистидина в медицине весьма значительные. В одном из недавних исследований ученые выяснили, что гистидин хорошо сочетается с . Медики уверены, что такая комбинация — прекрасное лекарство против ОРВИ и других простудных заболеваний. После ряда экспериментов выяснилось, что пациенты, принимавшие гистидин с цинком , выздоравливали намного быстрее. Стоит отметить, что данный микроэлемент улучшает усвоение аминокислоты. В свою очередь гистидин переносит цинк в клетки, повышая их работоспособность.
Также вещество применяется при радиационном воздействии и для выведения тяжелых металлов, используется как средство для лечения СПИДа. Помимо этого гистидин зарекомендовал себя в качестве лекарства от заболеваний почек.
В каких продуктах
содержится гистидин
Поскольку это , нам нужно получать ее постоянно. Восполнить запас этой аминокислоты в организме нетрудно, но далеко не все знают, в каких продуктах содержится гистидин . Назовем источники аминокислоты в пище животного происхождения:
- говядина;
- курица;
- рыба (лососевые, скумбрия, палтус);
- молочные продукты (йогурт, сметана);
В значительных количествах содержат это вещество и многие растительные продукты:
- арахис;
- чечевица;
- соевые бобы;
- рожь;
- пшеница;
- гречка;
- цветная капуста;
- картофель;
- грибы;
- бананы;
- дыня.
Суточная норма
аминокислоты
Чтобы знать, сколько продуктов нам употреблять в пищу, нужно знать о суточной норме аминокислоты гистидин. Итак, в день человеку необходимо 1,5-2 грамма данного вещества. Для правильного составления рациона можно пользоваться такой формулой: 10 мг аминокислоты на килограмм веса. Спортсмены, испытывающие значительные нагрузки и нуждающиеся в особой диете, могут принимать больше аминокислоты. Считается, что количество потребляемого с пищей гистидина не должно превышать 7-8 грамм в сутки. В то же время в некоторых источниках содержится информация, что терапевтическая доза данного соединения может доходить до 20 граммов.
Подводя итог нашим рассуждениям, можно сказать, что условно незаменимая аминокислота гистидин очень важна для здоровья. Кроме участия в образовании белков, она является важным компонентом многих ферментов. Также она помогает выполнять свои функции печени, иммунной системе и сердцу. Без этого «кирпичика тела» наша жизнь была бы невозможна.