Дистрофия – это патологический процесс, который является следствием нарушения обменных процессов, при этом происходит повреждение структур клетки и появление в клетках и тканях организма веществ, которые в норме не определяются.
Дистрофии классифицируются:
1) по масштабу распространенности процесса: местные (локализованные) и общие (генерализованные);
2) по причине возникновения: приобретенные и врожденные. Врожденные дистрофии имеют генетическую обусловленность заболевания.
Наследственные дистрофии развиваются вследствие нарушения обмена белков, углеводов, жиров, в этом случае имеет значение генетический недостаток того или иного фермента, который участвует в метаболизме белков, жиров или углеводов. В дальнейшем в тканях происходит накопление не до конца преобразованных продуктов углеводного, белкового, жирового обмена. Этот процесс может развиваться в различных тканях организма, но обязательно происходит поражение ткани центральной нервной системы. Такие заболевания получили название – болезни накоп-ления. Дети, имеющие данные заболевания, погибают на 1-ом году жизни. Чем больше недостаток необходимого фермента, тем быстрее происходит развитие болезни и тем раньше наступает смерть.
Дистрофии подразделяются:
1) по виду того обмена, который был нарушен: белковые, углеводные, жировые, минеральные, водные и т. д.;
2) по точке приложения (по локализации процесса): клеточные (паренхиматозные), неклеточные (мезенхимальные), которые развиваются в соединительной ткани, а также смешанные (наблюдаются и в паренхиме и в соединительной ткани).
Выделяют четыре патогенетических механизма.
1. Трансформация – это способность одних веществ преобразовываться в другие, имеющие сходное строение и состав. Например, данной способностью обладают углеводы, трансформируясь в жиры.
2. Инфильтрация – это способность клеток или тканей наполняться избыточным количеством разнообразных веществ. Существует два типа инфильтрации. Для инфильтрации первого типа характерно, что клетка, которая участвует в нормальной жизнедеятельности, получает избыточное количество какого-либо вещества. Через некоторое время наступает предел, когда клетка не может переработать, ассимилировать этот избыток. Для инфильтрации второго типа характерно понижение уровня жизнедеятельности клетки, в результате она не справляется даже с нормальным количеством вещества, поступающего в нее.
3. Декомпозиция – характеризуется распадом внутриклеточных и внутритканевых структур. Происходит распад белково-липидных комплексов, которые входят в состав мембран органелл. В мембране белки и липиды находятся в связанном состоянии, и поэтому они не видны. Но при распаде мембран они образуются в клетках и становятся заметными под микроскопом.
4. Извращенный синтез – происходит образование в клетке аномальных чужеродных веществ, которые при нормальном функционировании организма не образуются. Например, при амилоидной дистрофии в клетках происходит синтез аномального белка, из которого затем образуется амилоид. У больных хроническим алкоголизмом в клетках печени (гепатоцитах) начинает происходить синтез чужеродных белков, из которых в дальнейшем формируется так называемый алкогольный гиалин.
Для различных видов дистрофий характерно свое нарушение функции ткани. При дистрофии расстройство бывает двояким: количественным, со снижением функции, и качественным, с извращением функции, т. е. появляются черты, несвойственные нормальной клетке. Примером такой извращенной функции является появление в моче белка при заболеваниях почек, когда имеются дистрофические изменения почки, или изменения печеночных проб, появляющиеся при заболеваниях печени, а при заболеваниях сердца – изменение сердечных тонов.
Паренхиматозные дистрофии делятся на белковые, жировые и углеводные.
Белковая дистрофия – это дистрофия, при которой нарушается белковый обмен. Процесс дистрофии развивается внутри клетки. Среди белковых паренхиматозных дистрофий выделяют зернистую, гиалиново-капельную, гидропическую дистрофии.
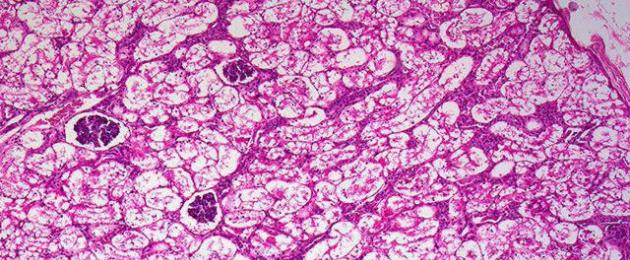
При зернистой дистрофии во время гистологического исследования в цитоплазме клеток можно увидеть белковые зерна. Зернистая дистрофия поражает паренхиматозные органы: почки, печень и сердце. Эта дистрофия получила название мутное или тусклое набухание. Это имеет связь с макроскопическими особенностями. Органы при данной дистрофии становятся слегка набухшими, а поверхность на разрезе смотрится тусклой, мутной, как бы «ошпаренная кипятком».
Способствует развитию зернистой дистрофии несколько причин, которые можно разделить на 2 группы: инфекции и интоксикации. Почка, пораженная зернистой дистрофией, увеличивается в размерах, становится дряблой, может быть определена положительная проба Шорра (при приведении друг к другу полюсов почки ткань почки рвется). На разрезе ткань тусклая, границы мозгового и коркового вещества смазаны или вообще могут быть неразличимы. При этом виде дистрофии поражается эпителий извитых канальцев почки. В нормальных канальцах почек наблюдаются ровные просветы, а при зернистой дистрофии апикальный отдел цитоплазмы подвергается разрушениям, и просвет становится звездчатой формы. В цитоплазме эпителия почечных канальцев находятся многочисленные зерна (розового цвета).
Почечная зернистая дистрофия заканчивается двумя вариантами. Благоприятный исход возможен при устранении причины, эпителий канальцев в данном случае возвращается к норме. Неблагоприятный исход наступает при продолжающемся воздействии патологического фактора – процесс становится необратимым, дистрофия преобразуется в некроз (часто наблюдается при отравлении почечными ядами).
Печень при зернистой дистрофии также немного увеличена. На разрезе ткань приобретает цвет глины. Гистологический признак зернистой дистрофии печени – непостоянное наличие белковых зерен. Необходимо обращать внимание – имеется или разрушена балочная структура. При этой дистрофии белки разделяются на отдельно располагающиеся группы или отдельно лежащие гепатоциты, что получило название дискомплексация печеночных балок.
Сердечная зернистая дистрофия: сердце внешне также слегка увеличено, миокард становится дряблым, на разрезе напоминает вареное мясо. Макроскопически белковых зерен не наблюдается.
При гистологическом исследовании критерием данной дистрофии является базофилия. Волокна миокарда различно воспринимают гематоксилин и эозин. Одни участки волокон интенсивно окрашиваются гематоксилином в сиреневый, а другие интенсивно красятся эозином в синий.
Гиалиново-капельная дистрофия развивается в почках (поражается эпителий извитых канальцев). Встречается при таких заболеваниях почек, как хронический гломерулонефрит, хронический пиелонефрит, при отравлениях. В цитоплазме клеток образуются капли гиалиноподобного вещества. Такая дистрофия характеризуется значительным нарушением почечной фильтрации.
Гидропическая дистрофия может встречаться в печеночных клетках при вирусных гепатитах. При этом в гепатоцитах образуются крупные светлые капли, часто заполняющие клетку.
Жировая дистрофия . Существует 2 вида жиров. Количество подвижных (лабильных) жиров меняется на протяжении всей жизни человека, они локализуются в жировых депо. Стабильные (неподвижные) жиры включены в состав клеточных структур, мем-бран.
Жиры осуществляют самые разнообразные функции – опорную, защитную и т. д.
Жиры определяются при помощью специальных красителей:
1) судан-III обладает способностью окрашивать жир в оранжево-красный цвет;
2) шарлах окрашивает в красный цвет;
3) судан-IV (осмиевая кислота) окрашивает жир в черный цвет;
4) нильская голубая имеет метахромазию: она окрашивает нейтральные жиры в красный, а все остальные жиры под ее воздействием приобретают синий или голубой цвет.
Непосредственно перед окрашиванием исходный материал обрабатывают при помощи двух способов: первый – спиртовая проводка, второй – замораживание. Для определения жиров используется замораживание срезов тканей, так как жиры растворяются в спиртах.
Нарушения жирового обмена представляют собой три патологии:
1) собственно жировая дистрофия (клеточная, паренхиматозная);
2) общее ожирение или тучность;
3) ожирение межуточного вещества стенок кровеносных сосудов (аорты и ее ветвей).
Собственно жировая дистрофия лежит в основе атеросклероза. Причины жировой дистрофии можно разделить на две основные группы: инфекции и интоксикации. В наше время основным видом хронической интоксикации является алкогольная интоксикация. Нередко могут наблюдаться медикаментозные интоксикации, эндокринные интоксикации – развивающиеся при сахарном диабете.
Примером инфекции, которая провоцирует жировую дистрофию, является дифтерия, так как дифтерийный токсин может вызывать жировую дистрофию миокарда. Жировая дистрофия наблюдается в тех же органах, что и белковая – в печени, почках и миокарде.
При жировой дистрофии происходит увеличение печени в размерах, она становится плотной, на срезе – тусклая, ярко-желтого цвета. Такой вид печени получил образное название «гусиная печень».
Микроскопические проявления: в цитоплазме гепатоцитов появляются жировые капли мелких, средних и крупных размеров. Как правило, они располагаются в центре печеночной дольки, но могут занимать ее всю.
В процессе ожирения выделяют несколько стадий:
1) простое ожирение, когда капля занимает весь гепатоцит, но при прекращении воздействия патологического фактора (когда пациент прекращает употреблять алкоголь), через 2 недели печень возвращается к нормальным показателям;
2) некроз – вокруг очага некроза возникает инфильтрация лейкоцитов как ответная реакция на повреждение; процесс на данной стадии является обратимым;
3) фиброз – рубцевание; процесс переходит в необратимую цирротическую стадию.
Происходит увеличение сердца, мышца становится дряблой, тусклой и, если внимательно осмотреть эндокард, под эндокардом папиллярных мышц можно наблюдать поперечную исчерченность, которая называется «тигровое сердце».
Микроскопическая характеристика: жир имеется в цитоплазме кардиомиоцитов. Процесс имеет мозаичный характер – патологическое поражение распространяется на кардиомиоциты, расположенные вдоль мелких вен. Исход может быть благоприятным, когда происходит возвращение к норме (если устранить причину), а если причина продолжает воздействовать, то наступает гибель клетки, и на ее месте происходит формирование рубца.
В почках жир локализуется в эпителии извитых канальцев. Такая дистрофия встречается при хронических заболеваниях почек (нефриты, амилоидоз), при отравлениях, общем ожирении.
При ожирении нарушается обмен нейтральных лабильных жиров, которые в избытке образуются в жировых депо; значительно увеличивается масса тела в результате накопления жира в подкожной жировой клетчатке, в сальнике, брыжейке, в паранефральной, забрюшинной клетчатке, в клетчатке, покрывающей сердце. При ожирении сердце становится как бы закупорен-ным толстой жировой массой, а затем происходит проникновение жира в толщу миокарда, что вызывает ее жировое перерождение. Мышечные волокна претерпевают давление ожиревшей стромы и атрофируются, что приводит к развитию сердечной недостаточности. Чаще всего поражается толща правого желудочка, в результате этого в большом круге кровообращения развиваются застойные явления. Помимо этого, ожирение сердца может закончиться разрывом миокарда. В литературных источниках такое ожиревшее сердце характеризуется как синдром Пиквика.
В печени при ожирении жир может образовываться внутри клеток. Печень приобретает вид «гусиной печени», как и при дистрофии. Дифференцировать образовавшийся жир в клетках печени можно с помощью цветного окрашивания: нильский голубой обладает способностью окрашивать нейтральный жир при ожирении в красный цвет, а при развившейся дистрофии – в синий.
Ожирение межуточного вещества стенок кровеносных сосудов (имеется в виду обмен холестерина): при инфильтрации из плазмы крови в уже подготовленную сосудистую стенку происходит поступление холестерина, который затем откладывается на сосудистой стенке. Часть его вымывается обратно, а часть перерабатывается макрофагами. Макрофаги, нагруженные жиром, получили название ксантомные клетки. Над отложениями жира происходит разрастание соединительной ткани, которая выпячивается в просвет сосуда, таким образом образуется атеросклеротическая бляшка.
Причины ожирения:
1) генетически обусловленные;
2) эндокринные (диабет, болезнь Иценко-Кушинга);
3) гиподинамия;
4) переедание.
Углеводная дистрофия может быть связана с нарушением обмена гликогена или гликопротеидов. Нарушение содержания гликогена проявляется в уменьшении или увеличении его количества в тканях и появлении там, где он обычно не выявляется. Эти нарушения выражены при сахарном диабете, а также при наследственных углеводных дистрофиях – гликогенозах.
При сахарном диабете происходит недостаточное потребление глюкозы тканями, увеличение ее количества в крови (гипергликемия) и выведение с мочой (глюкозурия). Тканевые запасы гликогена резко уменьшаются. В печени происходит нарушение синтеза гликогена, что приводит к инфильтрации ее жирами – возникает жировая дистрофия печени. При этом в ядрах гепатоцитов появляются включения гликогена, они становятся светлыми («дырчатые» и «пустые» ядра). При глюкозурии в почках появляются изменения, проявляющиеся в гликогенной инфильтрации эпителия канальцев. Эпителий становится высоким, со светлой пенистой цитоплазмой; зерна гликогена обнаруживаются и в просвете канальцев. Канальцы почек становятся более проницаемыми для белков плазмы и сахаров. Развивается одно из проявлений диабетической микроангиопатии – интеркапиллярный (диабетический) гломерулосклероз. Гликогенозы обусловлены отсутствием или недостаточностью фермента, который участвует в расщеплении депонированного гликогена, и относится к наследственным ферментопатиям (болезням накопления).
При углеводных дистрофиях, связанных с нарушением обмена гликопротеидов, происходит накопление муцинов и мукоидов, называемых также слизистыми и слизеподобными веществами (слизистая дистрофия). Причины различны, но чаще всего это воспаление слизистых оболочек. Системная дистрофия лежит в основе наследственного системного заболевания – муковисцидоза. Поражаются эндокринный аппарат поджелудочной железы, железы бронхиального дерева, пищеварительного и мочевого тракта, желчных путей, половые и слизистые железы. Исход различный – в одних случаях происходит регенерация эпителия и полное восстановление слизистой оболочки, а в других она атрофируется, склерозируется, и нарушается функция органа.
Стромально-сосудистая дистрофия – это нарушение обмена в соединительной ткани, преимущественно в ее межклеточном веществе, накопление продуктов метаболизма. В зависимости от вида нарушенного обмена мезенхимальные дистрофии делятся на белковые (диспротеинозы), жировые (липидозы) и углеводные. Среди диспротеинозов различают мукоидное набухание, фибринозное набухание, гиалиноз и амилоидоз. Первые три связаны с нарушением проницаемости сосудистой стенки.
1. Мукоидное набухание – это обратимый процесс. Происходят поверхностные неглубокие изменения структуры соединительной ткани. За счет действия патологического фактора в основном веществе возникают процессы декомпозиции, т. е. распадаются связи белков и аминогликанов. Аминогликаны находятся в свободном состоянии и обнаруживаются в соединительной ткани. За их счет соединительная ткань окрашивается базофильно. Возникает феномен метахромазии (способность ткани изменять цвет красителя). Так, толуидиновый синий в норме синий, а при мукоидном набухании – розовый или сиреневый. Муцин (слизь) состоит из протеидов и поэтому своеобразно окрашивается. Глюкозоаминогликаны хорошо впитывают жидкость, которая выходит из сосудистого русла, и волокна набухают, но не разрушаются. Макроскопическая картина не изменена. К факторам, вызывающим мукоидное набухание, относятся: гипоксии (гипертоническая болезнь, атеросклероз), иммунные нарушения (ревматическая болезнь, эндокринные нарушения, инфекционные заболевания).
2. Фибриноидное набухание – это глубокая и необратимая дезорганизация соединительной ткани, в основе которой лежит деструкция основного вещества ткани и волокон, сопровождающаяся резким повышением сосудистой проницаемости и образованием фибриноида. Может быть следствием мукоидного набухания. Волокна разрушаются, процесс носит необратимый характер. Свойство метахромазии пропадает. Макроскопическая картина без изменений. Микроскопически наблюдаются коллагеновые волокна, пропитанные белками плазмы, окрашиваемые в желтый цвет пирофуксином.
Исходом фибриноидного набухания могут быть некроз, гиалиноз, склероз. Вокруг зоны фибриноидного набухания скапливаются макрофаги, под действием которых клетки разрушаются и наступает некроз. Макрофаги способны вырабатывать монокины, которые способствуют размножению фибробластов. Таким образом, зона некроза заменяется соединительной тканью – возникает склероз.
3. Гиалиновая дистрофия (гиалиноз) . В соединительной ткани образуются однородные прозрачные плотные массы гиалина (фибриллярного белка), которые устойчивы по отношению к щелочам, кислотам, ферментам, ШИК-положительны, хорошо воспринимают кислые красители (эозин, кислый фуксин), пирофуксином окрашиваются в желтый или красный цвет.
Гиалиноз – это исход разных процессов: воспаления, склероза, фибриноидного набухания, некроза, плазматического пропитывания. Различают гиалиноз сосудов и собственно соединительной ткани. Каждый может быть распространенным (системным) и местным.
При гиалинозе сосудов поражаются преимущественно мелкие артерии и артериолы. Микроскопически – гиалин обнаруживается в субэндотелиальном пространстве, разрушая эластическую пластинку, сосуд превращается в утолщенную стекловидную трубочку с очень суженным или полностью закрытым просветом.
Гиалиноз мелких сосудов носит системный характер, но значительно выражен в почках, головном мозге, сетчатке глаза, поджелудочной железе. Характерен для гипертонической болезни, диабетической микроангиопатии и заболеваний с нарушениями иммунитета.
Выделяют три вида сосудистого гиалина:
1) простой, возникающий вследствие инсудации неизмененных или малоизмененных компонентов плазмы крови (при гипертонической болезни, атеросклерозе);
2) липогиалин, содержащий липиды и?-липопротеиды (при сахарном диабете);
3) сложный гиалин, строящийся из иммунных комплексов, разрушающихся структур сосудистой стенки, фибрина (характерен для заболеваний с иммунопатологическими нарушениями – например, для ревматических заболеваний).
Гиалиноз собственно соединительной ткани развивается в исходе фибриноидного набухания, которое ведет к деструкции коллагена и пропитыванию ткани белками плазмы и полисахаридами. Внешний вид органа изменяется, возникает его атрофия, происходят деформация и сморщивание. Соединительная ткань становится плотной, белесоватой и полупрозрачной. Микроскопически – соединительная ткань теряет фибриллярность и сливается в однородную плотную хрящеподобную массу; клеточные элементы сдавливаются и подвергаются атрофии.
При местном гиалинозе исходом являются рубцы, фиброзные спайки серозных полостей, склероз сосудов и т. д. Исход в большинстве случаев неблагоприятный, но возможно и рассасывание гиалиновых масс.
4. Амилоидоз – разновидность белковой дистрофии, которая является осложнением различных заболеваний (инфекционной, воспалительной или опухолевой природы). В таком случае имеется приобретенный (вторичный) амилоидоз. Когда амилоидоз является следствием неизвестной этиологии – это первичный амилоидоз. Заболевание было описано К. Ракитанским и носило название «сальная болезнь», так как микроскопическим признаком амилоидоза является сальный блеск органа. Амилоид представляет собой сложное вещество – гликопротеид, в котором глобулярные и фибриллярные белки имеют тесную связь с мукополисахаридами. Если для белков характерен примерно одинаковый состав, то полисахариды всегда имеют различный состав. В результате амилоид никогда не имеет постоянного химического состава. Доля белков составляет 96–98 % всей массы амилоида. Существуют две фракции углеводов – кислые и нейтральные полисахариды. Физические свойства амилоида представлены анизотропией (способностью к двойному лучепреломлению, что проявляется в поляризованном свете), под микроскопом амилоид продуцирует желтое свечение, чем отличается от коллагена и эластина. Красочные реакции для определения амилоида: элективная окраска «Конго красный» окрашивает амилоид в кирпично-красный цвет, что происходит вследствие наличия в составе амилоида фибрилл, которые обладают способностью связывать и прочно удерживать на себе краску.
Метахроматические реакции: йод зеленый, метил-фиолет, генциан-фиолет окрашивают амилоид в красный цвет на зеленом или синем фоне. Окрашивание происходит за счет гликозоаминогликанов. Самой чувствительной методикой является обработка флюорохромом (тиофлавин S, F). С помощью этого метода можно выявить минимальные отложения амилоида. Может наблюдаться ахроматический амилоид, который полностью не окрашивается; в таком случае используется электронная микроскопия. Под электронным микроскопом становятся видны 2 компонента: Ф-компонент – фибриллы и П-компонент – периодические палочки. Фибриллы представляют собой две параллельные нити, периодические палочки состоят из пентагональных образований.
Выделяют IV звена морфогенеза.
I. Клеточная трансформация ретикуло-эндотелиальной системы, предшествующая образованию клонов клеток – амилоидобластов.
II Синтез амилоидобластами главного компонента амилоида – фибриллярного белка.
III Агрегация фибрилл друг с другом с образованием каркаса амилоида.
IV. Соединение агрегированных фибрилл с белками плазмы крови, а также с гликозоаминогликанами тканей, что приводит к выпадению в тканях аномального вещества – амилоида.
На первой стадии происходит образование в органах ретикуло-эндотелиальной системы плазматических клеток (плазматизация костного мозга, селезенки, лимфатических узлов, печени). Плазматизация отмечается и в строме органов. Плазматические клетки преобразуются в клетки-амилоидобласты. Синтез фибриллярного белка всегда происходит в клетках, имеющих мезенхимное происхождение. Это лимфоциты, плазматические клетки, фибробласты, ретикулярные клетки (фибробласты чаще всего встречаются при семейном амилоидозе), плазматические – при первичном амилоидозе (обусловлены опухолью), ретикулярные – при вторичном амилоидозе. Также в качестве амилоидобласта могут выступать купферовские клетки печени, звездчатые эндотелиоциты, мезангиальные клетки (в почке). Когда белка накапливается достаточно, происходит формирование каркаса.
Фибриллярный белок рассматривается как чужеродный, аномальный. В ответ на его образование появляется дополнительная группа клеток, которая начинает пытаться лизировать амилоид. Эти клетки называются амилоидокластами. Функцию таких клеток могут осуществлять свободные и фиксированные макрофаги. В течение долгого времени между клетками, которые образуют и рассасывают амилоид, происходит равная борьба, но она всегда заканчивается победой амилоидобластов, так как в тканях возникает иммунологическая толерантность к белку фибрилл амилоида. На фибриллярный скелет происходит осаждение белков и полисахаридов.
Образуется амилоид всегда вне клеток и всегда имеет тесную связь с волокнами соединительной ткани: с ретикулярными и коллагеновыми. Если выпадение амилоида происходит по ходу ретикулярных волокон в мембранах сосудов или желез, то он называется периретикулярным амилоидом (паренхиматозным) и наблюдается в селезенке, печени, почках, надпочечниках и кишечнике. Если образование и выпадение амилоида приходится на коллагеновые волокна, то он называется периколлагеновым или мезенхимальным. В данном случае поражается адвентиция крупных сосудов, строма миокарда, поперечно-полосатая и гладкая мускулатура, нервы и кожа.
Существует 3 старых и 1 новая современная теория, которая объединяет все три теории патогенеза амилоидоза.
1. Теория диспротеиноза . По данным этой теории, развивается диспротеинемия, при ней происходит накопление в плазме крови грубодисперсных белковых фракций и аномальных белков – парапротеинов. Они появляются за счет нарушенного белкового обмена. Потом они выходят за пределы сосудистого русла, взаимодействуют с мукополисахаридами тканей. Эта теория является прямолинейной и не дает объяснения возникновения диспротеинемии.
2. Иммунологическая теория . При разнообразных заболеваниях накапливаются продукты распада тканей, лейкоцитов, в крови циркулируют также токсины бактерий – все эти вещества имеют антигенные свойства и приводят к образованию антител самим себе. Развивается иммунная реакция соединения антигенов антителами в тех местах, где происходила продукция антител, т. е. в органах ретикуло-эндотелиальной системы. Эта теория объяснила только часть амилоидной дистрофии, т. е. ту, где имеется хроническое нагноение, и не объясняет генетические формы амилоидоза.
3. Теория клеточно-локального синтеза . Эта теория изучает амилоид как секрет мезенхимальных клеток.
4. Универсальная теория – мутационная. Мутагенные факторы оказывают влияние на клетки, тем самым вызывают мутации, и происходит запуск механизма, ведущего к формированию клеток-амилоидобластов.
Различают вторичные, или приобретенные, формы и идиопатические (первичные), наследственные (семейные, старческие, опухолевидные). Вторичная форма является осложнением самых разных инфекций. Причины первичных амилоидозов неизвестны.
Вторичные амилоидозы локализованы периретикулярно, оказывают разрушительное воздействие на паренхиматозные органы. Вторичные амилоиды выпадают по ходу коллагеновых волокон. Чаще всего происходит поражение органов мезенхимального происхождения. При идиопатической форме подвергаются поражению сердце, нервы, кишечник. При наследственном или семейном амилоидозе идет воздействие на симпатические нервные ганглии, а также паренхиматозные органы – почки. Характерна так называемая периодическая болезнь, которая наблюдается у лиц наиболее древних национальностей, например у евреев, арабов, армян. При старческой форме поражаются сердце, семенные пузырьки.
Опухолевидный амилоидоз имеет такое название, потому что отложение амилоида, возникающее при нем, напоминает опухоль. Она поражает дыхательные пути, трахею, мочевой пузырь, кожу, конъюнктиву.
К этиологическим причинам вторичного амилоидоза относятся:
1) хронические неспецифические заболевания легких, такие как хронический бронхит с бронхоэктазами, хронические абсцессы легкого, бронхоэктатическая болезнь;
2) туберкулез в кавернозной форме;
3) ревматоидный полиартрит (около 25 %).
Макроскопическая характеристика: органы увеличены в размерах, плотные, хрупкие, легко ломаются, край разреза острый, так как амилоид откладывается под мембраной сосудов, вызывает их сужение, развивается ишемия, и орган становится бледным. Амилоид придает органу характерный сальный блеск.
При вскрытии на органах используется макроскопическая проба Вирхова на амилоид. Проба проводится на свежих, нефиксированных органах: берут пластинку из органа, промывают водой от крови и поливают раствором Люголя, а через 30 мин орган поливают 10 %-ной серной кислотой. При появлении грязно-бутылочного окрашивания проба положительна.
Селезенка поражается в II стадии. На первой стадии происходит накопление амилоида в фолликулах селезенки, в белой пульпе, и имеет вид белых зерен. Они похожи на саговые зерна, и такая селезенка называется саговой. На второй стадии амилоид распространяется по всему органу. Селезенка сильно увеличивается в размерах, плотной консистенции, на разрезе коричневато – красная с сальным блеском. Она получила название сальная (ветчинная) селезенка.
В почке амилоид появляется под мембраной капилляров клубочков, под мембраной сосудов мозгового и коркового слоя, под мембранами извитых и прямых канальцев, а также в строме почки по ходу ретикулярных волокон. Этот процесс постоянный: первая стадия – скрытая (латентная) амилоид начинает формироваться в пирамидах, в клубочковых кровеносных сосудах; вторая стадия характеризуется протеинурией. В моче определяется большое количество белка. В строме отмечаются явления склероза – за счет развивающейся ишемии. В эпителии обнаруживаются признаки жировой и гиалиново-капельной дистрофии.
Третья стадия – нефротическая. Макроскопические изменения соответствуют большой сальной почке: орган значительно увеличен в размерах, толстый и достаточно бледный корковый слой с сальным блеском и набухшие багрово-синюшные пирамидки. На микроскопической картине видно, что все клубочки содержат диффузно расположенный амилоид. Последняя, заключительная стадия – уремическая. На этой стадии развивается сморщивание почки. Почечная недостаточность ведет к смерти.
В печени откладывание амилоида начинается в синусоидах между купферовскими клетками, по ходу ретикулярной стромы долек, печеночные клетки сдавливаются и погибают от атрофии. В надпочечниках амилоид откладывается только в корковом слое по ходу капилляров, что приводит к недостаточности надпочечников, поэтому любая травма или стресс может привести больного к гибели.
В кишечнике поражается чаще всего тонкая кишка. Амилоид откладывается по ходу ретикулярной стромы слизистой оболочки, под мембраной мелких сосудов, что в дальнейшем ведет к атрофии, изъязвлению слизистой. Происходит нарушение всасывания, развивается истощение вследствие поносов.
При липидозах происходит нарушение обмена нейтральных жиров, холестерина или его эфиров. Ожирение или тучность – это увеличение количества нейтральных жиров в жировых депо. Оно выражается в обильном отложении жиров в подкожной клетчатке, сальнике, брыжейке, средостении, эпикарде.
Жировая ткань появляется там, где она обычно отсутствует. Большое клиническое значение имеет развившееся ожирение сердца. Жировая ткань разрастается под эпикардом, окутывает сердце, прорастает строму миокарда и приводит к атрофии мышечных клеток. Может произойти разрыв сердца.
Ожирение подразделяется:
1) по этиологии – на первичное (идиопатическое) и вторичное (алиментарное, церебральное, эндокринное и наследственное);
2) по внешним проявлениям – на симметричный, верхний, средний и нижний типы ожирения;
3) по превышению массы тела – I степени (ИМТ 20–29 %), II степени (30–49 %), III степени (50–99 %), IV степени (до 100 % и более).
Нарушение обмена холестерина и его эфиров лежит в основе атеросклероза. При этом в интиме артерий происходит накопление не только холестерина и его эфиров, но и?-липопротеидов низкой плотности и белков плазмы крови, чему способствует повышение сосудистой проницаемости.
Накапливающиеся высокомолекулярные вещества ведут к деструкции интимы, распадаются и омыляются. В результате этого в интиме образуется жиробелковый детрит, разрастается соединительная ткань и формируется фиброзная бляшка, суживающая просвет сосуда.
При углеводных стромально-сосудистых дистрофиях нарушается баланс гликопротеидов и гликозоаминогликанов. Происходит замещение коллагеновых волокон слизеподобной массой. Причинами являются дисфункция эндокринных желез и истощение. Процесс может быть обратимым, но прогрессирование его ведет к колликвации и некрозу ткани с формированием полостей, заполненных слизью.
Смешанные дистрофии. О смешанных дистрофиях говорят в тех случаях, когда морфологические проявления нарушенного метаболизма накапливаются как в паренхиме, так и в строме, стенке сосудов и тканей. Они возникают при нарушении обмена сложных белков – хромопротеидов, нуклеопротеидов и липопротеидов, а также минералов.
1. Нарушение обмена хромопротеидов (эндогенные пигменты). Эндогенные пигменты в организме выполняют определенную роль:
а) гемоглобин осуществляет перенос кислорода – дыхательная функция;
б) меланин защищает от УФ-лучей;
в) билирубин участвует в пищеварении;
г) липофусцин обеспечивает клетку энергией в условиях гипоксии.
Все пигменты в зависимости от источника образования делятся на гемоглобиногенные, протеиногенные и липидогенные. Гемоглобинные пигменты состоят из ферритина, гемосидерина и билирубина.
Гемосидерин – это пигмент, который в небольшом количестве образуется в нормальных условиях при естественном старении эритроцитов и их распаде.
Продукты распада эритроцитов захватываются клетками ретикуло-эндотелиальной системы печени, селезенки, костным мозгом и лимфатическими узлами, где представлены в виде коричневых зерен гемосидерина. Образуются в сидеробластах, которые содержат сидеросомы. Основой образования является ферритин (железопротеин), который образуется при соединении с мукопротеидами клетки. Сидеробласты могут его удерживать, но при большой его концентрации клетки разрушаются и пигмент попадает в строму. Выявляют ферритин реакцией Перлса (желтая кровяная соль в сочетании с соляной кислотой приобретает синий или сине-зеленоватый цвет). Это единственный железосодержащий пигмент. Синтез этого пигмента осуществляется в живой, функционирующей клетке. О нарушении этого пигмента говорят тогда, когда его количество резко возрастает.
Различают общий и местный гемосидероз. Общий гемосидероз возникает при внутрисосудистом гемолизе эритроцитов. Причины – различные инфекции (сепсис, малярия и т. д.), интоксикации (соли тяжелых металлов, фтор, мышьяк) и болезни крови (анемия, лейкозы, переливание крови, несовместимой по группе или резус-фактору). При этом органы увеличены в объеме, уплотнены, на разрезе коричневого или ржавого цвета.
При микроскопии печени гемосидерин в клетках ретикуло-эндотелиальной системы в балках по ходу синусов, а также в гепатоцитах, т. е. в паренхиме. Если процесс носит незначительный характер, то возможно полное структурное и функциональное выздоровление, а при значительной выраженности процесса – склероз и, как завершающий этап, цирроз. Местный гемосидероз развивается при распаде эритроцитов вне сосудистого русла, т. е. в очагах кровоизлияний. Наибольшее значение имеют 2 локализации гемосидероза – в веществе головного мозга и легких.
Различают 2 вида кровоизлияний:
1) мелкие, диапедезного характера; ткань мозга сохранена, не разрушена, поэтому гемосидерин будет образовываться как в центре, так и на периферии очага кровоизлияния; в веществе головного мозга микроглия и небольшое количество лейкоцитов;
2) гематомного типа – при разрыве стенок кровеносных сосудов и сопровождаются разрушением вещества головного мозга; в дальнейшем формируется полость (киста) с коричневыми (ржавыми) стенками; при таких кровоизлияниях гемосидерин образуется только на периферии в стенке кисты.
Гемосидерин появляется в очаге кровоизлияния только в конце 2-х – начале 3-х суток. Кровоизлияние, в котором его нет, называется свежим, а где присутствует – старым. Гемосидероз легких или бурая индурация легких, так как в легком сочетаются гемосидероз и склероз.
При хроническом венозном полнокровии в малом кругу кровообращения возникает гипоксия, приводящая к диапедезу кровоизлияний в ткань легкого. Пигмент находится в альвеолах и межальвеолярной перегородке, а гипоксия вызывает усиленную продукцию коллагена. Межальвеолярная перегородка утолщается и уплотняется. Нарушаются газообмен и вентиляция легких.
Гематоидин образуется на 10-12-е сутки в очень крупных и старых очагах кровоизлияний, которые сопровождаются деструкцией ткани. Располагается всегда в центре очага. Морфологическая картина: кристаллы или ромбовидные структуры желтого или розового цвета.
Билирубин содержится в виде непрямого, т. е. связанного с альбумином, или неконъюгированного. Билирубин захватывается гепатоцитами печени, где осуществляется конъюгация с глюкуроновой кислотой, и такой прямой билирубин попадает в кишечник. О нарушении говорят при повышении его количества в сыворотке крови с последующим окрашиванием кожных покровов и слизистых в желтый цвет.
По механизму развития различаются:
1) гемолитическая, или надпеченочная, желтуха, причинами которой являются инфекции, болезни крови, интоксикации, переливание несовместимой крови;
2) паренхиматозная, или печеночная, желтуха – возникает вследствие болезни печени; гепатоциты не могут осуществлять полный захват непрямого билирубина и конъюгировать;
3) механическая, или подпеченочная, желтуха; причины – закупорка общего или печеночного протоков, фатерова сосочка; опухоль головки поджелудочной железы и т. д.
Вследствие нарушения оттока желчи возникает холистаз, что сопровождается расширением капилляров в дольках, уплотнением желчи и образованием желчных тромбов. Гепатоциты начинают инфильтрироваться желчными пигментами и разрушаться, а содержимое начинает попадать в кровеносные сосуды. Таким образом, в кровь попадает прямой билирубин и возникают интоксикация и желтушное окрашивание. Кроме того, в кровь попадают желчные кислоты, вызывающие кожный зуд и мелкие точечные кровоизлияния, которые связаны с высокой сосудистой проницаемостью. Исходы: холангит (воспаление желчных капилляров и протоков) и склероз, а затем и цирроз печени.
Гемомеланин, или малярийный пигмент, возникает только при малярии, так как вырабатывается малярийным плазмодием. Он внедряется в эритроциты, а затем захватывается клетками ретикуло-эндотелиальной системы. Пигмент имеет вид зерен черного цвета. Органы увеличены, плотные, на разрезе серовато-черного цвета или аспидного. При избытке пигмента возникает агрегация этих зерен – малярийный стаз. Последствие стаза сказывается на ЦНС, возникают участки ишемизации с последующим некрозом и мелкими кровоизлияниями. Кроме того, имеет место общий гемосидероз, а также развитие гемолитической желтухи.
Меланин синтезируется меланоцитами. Для синтеза необходимы тирозин и тирозиназные ферменты. Синтез регулируют вегетативная, эндокринная системы и сами УФ-лучи. Вегетативная (симпатическая) система повышает выработку, а парасимпатическая снижает. Эндокринная система – адренокортикотропный гормон стимулирует, а мелатонин угнетает. Пигмент располагается в базальном слое эпидермиса. Соотношение меланоцитов ко всем клеткам базального слоя – 1: 15. Нарушение идет по пути гиперпродукции и гипопродукции.
Гипермеланизы, или бронзовая болезнь (аддисонова болезнь), – это приобретенная болезнь, при которой имеют место усиленное диффузное окрашивание кожи, гипотония, адинамия и мышечная слабость. Обусловлено заболевание поражением надпочечников (туберкулез, амилоидоз, онкологические процессы). В этих условиях усиленно синтезируется АКТГ.
Пигментная ксеродерма – это врожденное заболевание. Кожа сухая, желтушная, гиперемированная, гиперпигментированная и шелушащаяся. Возникает вследствие недостатка фермента эндонуклеаза, который участвует в утилизации меланина. К местным гипермеланозам относятся родимые пятна. Это врожденный порок развития кожи, который характеризуется тем, что в процессе эмбриогенеза происходит смещение из нейроэктодермальной трубки меланобластов не только в эпидермис, но и в дерму. Иногда родимое пятно может переходить в злокачественную опухоль (меланома).
Среди гипомеланоза различают альбинизм, вейтилиго и лейкодерму.
Альбинизм – это врожденная генетически обусловленная патология, связанная с отсутствием или недостаточной выработкой фермента тиротиназы. У таких людей кожа и волосы белого цвета, глаза красные, нарушены терморегуляция и барьерная функция кожи. Продолжительность жизни короткая.
Вейтилиго – это участок депигментации неправильной формы. Данная патология генетически обусловлена и носит наследственный характер.
Лейкодерма – это участок депигментации кожи округлой формы, возникший в результате воздействия на кожу патогенных факторов. Присутствует у больных сифилисом, лепрой. При этой патологии отмечается поражение кожи с деструкцией телец Фатеро-Пачино (рецепторы). Сначала депигментация появляется на коже шеи и напоминает ожерелье Венеры. Депигментация может быть после ожогов, синтетических веществ и т. д.
Липофусцин – это пигмент, имеющий вид желтых гранул и локализующийся в митохондриях или вблизи них. В норме он содержится в гепатоцитах, кардиоцитах и ганглиозных клетках, депонируя кислород; в условиях гипоксии – обеспечивает клетку кислородом. В условиях патологии, а именно при хронических инфекциях (например, туберкулез) и при онкологических процессах, в клетках печени, сердца и ЦНС количество этого пигмента резко возрастает и локализуется в лизосомах. Функция депонирования и обеспечения клеток кислородом не выполняется. Печень и сердце уменьшаются в размерах, становятся очень плотными, цвет приобретают коричнево-серый (бурый).
Подробности
Дистрофия – сложный патологический процесс, в основе которого лежит нарушение тканевого метаболизма, ведущее к структурным изменениям.
Трофика – совокупность механизмов, определяющих метаболизм и структурную организацию клетки (ткани), необходимых для выполнения специализированной функции.
Причины дистрофий:
1) расстройства ауторегуляции клетки, которые могут быть вызваны гиперфункцией, токсическими веществами, радиацией, недостаточностью фермента и т.д.
2) нарушение функции транспортных систем, обеспечивающих метаболизм и структурную сохранность тканей, вызывают гипоксию.
3) нарушение эндокринной, нервной регуляции
Морфогенез дистрофий:
1) инфильтрация
Избыточное накопление вещества (нормального, не аномального) в результате избыточного синтеза.
Пример: жировой гепатоз печени, гемосидероз почки.
2) декомпозиция (фанероз )
Распад ультраструктур клеток и межклеточного вещества, ведущий к нарушению тканевого метаболизма и накоплению продуктов нарушенного обмена в ткани.
3) извращенный синтез
Синтез аномальных продуктов. К ним относятся: синтез аномального белка амилоида в клетке, синтез белка алкогольного гиалина гепатоцитом.
4) трансформация
Образование продуктов одного вида обмена из общих исходных продуктов, которые идут на построение БЖУ.
Классификации дистрофии.
В классификации придерживаются нескольких принципов. Выделяют дистрофии:
1) по преобладанию морфологических изменений в тканевых структурах: паренхиматозные, смешанные, мезенхимальные (стромально-сосудистые)
2) по преобладанию нарушений того или иного вида обмена : белковые, жировые, углеводные, минеральные.
3) в зависимости от влияния генетических факторов : приобретенные, наследственные.
4) по локализации : местные, общие.
Паренхиматозные дистрофии.
Проявления нарушений обмена в высокоспециализированных в функциональном отношении клетках.
1) Паренхиматозные белковые дистрофии (диспротеинозы)
Сущность таких дистрофий состоит в изменении физико-химических и морфологических свойства белков клетки: они подвергаются денатурации и коагуляции или колликвации, что ведет к гидратации цитоплазмы. В тех случаях, когда нарушатся связи белков с липидами, возникает деструкция мембранных структур клетки.
Нарушение обмена белков часто сочетается с расстройствами работы Na-K-помпы: что ведет к накоплению ионов Nа и набуханию клетки. Такой патологический процесс называется гидропической дистрофией.
Виды:
-зернистая
Обратима, выглядит как накопление мелких зерен белка в цитоплазме. Органы увеличиваются в размерах, становятся дряблыми и тусклыми.
-гиалиново-капельная
В цитоплазме появляются крупные гиалиноподобные белковые капли, сливающиеся между собой и заполняющие тело клетки. В ряде случаев завершается фокальным коагуляционным некрозом клетки.
Часто встречается в почках, редко – в печени и миокарде.
В почках при исследовании накопление капель находят в нефроцитах. Накопление часто отмечается при нефротическом синдроме, так как в основе этой дистрофии лежит недостаточность вакуолярно-лизосомального аппарата эпителия проксимального канальца, в котором в норме реабсорбируются белки. Именно поэтому в моче появляется белок (протеинурия) и цилиндры (цилиндрурия).
Внешний вид не имеет каких-либо характерных черт.
В печени при микроскопии обнаруживаются тельца Мэлори, состоящие из фибрилл и алкогольного гиалина. Появление таких капель – проявление извращенной синтетической функции гепатоцита, что встречается при алкогольном гепатите, первичном билиарном циррозе. Внешний вид печени различен.
Исход гиалиново-капельной дистрофии неблагоприятен, она ведет к некрозу клетки.
-гидропическая дистрофия
Характеризуется появление в клетке вакуолей, наполненных цитоплазматической жидкостью. Наблюдается чаще в эпителии кожи и почечных канальцев, в гепатоцитах и миоцитах.
Паренхиматозные клетки увеличены в объеме, их цитоплазма заполнена вакуолями, содержащими прозрачную жидкость. Затем клетка превращается в огромный баллон (вся клетка стала большой вакуолью) – фокальный колликвационный некроз. Внешний вид тканей мало изменяется.
Большую роль в механизме развития играет нарушение проницаемости мембраны, которое ведет к закислению цитоплазмы, активации гидролитических ферментов лизосом, которые разрывают внутримолекулярные связи с присоединением воды.
Причины: в почках – повреждение почечного фильтра, что ведет к гиперфильтрафии, в печени – гепатиты различной этиологии, в эпидермисе – отек, инфекция.
Исход такой дистрофии, как правило, неблагоприятный – она завершается фокальным коагуляционным некрозом.
-роговая дистрофия
Характеризуется избыточным образованием рогового вещества в ороговевающем эпителии (гиперкератоз, ихтиоз) или образование рогового вещества там, где в норме его не бывает (патологическое ороговение на слизистых оболочках). Причины разнообразны: нарушения развития кожи, хроническое воспаление, авитаминозы и т.д.
Исход: иногда при устранении причины происходит восстановление ткани, однако в запущенных случаях наступает гибель клеток.
- наследственные нарушения обмена аминокислот
Так называемые болезни накопления, в основе которых лежит нарушение внутриклеточного метаболизма ряда аминокислот в результате наследственной недостаточности метаболизирующих ферментов.
А) цистиноз. Науке еще не известно, недостаточность какого фермента приводит к этому заболеванию. АК накапливается в печени, почках, селезенке, глазах, костном мозге, коже.
Б) тирозиноз. Возникает при дефиците тирозинаминотрансферазы. Накапливается в печени, почках, костях.
В) фенилпировиноградная олигофрения. Возникает при дефиците фенилаланин-4-гидроксилазы и накапливается в нервной системе, мышцах и крови.
2) Паренхиматозные жировые дистрофии (липидозы)
Нарушения обмена цитоплазматических липидов могут проявляться в увеличении их содержания в клетках, где они обнаруживаются и в норме., в появлении липидов там, где они обычно не встречаются, и в образовании жиров необычного химического состава.
-нарушения обмена липидов
В печени жировая дистрофия проявляется резким увеличением содержания жиров в гепатоцитах и изменением их состава. В клетках печени сначала появляются гранулы липидов (пылевидное ожирение), затем мелкие капли (мелкокапельное ожирение), которые затем сливаются в крупные капли (крупнокапельное) или в одну жировую вакуоль. Печень увеличена, дряблая и охряно-желтого цвета. Среди механизмов жировой дистрофии печени различают, чрезмерное поступление в гепатоциты жирных кислот или повышенный их синтез этими клетками, воздействие токсических веществ, блокирующих окисление жирных кислот и синтез липопротеидов в гепатоцитах, недостаточное поступление в печеночные клетки аминокислот, необходимых для синтеза. Итак, ЖДП возникает в результате: липопротеидемии (алкоголизм, сахарный диабет, общее ожирение), гепатотропных интоксикациях (этанол, хлороформ), нарушения питания.
Жировая дистрофия миокарда возникает вследствие гипоксии и интоксикации. Механизм развития связан со снижением окисления жирных кислот из-за деструкции митохондрий под действием гипоксии или токсина. При макроскопическом исследовании размеры сердца увеличены, сердечная мышца глиняно-желтого цвета. Миокард похож на шкуру тигра – бело-желтая исчерченность. Липиды определяются в виде мелких капель.
Причины жировой дистрофии разнообразны. Они могут быть связаны с кислородным голоданием (потому часто встречается при заболеваниях ССС), инфекциями и интоксикациями, авитаминозами и односторонним питанием.
Исход жировой дистрофии зависит от ее степени. Если не сопровождается грубым поломом клеточных структур, то она обратима.
-наследственные ферментопатии
Возникают вследствие наследственного дефицита ферментов, участвующих в метаболизме липидов.
А) болезнь Гоше при дефиците глюкоцереброзидазы. Липид накапливается в печени, селезенке, костном мозге.
Б) болезнь Ниманна -Пика при дефиците сфингомиелиназы. Накопление в печени, селезенке, костном мозге.
В) болезнь Сакса при дефиците кислой галактозидазы.
Г) болезнь Нормана -Ландинга при дефиците бета-галактозидазы.
3) Паренхиматозные углеводные дистрофии
-углеводные дистрофии, связанные с нарушением обмена гликогена
При сахарном диабете происходит недостаточное использование глюкозы тканями, увеличение ее содержания в крови и выведение с мочой. Тканевые запасы гликогена резко уменьшаются. В печени нарушается синтез гликогена, что ведет к ее инфильтрации жирами и жировой дистрофии печени.
В почках при сахарном диабете происходят следующие изменения: гликогенная инфильтрация эпителия канальцев.
-наследственные гликогенозы
а) 1 типа – болезнь Гирке – дефицит глюкозо-6-фосфатазы
б) 2 типа – болезнь Помпе – дефицит кислой альфа-1,4-глюкозидазы
в) 3 типа – болезнь Форбса – дефицит амило-1,6-глюкозидазы
г) 4 типа – болезнь Андресона – дефицит амило-(1,4-1,6)-трансглюкозидазы
д) 5 типа – болезнь Мак-Ардля – дефицит миофосфорилазы
е) 6 типа – болезнь Герса – дефицит фосфорилазы печени
При болезнях 1,2,5,6 типов структура гликогена не нарушена.
-углеводные дистрофии, связанные с нарушениями обмена гликопротеидов
В клетках или межклеточном веществе происходит накопление муцинов и мукоидов, называемых также слизистыми или слизеподобными вещества.
Многие секретирующие клетки погибают и десквамируются, выводные протоки желез обтурируются слизью, что ведет к развитию кист.
Причины разнообразны, но чаще всего – воспаление слизистых оболочек в результате действия различных патогенных раздражителей.
Иногда в клинической практике встречается такое явление, как паренхиматозные дистрофии. Патологическая анатомия относит их к нарушениям обмена в клетках. Если говорить простым языком, то в органе нарушается процесс питания и накопления полезных веществ, что приводит к морфологическим (визуальным) изменениям. Выявить такую патологию можно на секции или после серии высокоспецифических тестов. Паренхиматозные и стромально-сосудистые дистрофии лежат в основе многих летальных заболеваний.
Определение
Паренхиматозные дистрофии - это патологические процессы, которые ведут к изменениям структуры клеток органов. Среди механизмов развития заболевания выделяют расстройства саморегуляции клетки с энергетическим дефицитом, ферментопатии, дисциркуляторные расстройства (кровь, лимфа, интерстиций, межклеточная жидкость), эндокринные и церебральные дистрофии.
Различают несколько механизмов дистрофии:
Инфильтрацию, то есть избыточный транспорт продуктов обмена из крови внутрь клетки или межклеточное пространство, обусловленный сбоем в ферментных системах организма;
Декомпозиция, или фанероз, представляет собой распад внутриклеточных структур, который приводит к нарушению метаболизма и накоплению недоокисленных продуктов обмена веществ;
Извращенный синтез веществ, которые в норме клетка не воспроизводит;
Трансформация поступающих в клетку питательных веществ для построения какого-то одного вида конечных продуктов (белков, жиров или углеводов).
Классификация
Патоморфологи выделяют следующие виды паренхиматозных дистрофий:
1. В зависимости от морфологических изменений:
Чисто паренхиматозные;
Стромально-сосудистые;
Смешанные.
2. По виду накапливаемых веществ:
Белковые или диспротеинозы;
Жировые или липидозы;
Углеводные;
Минеральные.
3. По распространенности процесса:
Системные;
Местные.
4. По времени появления:
Приобретенные;
Врожденные.
Те или иные паренхиматозные дистрофии патологическая анатомия определяет не только по повреждающему агенту, но и по специфике пораженных клеток. Переход одной дистрофии в другую теоретически возможен, но практически возможна только сочетанная патология. Паренхиматозные дистрофии - это суть процесса, происходящего в клетке, но только часть клинического синдрома, который охватывает морфологическую и функциональную недостаточность определенного органа.
Диспротеинозы
Человеческое тело по большей части состоит из белков и воды. Белковые молекулы являются составляющей клеточных стенок, мембраны митохондрий и других органелл, кроме того, они находятся в свободном состоянии в цитоплазме. Как правило, это ферменты.
Диспротеинозом иначе называют такую патологию, как паренхиматозная белковая дистрофия. И его суть состоит в том, что клеточные белки меняют свои свойства, а так же подвергаются структурным изменениям, таким как денатурация или колликвация. К белковым паренхиматозным дистрофиям относят гиалиново-капельную, гидропическую, роговую и зернистую дистрофии. О первых трех будет написано подробнее, а вот последняя, зернистая, характеризуется тем, что в клетках накапливаются зерна белка, из-за чего клетки растягиваются, а орган увеличивается, становится рыхлым, тусклым. Именно поэтому зернистую дистрофию еще называют тусклым набуханием. Но у ученых есть сомнения, что это паренхиматозная дистрофия. Патанатомия данного процесса такова, что за зерна можно принять компенсаторно увеличенные клеточные структуры, как ответ на функциональное напряжение.
Гиалиново-капельная дистрофия

Болезнь Мак-Ардля;
Болезнь Герса;
Болезнь Форбса-Кори;
Болезнь Андерсена.
Их дифференциальная диагностика возможна после биопсии печени и использования гистоферментного анализа.
Нарушение обмена гликопротеинов

Это паренхиматозные дистрофии, вызванные накоплением в тканях муцинов или мукоидов. Иначе эти дистрофии еще называют слизистыми или слизеподобными, из-за характерной консистенции включений. Иногда накапливаются на истинные муцины, а только похожие на них вещества, которые могут уплотняться. В таком случае идет речь о коллоидной дистрофии.
Микроскопия ткани позволяет определить не только факт наличия слизи, но и ее свойства. Из-за того, что остатки клеток, а также вязкий секрет препятствует нормальному оттоку жидкости из желез, образуются кисты, а содержимое их имеет тенденцию к воспалению.
Причины этого вида дистрофий могут быть самые разные, но чаще всего это катаральное воспаление слизистых. Кроме того, если наследственное заболевание, патогенетическая картина которого хорошо вписывается в определение слизистая дистрофия. Это муковисцидоз. Поражается поджелудочная железа, кишечная трубка, мочевыводящий тракт, желчные протоки, потовые и слюнные железы.
Разрешение данного вида заболеваний зависит от количества слизи и длительности ее выделения. Чем меньше времени прошло от начала патологического процесса, тем более вероятно, что слизистая восстановится полностью. Но в некоторых случаях наблюдается слущивание эпителия, склероз и нарушение функции пораженного органа.
Патологическая анатомия – это наука, которая изучает патоморфологию болезней на разных морфологических уровнях - макроскопическом, анатомическом, микроскопическом, электронно-микроскопическом и других уровнях структурной организации организма.
Патанатомия включает два раздела:
1. общая патанатомия;
2. частная патанатомия.
В общей патанатомии изучаются общепатологические процессы.
1. повреждение;
2. дисциркуляция;
3. воспаление;
4. компенсаторно-приспособительные процессы;
5. опухоли.
Повреждение или альтерация является универсальным общепатологическим процессом. Без повреждения нет болезней.
Повреждение касается всех уровней структурной организации.
Это- 8 уровней:
1. молекулярный;
2. ультраструктурный;
3. клеточный;
4. межклеточный;
5. тканевой;
6. органный;
7. системный;
8. организменный.
При повреждении структуры на разных уровнях в итоге имеет место снижение ее жизнедеятельности.
При изучении развития болезней вследствие повреждения структур выделяют два раздела патологии.
1. Этиология.
2. Патогенез.
Этиология это учение о причинах повреждения и болезней.
Патогенез это учение о механизмах развития повреждения и болезней.
Все этиологические факторы можно объединить в 7 групп:
1. Физические факторы: термические высокая и низкая температуры, механические, лучевые, электромагнитные колебания.
2. Химические: кислоты, щелочи, отравляющие вещества, соли тяжелых металлов и другие.
3. Токсины - эндогенные и экзогенные яды.
4. Инфекции.
5. Дисциркуляция.
6. Нервно-трофические.
7. Метаболические - нарушение обмена веществ при голодании, авитаминозах, дисбалансе питания.
Патогенез
В этом разделе изучаются такие механизмы повреждения как характер действия повреждающего факторы, который может быть –
прямым и непрямым.
Прямой - это непосредственное разрушение структуры. Непрямой - разрушение через гуморальные, нервные, эндокринные, иммунные факторы.
Изучается также глубина и выраженность повреждения в зависимости от силы повреждающего фактора и реактивности структур организма.
Характеристика повреждения
Оно может быть обратимым и необратимым. В развитии повреждения проходит несколько этапов, когда повреждение от легких форм переходит к средне–тяжелым, тяжелым и, наконец, к гибели структуры. Гибель структуры обозначает термин некроз.
Разновидностью повреждения является дистрофия. Это такой вариант повреждения, когда структура частично разрушено, но еще сохранена и функционирует.
Дистрофия
Расшифровка термина: дис – расстройство, трофика питания. То есть прямой перевод означает расстройство питания.
Развернутое определение термина дистрофии.
Дистрофия это повреждение клеточных и тканевых структур в ответ на нарушение их трофики.
Трофика-это совокупность механизмов, обеспечивающих функциональную и структурную организацию клеток и тканей в целом.
Выделяют два типа трофических механизмов:
1. клеточные;
2. внеклеточные.
Клеточные механизмы включают структурные компоненты клеточной организации, обеспечивающие внутриклеточный обмен веществ. Клетка при этом представляется как саморегулирующая система, в которой задействованы органеллы цитоплазмы, гиалоплазма и ядро.
Внеклеточные механизмы представлены-
1. транспортными системами кровеносные и лимфатические сосуды;
2. эндокринная система;
3. нервная система.
Дистрофии могут быть результатом нарушения и клеточных и неклеточных механизмов трофики.
Потому можно говорить о 3 группах дистрофий в зависимости от нарушения деятельности тофических механизмов-
1. дистрофии вследствие нарушения клеточных механизмов трофики;
2. дистрофии вследствие нарушения работы транспортных систем;
3. дистрофии вследствие нарушения деятельности нервной и эндокринной систем.
При первой группе дистрофий основным патогенетическим звеном является ферментопатия.
Она может быть абсолютной отсутствие ферментов, относительной мало ферментов.
При ферментопатиях развиваются процессы накопления предшествующих метаболитов и блокировка последующих биохимических реакций.
Накопление метаболитов определяется термином тезаурисмозы - болезни накопления. От греческого слова тезаурос – запас.
Вторая группа дистрофий связана с нарушением деятельности транспортных систем, обеспечивающих подвоз продуктов питания и удаления вредных метаболитов.
Главным патогенетическим звеном при этом является гипоксия- снижение количества кислорода.
При третьей группе дистрофий имеет место нарушение деятельности нервной и эндокринных систем. Главным патогенетическим звеном в этом случае является недостаток биологических активных веществ – биоактиваторов - различных гормонов и медиаторов.
В развитии дистрофий отмечаются следующие морфогенетические и биохимические процессы -
1. инфильтрация- накопление белков, жиров, углеводов в клетках и вне клеток;
2. извращенный синтез- синтез необычных веществ;
3. трансформация – переход одних веществ в другие - белков в жиры, углеводов в жиры и так далее;
4. декомпозиция (фанероз) - распад белково-полисахаридных комплексов, белково-липопротедных комплексов.
Классификация дистрофий
В основу классификации положено 4 принципа:
1. морфологический;
2. биохимический;
3. генетический;
4. количественный.
По морфологическому принципу выделяют три вида дистрофий в зависимости от того, что поражается первично - паренхима клетки или мезенхима межклеточные структуры- строма сосуды.
1. Паренхиматозный - первично поражаются клетки.
2. Мезенхимальный – первично поражаются межклеточные структуры.
3. Смешанный – одновременное поражение и паренхимы и мезенхимы.
По биохимическому принципу выделяют дистрофии с нарушением белкового, жирового, углеводного, минерального, пигментного, нуклеопртеодного обменов.
По генетическому принципу выделяют дистрофии приобретенные и наследственные.
По количественному принципу выделяют дистрофии локальные и распространенные.
Основной принцип – морфологический. В рамках морфологической классификации работают и другие классификации.
В итоге можно говорить о 3 видах дистрофий:
1. Паренхиматозная дистрофия.
2. Мезенхимальная дистрофия.
3. Смешанная дистрофия.
Паренхиматозные дистрофии
По биохимическому принципу они делятся на:
1. белковые диспротеинозы;
2. жировые липидозы;
3. углеводные.
Диспротеинозы
В основе этих дистрофий лежит нарушение белкового обмена.
Выделяют 4 вида белковых дистрофий
1. Зернистая.
2. Гидропическая.
3. Гиалиновокапельная.
4. Роговая.
Зернистая дистрофия
Синонимы - тусклое, мутное набухание.
Термин зернистая - отражает гистологическую картину патологии. При этом виде дистрофий цитоплазма вместо гомогенной становится зернистой.
Термины - мутное, тусклое набухание отражают внешний вид поврежденного органа.
Суть патологии - под влиянием действия повреждающего фактора происходит увеличение митохондрий, которые придают цитоплазме зернистый вид.
В развитии дистрофии выделяют две стадии-
Компенсации;
Декомпенсации.
На стадии компенсации митохондрии увеличены, но не повреждены.
На стадии декомпенсации митохондрии увеличены и несколько повреждены.
Однако повреждение митохондрий легкое. При прекращении действия повреждающего фактора они полностью восстанавливают свою структуру.
Микроскопически отмечается в цитоплазме клеток разных органов гепатоцитах, эпителии почечных канальцев, миокардиоцитах зернистость цитоплазы. Состояние митохондрий раскрывают только электронно-микроскопические исследования.
Макроскопический вид органов:
Почка несколько увеличена в размерах, на разрезе тусклая, мутная.
Печень дряблая, края печени закруглены.
Сердце - дряблое, миокард тусклый, мутный, цвета вареного мяса.
Причины зернистой дистрофии:
1. нарушение кровоснабжения органов;
2. инфекции;
3. интоксикации;
4. физические, химические факторы;
5. нарушение нервной трофики.
Значение и исход- процесс обратим, но при продолжении действия повреждающего фактора зернистая дистрофия переходит в более тяжелый вид дистрофий.
Клиническое значение определяется масштабом дистрофии и локализацией. При тотальном поражении миокарда может наступить сердечная недостаточность.
Гидропическая дистрофия
Или водянистая. Характеризуется появлением жидких вакуолей в цитоплазме.
Локализация - эпителий кожи, гепатоциты, эпителий почечных канальцев, миокардиоциты, нервные клетки, клетки коры надпочечников и клетки других органов.
Макроскопия - картина неспецифична.
Микроскопия - обнаруживаются вакуоли, заполненные тканевой жидкостью.
Электронная микроскопия - свидетельствует, что тканевая жидкость накапливается прежде всего в митоходриях, структура которых полностью разрушается и от них остаются пузырьки, заполненные тканевой жидкостью.
В случаях выраженной гидропической дистрофии на месте клетки остается одна большая вакуоль, заполненная цитоплазматической жидкостью. В этом варианте дистрофии все органеллы цитоплазмы клетки разрушаются, а ядро оттесняется на периферию. Такой вариант гидропической дистрофии носит название - баллонная дистрофия.
Исход гидропической дистрофии, особенно баллонной неблагоприятен. Клетка может в последующем погибнуть. А функция поврежденного органа существенно снижается.
Причины гидропической дистрофии – инфекции, интоксикации, гипопротеинемия при голодании, и другие этиологические факторы повреждения.
Гиалиново-капельная дистрофия
Суть процесса - появление в цитоплазме клеток глыбок белка как результат разрушения органелл.
Локализация почки, печень и другие органы.
Причины - вирусные инфекции, алкогольные интоксикации, длительное применение эстрогенов и прогестерона с целью предохранения беременности.
Значение- функция клеток и в целом органа резко снижаются. Поврежденная клетка в дальнейшем погибает.
Роговая дистрофия
Выражается в избыточном появлении рогового вещества в ороговевающем эпидермисе или в местах, где процессы ороговения в норме отсутствуют.
Процесс может быть местным и общим.
1. пороки развития кожи ихтиоз - рыбья чешуя - врожденная патология, при которой на значительной поверхности кожи отмечается ороговение эпидермиса;
2. хроническое воспаление;
3. авитаминоз;
4. вирусная инфекция.
Исход часто необратим для пораженной клетки - она гибнет. Но в целом болезнь можно излечить в случае прекращения действия причинного фактора.
Значение - местные очаги повышенного ороговения особого клинического значения не имеют. Но иногда из очагов поражения на слизистой лейкоплакии- белые пятна - может возникать рак.
Распространенный врожденный вариант роговой дистрофии ихтиоз - несовместим с жизнью. Больные быстро погибают.
Болезни накопления при нарушении метаболизма аминокислот также относятся белковым паренхиматозным дистрофиям.
Наиболее часто отмечается 3 вида патологии:
1. Фенилкетонурия.
2. Гомоцистинурия.
3. Тирозиноз.
Фенилкетонурия
Фенилкетонурия - заболевание связано с дефицитом фермента- фенил-аланин – 4 гидролаза. При это отмечается накопление фенил-пировиноградной кислоты.
Клиника: слабоумие, судорги, дефекты пигментации светлые волосы, голубые глаза, дерматиты, экземы, мышиный запах. Отмечаются также - эпилептиформные припадки, повышенная возбудимость, агрессивность, потемнение мочи.
Патоморфология:
1. Демиелинизация волокнистой глии центральной нервной системы.
2. Жировая дистрофия печени.
3. Ангиоматоз.
4. Гипоплазия тимуса.
5. Исчезновение нервных клеток головного мозга.
6. Сосудистая патология глаз.
Гомоцистинурия (цистиноз)
1. умственная отсталость;
2. подвывих хрусталика;
3. тромбоэмболия;
4. судороги.
Патоморфология: дистрофия и некроз клеток головного мозга, печени, почек, дисплазия костной ткани.
Тирозиноз
В основе болезни лежит дефицит тирозинтрансаминазы. Поражаются центральная нервная система, печень, почки, кости. Часто сочетается с цистинозом. Редкая патология.
Липидозы
Липиды явлются одним из компонентов белково-липидных комплексов, составляющих основу клеточных мембран.
Типы липидов:
1. Фосфатиды - присутствуют везде, особенно их много в центральной нервной системе.
2. Стериды - эфиры жирных кислот + циклические спирты (стерины). Широко распространенный класс веществ, играющих большую роль в организме (холестерин, холестероиды).
3. Сфинголипиды: сфингомиелины, цереброзиды, ганглиозиды. Их особенно много в центральной нервной системе.
4. Воска - класс веществ, близкий к жирам.
В цитоплазме отмечаются и нейтральные жиры, основным депо которых является жировая ткань. Они представляют собой соединения глицерина(щелочь) и жирных кислот(кислоты). Гистохимически нейтральные жиры выявляются на замороженных срезах с помощью окраски судан 3. Окрашиваются в ярко красный цвет.
Паренхиматозная жировая дистрофия
Локализуется там же, где и белковая дистрофия. Обе дистрофии часто сочетаются.
Макроскопический вид пораженных органов имеет свои особенности.
Сердце - увеличено в объеме, желудочки расширены (дилятация), миокард дряблый, глинистого вида. Под эндокардом видны желтые полосы. Эта картина получила название тигровое сердце.
Печень увеличена, тестоватой консистенции, охряно-желтого цвета, при разрезе на лезвии ножа остаются скопления в виде налета жира.
Почки увеличены, дряблые, отмечаются желтоватые мелкие пятна под капсулой и на разрезе.
Микроскопическая картина- в цитоплазме кардиомиоцитов, эпителия почечных канальцев, гепатоцитов определяются включения жира в виде мелких, средних и крупных капель. Биохимический состав их сложен. Это могут быть нейтральные жиры, жирные кислоты, фосфолипиды, холестериды.
Причины паренхиматозных липидозов:
1. тканевая гипоксия (особенно часто в миокарде);
2. инфекции - туберкулез, нагноительные процессы, сепсис, вирусы, алкоголь;
3. интоксикации - фосфор, мышьяк, соли тяжелых металлов, алкоголь;
4. авитаминозы;
5. голодание - алиментарная дистрофия.
Исходные варианты:
1. при незначительно выраженном процессе - патология обратима;
2. в случаях очень выраженного процесса может наступить гибель клетки - некроз.
Значение - снижение функции органов вплоть до развития недостаточности, особенно опасно и скоротечно протекает повреждение миокарда. Развивается сердечная недостаточность и смерть больного.
Наследственные липидозы
Самый частый вариант болезней накопления.
Виды патологии:
1. Ганглиозидозы.
2. Сфингомиелинозы.
3. Глюкоцереброзидозы.
4. Лейкодистрофии.
1. Ганглиозидозы – различают 7 видов ганлиозидозов в зависимости от вариантов ферментопатий. Болезнь может проявляться в детском и юношеском возрасте. Особенно тяжело протекает заболевание в ранне-детском варианте. Оно получило название амавротическая идиотия Тея – Сакса. Симптомы болезни - слепота (амавроз), дистрофия и гибель нервных клеток головного мозга с развитием слабоумия (идиотия). Смерть детей наступает в 2- 4 года.
2. Сфингомиелинозы - дефицит фермента сфингомиелиназы с накоплением сфингомиелинов в клетках головного мозга, печени, селезенки, лимфатических узлах. Патоморфология болезни характеризуется появлением пенистых клеток – клеток в цитоплазме которых накапливаются сфингомиелины, которые при обработке в спиртах и эфирах в процессе приготовления гистологических срезов растворились. А на месте их в цитоплазме остались пустоты, что и обусловливает пенистый вид цитоплазмы этих клеток.
Клинические симптомы в классическом варианте болезни (болезнь Нимана-Пика): начало - 5-6 месяц жизни, слабоумие, похудание, увеличение печени и селезенки, приступы удушья, напоминающие приступы бронхиальной астмы, гипертермические кризы (повышение температуры).
3. Глюкоцереброзидоз (болезнь Гоше).
Главное - дефицит глюкоцереброзидазы и накопление глюкоцереброзидов в цитоплазме клеток разных органов.
Патанатомия – дистрофия печени, увеличение селезенки, распространенная дистрофия и гибель нервных клеток коры головного мозга. Геморрагический синдром - кровоизлияния в разных органах.
1. хроническое течение;
2. гепатоспленомегалия;
3. гперпигментация;
4. слабоумие.
Варианты болезни:
1. хронический висцеральный: начинается в детстве и кончается гибелью больного в возрасте 20-50 лет;
2. острый раннедетский, нейровисцеральный тип – смерть наступает в возрасте 2 лет;
3. подострый юношеский- начинается в юношеском возрасте (18-20 лет) и через несколько лет кончается гибелью больного.
4. Лейкодистрофии.
Группа заболеваний, при которых происходит деструкция белого вещества головного и спинного мозга (лейко - белый; дистрофия- разрушение, повреждение).
Это наследственная патология, генетически обусловленная.
Клиника- нарушение деятельности головного и спинного мозга, в том числе и слабоумие, параличи, нарушение деятельности сердца.
Углеводные паренхиматозные дистрофии
Углеводы - особый класс биохимических соединений.
В живых тканях выделяют следующие виды сложных углеводов (полисахаридов):
1. Гликоген.
2. Мукополисахариды.
3. Глюкопротеиды.
Поэтому выделяют следующие виды углеводных паренхиматозных дистрофий:
1. Гликогенозы.
2. Мукополисахаридозы.
3. Глюкопротеидозы.
Гликогенозы
Они могут быть наследственными и приобретенными.
Приобретенный особенно часто имеет место при сахарном диабете, когда происходит уменьшение гликогена в гепатоцитах, как результат его повышенного распада и превращения в глюкозу, которая накапливается в крови, лимфе и тканевой жидкости. Отмечается также повышенная глюкозурия (выход глюкозы в мочу).
А также накопление гликогена в эпителии почечных канальцев как результат усиленной инфильтрации глюкозы в эпителий почечных канальцев.
Наследственные гликогенозы
Это группа болезней, при которых не происходит полного расщепления гликогена вследствие дефицита ферментов. Гликоген накапливается в цитоплазме гепатоцитов, миокардиоцитов, в эпителии почечных канальцев, скелетной мускулатуре, в клетках кроветворной ткани.
Клинико-патоморфологические варианты болезни:
1. Паренхиматозный: поражаются печень и почки.
2. Мышечно-сердечный: поражаются скелетная мускулатура и сердце.
3. Паренхиматозно-мышечно-сердечный: поражаются печень, почки, скелетная мускулатура, миокард.
4. Паренхиматозно-кроветворный: поражаются печень, почки, селезенка, лимфатические узлы.
Патоморфология: органы увеличены в размерах, особенно печень, селезнка, цвет органов - бледный. Микроскопически отмечается увеличение клеток в размерах и накопление гликогена.
Биохимические особенности - в клетках может накапливаться обычный гликоген, длинный гликоген и короткий гликоген.
Мукополисахаридозы
Подробное описание в разделе мезенхимальные дистрофии.
Глюкопротеидозы
1. Приобретенные.
2. Наследственные.
1. Приобретенные.
Слизистая дистрофия
Коллоидная дистрофия
Слизистая дистрофия-накопление слизистых масс в цитоплазме клеток. Отмечается при респираторных инфекциях, бронхиальной астме в эпителии бронхов, в раковых клетках при слизистом раке желудка. Макроскопически – признаки ослизнения, микроскопически - появление перстневидных клеток (клеток цитоплазма которых заполнена слизью, а ядро оттеснено на периферию и сплющено, почему клетка напоминает перстень).
Коллоидная дистрофия отмечается при коллоидном зобе и коллоидном раке. Исход процесса – обратное развитие или гибель клетки с последующими склерозом и атрофией.
2. Наследственные.
Особая болезнь – муковисцидоз.
Мукос- слизь, вискус- птичий клей.
Главное: накопление густой вязкой слизи, которая вырабатывется эпителием слизистых органов дыхания и желудочно - кишечного тракта. В результате происходит образование кист и развитие воспалительных процессов и некроза.
Лекция 3. Дистрофии
1. Определение, этиология, классификация, общая характеристика
Под дистрофией (дегенерацией, перерождением ) понимают патологические изменения в органах, возникающие в результате нарушения в них обмена веществ. Это качественные изменения химического состава, физико-химических свойств и морфологии клеток и тканей организма, связанные с нарушением обмена веществ.
Дистрофии относят к повреждениям, или альтеративным процессам: это изменение структуры клеток, межклеточного вещества, тканей и органов, которое сопровождается нарушением их жизнедеятельности. Эти изменения как филогенетически наиболее древний вид реактивных процессов встречается на самых ранних этапах развития живого организма.
Повреждения способны вызвать самые разнообразные причины. Они воздействуют на клеточные и тканевые структуры непосредственно или через гуморальные и рефлекторные влияния. Характер и степень повреждения зависят от силы и природы патогенного фактора, строения и функции органа, а также от реактивности организма. В одних случаях возникают поверхностные и обратимые изменения, касающиеся ультраструктур, а в других – глубокие и необратимые, которые могут завершиться гибелью не только клеток и тканей, но и целого органа.
В основе дистрофии лежит нарушение метаболизма клеток и тканей, ведущее к структурным изменениям.
Непосредственной причиной развития дистрофий могут служить нарушения как клеточных, так и внеклеточных механизмов, обеспечивающих трофику:
1) расстройство ауторегуляции клетки (токсин, радиация, отсутствие ферментов) приводят к дефициту энергии и нарушению ферментативных процессов в клетке;
2) нарушение работ транспортных систем, обеспечивающих метаболизм и структуру клеток, вызывает гипоксию, которая является ведущей причиной в патогенезе дистрофии;
3) расстройство эндокринной регуляции трофики или нарушение нервной регуляции трофики ведут к эндокринной или нервной дистрофии.
Бывают и внутриутробные дистрофии.
При дистрофиях в клетках или вне их накапливаются продукты обмена (белки, жиры, углеводы, минеральные вещества, вода), которые характеризуется количественными или качественными изменениями.
Среди морфологических механизмов, ведущих к развитию характерных для дистрофий изменений, различают инфильтрацию, декомпозицию, извращенный синтез и трансформацию.
Первые два – ведущие морфологические механизмы дистрофии.
Характерная морфология дистрофий выявляется, как правило, на клеточном и тканевом уровнях.
Дистрофические процессы наблюдаются как в цитоплазме и ядре, так и в межклеточной субстанции и сопровождаются нарушением строения клеток и тканей, а также расстройством их функции.
Дистрофия – процесс обратимый, но может привести к необратимым изменениям в клетках и тканях, вызвать их распад и гибель.
В морфологическом отношении дистрофии проявляются нарушением строения, прежде всего ультраструктуры клеток и тканей, когда нарушается регенерация на молекулярном и ультраструктурном уровнях. При многих дистрофиях в клетках и тканях обнаруживают включения «зерна», камни или кристаллы различной химической природы, которые в обычных условиях не встречаются или их количество увеличивается по сравнению с нормой. В других случаях происходит уменьшение количества соединений до исчезновения (жира, гликогена, минеральных веществ).
Структура клетки утрачивается (мышечная ткань – поперечную исчерченность, железистые клетки – полярность, соединительная ткань – фибриллярную структуру и т. д.). В тяжелых случаях начинается дискомплексация клеточных элементов. Микроскопически изменяется цвет, величина, форма, консистенция, рисунок органов.
Изменение внешнего вида органа послужило основанием назвать этот процесс перерождением или дегенерацией – термином, не отражающим сущности дистрофических изменений.
Классификация дистрофий связана с видом нарушенного обмена веществ. Поэтому различают белковые дистрофии (внутриклеточные диспротеинозы, внеклеточные и смешанные); жировые (мезенхимальные и паренхиматозные), углеводные (нарушение обмена гликогена), минеральные (камни – конкременты, нарушение обмена кальция).
По распространенности их делят на общие, системные и местные; по локализации – паренхиматозные (клеточные), мезенхимальные (внеклеточные) и смешанные; по влиянию генетических факторов – приобретенные и наследственные.
Дистрофии относятся к числу обратимых процессов, но могут приводить к некрозу.
Этиология дистрофий: действия многих внешних и внутренних факторов (биологически неполноценное кормление, различные условия содержания и эксплуатации живых, механические, физические, химические и биологические воздействия, инфекции, интоксикации, нарушения крово – и лимфообращения, поражения желез внутренней секреции и нервной системы, генетическая патология и др.).
Патогенные факторы действуют на органы и ткани или непосредственно или рефлекторно через нервно-гуморальную систему, регулирующую обменные процессы. Характер дистрофий зависит от силы, продолжительности и частоты воздействия того или иного болезнетворного раздражения на организм, а также реактивного состояния организма и вида поврежденной ткани.
Дистрофии отмечают при всех болезнях, но в одних случаях они возникают извечно и определяют характер болезни, а в других – представляют собой неспецифический или нефизиологический, сопутствующий заболеванию патологический процесс.
Функциональное значение дистрофий заключается в нарушении основных функций органа (например, синтез белка, углеводов, липопротеидов, при гепатозе, появление белка в моче при нефрозе, слабость сердца при дистрофии миокарда у больных ящуром и т. д.).
2. Белковая дистрофия (диспротеинозы), ее сущность и классификация
Сущность белковых дистрофий состоит в том, что белок тканевых элементов при дистрофиях часто отличается от нормы по внешним признакам: он или разжижен или очень уплотнен. Иногда изменяется синтез белков, нарушается их химическая структура. Нередко в тканях и клетках откладываются продукты белкового обмена, которые в здоровом организме вообще не обнаруживаются. В одних случаях процессы ограничиваются нарушением белков, входящих в состав клетки, а в других – нарушается структура белков, входящих в межклеточные вещества. К белковым диспротеинозам, протекающим главным образом в клетках, относятся так называемые внутриклеточные дистрофические процессы: зернистая дистрофия, гиалиново-капельная, гидропическая, роговая дистрофии.
К внеклеточным диспротеинозам относятся гиалиноз и амилоидоз; к смешанным – нарушение обмена нуклеопротеидов и глюкопротеидов.
3. Внутриклеточные диспротеинозы, их характеристика, исход и значение для организма
Зернистая дистрофия наиболее часто встречается из всех видов белковых дистрофий. Она проявляется самостоятельно или в качестве слагаемого воспалительного процесса. Причины зернистых дистрофий – различные интоксикации расстройства кроволимфообращения, инфекционные болезни, лихорадочные состояния и др. Все эти факторы могут снижать окислительные процессы и способствовать накоплению кислых продуктов в клетках.
Зернистая дистрофия встречается во многих органах, наиболее ясно выражена в паренхиматозных: в почках, сердечной мышце, в печени, поэтому ее называют еще паренхиматозной.
Патолого – анатомические признаки: при внешнем осмотре орган незначительно увеличен, форма сохранена, консистенция обычно дряблая, цвет, как правило, на много бледнее, чем в норме, рисунок на поверхности разреза сглажен.
При разрезе, в частности почки, печени, вследствие набухания края этих органов могут значительно выпячиваться за края соединительно – тканной капсулы. При этом поверхность разреза мутная, тусклая, лишенная естественного блеска. Например, мышца сердца имеет сходство с видом мяса, ошпаренного кипятком; это дало основание многим исследователям при описании признаков зернистой дистрофии говорить, что мышца имеет вид вареного мяса. Мутность, тусклость, набухание органов являются весьма характерными признаками для этого вида дистрофии. Поэтому зернистую дистрофию называют еще мутное набухание. У животных при усиленном питании вскоре после кормления иногда появляются изменения в почках и в печени такие же, как и при зернистой дистрофии, мутность, тусклость, но выраженные в слабой степени. При зернистой дистрофии клетка набухшая, цитоплазма заполнена мелкой, едва заметной белковой зернистостью. При воздействии слабым раствором уксусной кислоты на такую ткань зернистость (белковая) исчезает и больше не возникает. Это указывает на белковый характер зернистости. То же самое наблюдается при исследовании мышечных волокон сердца. В мышце появляется белковая зернистость, располагающаяся между фибриллами. Волокна набухают, а поперечная исчерченность мышечных волокон при дальнейшем развитии процесса утрачивается. И если процесс на этом не прекращается, то может наступить распад волокна. Но зернистая дистрофия редко захватывает всю мышцу сердца, чаще процесс возникает на поверхности или внутренней части в миокарде левого желудочка; она имеет очаговое распространение. Измененные участки миокарда имеют серовато-красный цвет.
В патологии существует суждение о двух стадиях развития этого процесса. Одни считают, что мутное набухание – это первичная стадия зернистой дистрофии, а резко выраженные явления некробиотических изменений с некрозами клеток – это зернистая дистрофия. Такое деление процессов дистрофии является условным и не всегда оправданным. Иногда и при мутном набухании почек происходит некроз клеток.
Сущность процесса при дистрофии заключается в усиленном распаде белков, жиров, углеводов с возникновением кислой среды, с усиленным поглощением воды и задержкой в клетках продуктов обмена. Все это приводит к набуханию коллоидов и изменению вида группы крупнодисперсных белков, которые содержатся в цитоплазме клеток этих органов.
Особенно значительные изменения при белковых дистрофиях и, в частности, при зернистой дистрофии возникают в митохондриях. Известно, что в этих органоидах происходят окислительно-восстановительные процессы. В норме в зависимости от интенсивности окислительно-восстановительных процессов возникает значительная изменчивость форм и размеров митохондрий. А при патологических состояниях, особенно сопровождающихся гипоксией, наступает набухание митохондрий, они увеличиваются в размерах, их наружные мембраны растягиваются, а внутренние отодвигаются одна от другой, и появляются вакуоли. В этой стадии вакуолизация митохондрий обратима. При более интенсивном и длительном развитии процесса вакуолизация может приводить к необратимым некробиотическим изменениям и к некрозу.
Исходы зернистой дистрофии зависят от степени повреждения клеток. Начальная стадия этой дистрофии обратимая. В дальнейшем, если причины, вызвавшие ее, не устранены, то может наступить некроз или более тяжелый вид нарушения обмена – жировая, гидропическая дистрофия.
При длительном течении процесса, например при лихорадке, происходят не только дистрофии клеток, но и возникают некрозы. Последние имеют вид светлых участков.
Изменения при зернистой дистрофии иногда сходны с трупными изменениями. Но при трупных изменениях не будет набухания клеток, в то время как при зернистой дистрофии – неравномерное набухание клеток с одновременным наличием в органе неизменных участков тканей. Этим постмортальные изменения отличаются от зернистой дистрофии.
Гиалиново-капельная дистрофия характеризуется нарушением белкового обмена, протекает в цитоплазме с образованием крупных капель белкового характера. Вначале эти капли единичные, небольшие, ядро в клетке не нарушено. При дальнейшем действии причины, вызывающей этот процесс, капли увеличиваются в объеме и в количестве, ядро отодвигается в сторону, а затем, по мере дальнейшего образования капель, постепенно исчезает. Белковые отложения в цитоплазме приобретают гомогенный вид, похожий на гиалиновый хрящ. Митохондрии-набухшие или в состоянии распада. Белковые капли, возникающие в клетках, имеют гиалиновую структуру. Почки плотны, корковый слой серого цвета, тусклый, пирамиды красноватые. Чаще всего клетки в таких случаях приобретают характер мутного набухания с последующей денатурацией белков цитоплазмы клеток. Если же наступает гибель ядра, то это относится к некрозу клетки.
Гиалиново-капельная дистрофия чаще всего наблюдается в эпителии почечных канальцев, реже в печени. Иногда она сочетается с жировой дистрофией или с амилоидозом. Наблюдаются эти дистрофии при хронических инфекционных заболеваниях, интоксикации и отравлениях организма.
Водяночная (гидропическая, или вакуольная) дистрофия характеризуется тем, что клетки подвергаются растворению-разжижению. Вначале в цитоплазме, а иногда и в ядре видны вакуоли с жидкостью, а при дальнейшем развитии процесса вакуоли сливаются и вся цитоплазма заполняется жидкостью, в ней как бы плавает ядро, которое затем превращается в один пузырь, наполненный жидкостью. Такие клетки обычно гибнут. Межклеточное основное вещество и соединительная ткань набухают, и вся ткань разжижается. При водяночной дистрофии вакуоли видны на препаратах, обработанных спиртом, поэтому необходимо дифференцировать эти процессы от окраски на жир.
Водяночные дистрофии бывают при отеках, ожогах, при оспе, ящуре, вирусном гепатите, хронических неврозах и других септических заболеваниях.
Исход водяночной дистрофии благоприятный в начальных стадиях и при восстановлении нормального водного и белкового обмена, процесс легко обратимый, и клетки приобретают нормальный вид. Клетки, находящиеся в состоянии сильно выраженной гидропии, гибнут.
Вакуольная дистрофия определяется только при микроскопическом исследовании. Внешний вид органа не изменен, но цвет бледнее, чем в норме. Функция органов, как и при всяких дистрофиях, понижена. Вакуолизация чаще бывает в эпителии почек, клетках печени, кожи, лейкоцитах, в мышцах сердечной и скелетных, ганглиозных клетках ЦНС.
Патологическое ороговение или роговая дистрофия – избыточное (гиперкератоз) или качественно нарушенное (паракератоз, гипокератоз) образование рогового вещества.
Ороговение клеток-это физиологический процесс, который развивается в эпидермисе и характеризуется постепенным превращением плоского эпителия кожи в роговые чешуйки, образующие роговой слой кожи. Патологическое ороговение развивается в связи с заболеванием или повреждением кожи, слизистых оболочек. В основе этих процессов лежит избыточное образование рогового вещества кожи. Этот процесс носит название гиперкератоза. Иногда наблюдается разрастание рогового вещества в необычных местах-на слизистых. Иногда в опухолях, в эпителиальных клетках образуется роговое вещество при некоторых формах рака.
От физиологического ороговения патологическое отличается тем, что ороговение эпителия происходит на почве факторов, вызывающих усиленное образование рогового вещества. Часто встречается процесс гиперкератоза местного происхождения, который возникает при раздражении кожи, например неправильно пригнанной сбруей у лошади, длительное давление на кожу вызывают мозоли.
Паракератоз выражается в утрате способности клеток эпидермиса вырабатывать кератогиалин. Микроскопически при данном заболевании выявляют утолщение эпидермиса в результате гиперплазии клеток мальпигиевого слоя и избыточного накопления рогового слоя. При пара – и гипокератозе выражена атрофия зернистого слоя, роговой слой рыхлый, с дискомплексированными клетками, имеющими палочковидные ядра (неполное ороговение).
Макроскопически при паракератозе роговой слой утолщен, рыхлый, с повышенным слущиванием роговых чешуек. У взрослых животных, особенно у молочных коров, отмечают неправильный рост копытного рога, который утрачивает глазурь и растрескивается.
При лейкоплакии на слизистых оболочках образуются различного размера очаги ороговевшего эпителия в виде возвышающихся бляшек серо-белого цвета.
Исход роговой дистрофии зависит от течения основной болезни. При устранении причины, вызывающей патологическое ороговение, поврежденная ткань может восстанавливаться.
4. Внеклеточные и смешанные диспротеинозы
Внеклеточные диспротеинозы
Сюда относятся длительно протекающие патологические процессы в межуточном веществе соединительной ткани в связи с нарушением белкового обмена.
Причинами таких дистрофий могут быть различные инфекции и интоксикации, а также длительное употребление кормов, содержащих избыточное количество белков.
К внеклеточным диспротеинозам относятся: мукоидное, фибриноидное набухание, гиалиновая (гиалиноз) и амилоидная (амилоидоз) дистрофии.
Мукоидное набухание
Мукоидное набухание представляет собой поверхностную дезорганизацию соединительной ткани, начальную стадию ее изменений. При этом в основном веществе и в коллагеновых волокнах соединительной ткани происходит расщепление белково-полисахаридных комплексов и накопление кислых мукополисахаридов, которые обладают свойствами метахромазии, безофильной окрашиваемостью и гидрофильностью. Указанные вещества повышают тканевую и сосудистую проницаемость. Коллагеновые волокна при этом сохраняются, но меняется их окрашиваемость. При окраске пикрофуксином они оказываются не красными, а желто-оранжевыми. Эти изменения сопровождаются появлением лимфоцитарных и гистиолимфицитарных инфильтратов, мукоидное набухание обнаруживается только микроскопически. Эта дистрофия возникает в различных органах, но наиболее часто в артериях, клапанах сердца, эндокарде и эпикарде. Исход может быть двояким: полное восстановление ткани или переход в фибриноидное набухание. Причины: различные формы кислородной недостаточности, болезни обмена веществ и эндокринной системы.
Фибриноидное набухание
Фибриноидное набухание характеризуется дезорганизацией соединительной ткани, в основе которой лежит деструкция коллагена и основного межуточного вещества, и резким повышением сосудистой проницаемости. Процесс фибриноидного набухания представляет собой более тяжелую стадию дезорганизации соединительной ткани, чем при мукоидном набухании. Фибриноид наблюдается в строме органа, в стенке сосудов. Причем этот процесс совершается от поверхностной дезорганизации, т. е. от неглубоких изменений, до распада коллагеновой субстанции и основного вещества. При гистологическом исследовании нарушения коллагеновых волокон весьма значительны. Они становятся очень сильно набухшими, нарушается их волокнистая структура, приобретают при окрашивании свойства фибрина, поэтому этот процесс называют фибриноид, а также при этом выделяются белковые вещества типа фибрина. При фибриноидном набухании происходит дезорганизация соединительной ткани с перераспределением белка и мукополисахаридов. Причем, происходит деполяризация мукополисахаридов, растворение их. И в зависимости от того, какой степени достиг процесс распада, появляются и различные плазменные белки-альбумины, глобулины, фибриноген. Фибриноидное изменение представляет собой ряд состояний соединительной ткани, в основе которых лежит набухание, разрушение коллагена и образование патологических белковых соединений с мукополисахаридами и гиалуроновой кислотой.
Фибриноидный процесс чаще всего бывает необратимым, переходит в склероз или в гиалиноз. Значение фибриноидного набухания заключается в том, что включаются функции тканей, в которых развивается этот процесс.
Гиалиноз (гиалиновая дистрофия)
При этом виде нарушений белкового обмена между клетками появляется однородная, плотная, полупрозрачная белковая масса – гиалин.
Это вещество обладает значительной стойкостью: не растворяется в воде, спирте, эфире, кислотах и щелочах. Специальных реакций для обнаружения гиалина нет. В гистологических препаратах он окрашивается эозином или фуксином в красный цвет.
Гиалиноз не всегда явление патологическое. Он может происходить и как нормальное явление, например в яичниках при инволюции желтых тел и атрофии фолликулов, в артериях матки и послеродовом периоде, в селезеночной артерии у взрослых животных. При болезненных состояниях гиалиноз обычно наблюдается в исходе различных патологических процессов. Гиалиноз может быть местным и общим (системный).
Местная гиалиновая дистрофия
В старых рубцах, в капсулах, окружающих абсцессы, некрозы и инородные тела, происходит отложение гиалина. То же наблюдается при разрастании соединительной ткани в атрофирующихся органах, при хроническом интерстициальном воспалении, в тромбах, фиброзных спайках, в артериях со склеротическими изменениями.
Часто гиалиноз при внешнем осмотре органа ни в чем не проявляется и обнаруживается лишь при микроскопическом исследовании. В тех же случаях, когда гиалиноз выражен резко, ткань становится плотной, бледной и полупрозрачной.
Местное отложение гиалина может быть в собственных, или базальных, оболочках различных желез (в щитовидной, молочной, поджелудочной железах, в почках и т. д.), что чаще всего бывает при атрофических процессах и при наличии разрастания межуточной ткани. В этих случаях железистые пузырьки и канальцы оказываются окруженными вместо тонкой, еле заметной собственной оболочки толстым однородным кольцом гиалинового вещества. В эпителиальных клетках при этом обнаруживаются явления атрофии.
Гиалиновая дистрофия наблюдается и в органах, имеющих ретикулярную сеть, главным образом в лимфатических узлах. При этом ретикулярные волокна превращаются в массивные плотные тяжи, клеточные элементы между ними атрофируются и исчезают.
Процесс заключается в отложения по ходу ретикулярных волокон вначале жидкого, а затем уплотняющегося белка, который сливается с волокнами в однородную массу. В лимфатических узлах это наблюдается наиболее часто при атрофиях, хронических воспалениях, туберкулезе. При этом коллагеновые волокна набухают, сливаются в гомогенные тяжи. Клетки атрофируются.
Общий гиалиноз
Этот процесс приобретает особенно большое значение при отложении гиалина в стенках кровеносных сосудов. Он появляется в интиме и в периваскулярной ткани мелких артерий и капилляров. Происходит сужение или полная облитерация сосуда вследствие утолщения и гомогенизации стенки. Медиа атрофируется и замещается гиалинозными массами.
Гиалиноз сосудов и соединительной ткани может возникать двояким путем.
1. Происходит особое физико-химическое видоизменение волокнистого вещества с превращением его в однородную гиалиновую массу. Фибриллы соединительно – тканных пучков набухают и сливаются, фибриллярность теряется, пучки становятся однородными, бесструктурными. В дальнейшем соседние пучки сливаются, вследствие чего образуются более обширные гиалиновые поля. Соединительная ткань при этом приобретает весьма плотную, нередко хрящеобразную консистенцию.
2. Гиалиноз возникает в результате повышенной проницаемости сосудов и тканей. Происходит пропотевание белка из просвета сосудов, белок свертывается, уплотняется и приобретает вид стекловидной плотной массы. Указанный процесс обозначается как плазматическое пропитывание, или плазморрагия.
Гиалиноз, как правило, необратимый процесс, за исключением гиалинизации рубцовой соединительной ткани, в которой возможно разрыхление и рассасывание гиалина. Если процесс является местным, то особых функциональных нарушений не возникает. При значительном общем гиалинозе нарушаются функции органов, особенно сосудов.
Амилоидоз (амилоидная дистрофия)
Процесс заключается в том, что в тканях происходит отложнение белкового вещества, по химическому составу близкого к глобулинам (амилоид-протеин). Вещество это плотное, однородное, полупрозрачное, обладает стойкостью по отношению к кислотам, щелочам, желудочному соку, к аутолизу и гниению. Амилоид во многом сходен с гиалином, но отличается от него и других белков некоторыми химическими реакциями.
· Реакция с йодом и серной кислотой. Если на поверхность разреза органа, подвергшегося амилоидозу, подействовать люголевским раствором, то участки скопления амилоида окрашиваются в красно-бурый или буро-коричневый цвет. При последующем воздействии 10 %-ой серной кислоты амилоид приобретает сине-фиолетовый цвет и через некоторое время становится грязно-зеленым.
· Окраска метилвиолетом и генциаивиолетом придает амилоиду красный цвет, а тканям – фиолетовый.
· Окраска красным конго. Амилоид окрашивается в буровато-красный цвет, а ткани – в бледно-розовый или вовсе не окрашиваются.
Иногда указанные реакции не дают положительных результатов. Объясняется это изменениями химического состава амилоида. Неокрашивающееся амилоидное вещество называется ахроамилодом. Отложения его становятся похожими на гиалиновые.
При отложении небольших количеств амилоида внешний вид органа не изменяется. Если же процесс становится резко выраженным, орган увеличивается, становится плотным, ломким, малокровным; на разрезе имеет своеобразный полупрозрачный, восковидный или сальный вид. При микроскопии устанавливается, что вначале амилоидное вещество откладывается обычно в стенках мелких кровеносных сосудов, под аргирофильной мембраной эндотелия, а также по ходу ретикулярных волокон и под базальной мембраной эндотелия.
Амилоидная дистрофия может быть общей, распространенной, когда процесс захватывает несколько органов. В других случаях она местная: ограничивается каким-либо одним местом.
Амилоидоз селезенки бывает фолликулярный и диффузный.
А. При фолликулярной форме отложения амилоида происходят вначале по периферии фолликулов в ретикуломе, а затем распространяются на весь фолликул. Лимфоциты вытесняются.
Центральная артерия утолщена, имеет гомогенный вид. Макроскопически обнаруживается, что селезенка умеренно увеличена. На разрезе видны измененные фолликулы в виде зерен вареного саго («саговая селезенка»).
Б. При диффузной форме амилоид откладывается в фолликулах и красной пульпе. Первоначально появляются отдельные, неправильной формы островки, которые затем сливаются в сплошную массу. Клетки атрофируются. Селезенка увеличена, плотная (только у лошадей тестообразная). Поверхность разреза светлого красно-коричневого цвета напоминает ветчину («сальная, или ветчинная, селезенка»).
Амилоидоз печени. Изменения распространяются от периферии к центру долек. Вначале амилоид откладывается между эндотелием внутридольковых капилляров и печеночными балками, а также в стенках междольковых сосудов. По мере нарастания процесса образуются сплошные участки амилоидных масс, а печеночные клетки атрофируются. Печень увеличена, плотная, бледно-коричневая. Только у лошадей она дряблая и легко рвется.
Амилоидоз почек. Процесс начинается с клубочков. Амилоид откладывается под аргирофильными мембранами интимы артерий, артериол и сосудистых петель клубочков. Накопляются глыбки, сдавливающие петли. Постепенно весь клубочек замещается амилоидом. Амилоидоз распространяется также в стенках сосудов коркового и мозгового вещества под мембраной канальцевого эпителия. В эпителии канальцев происходят дистрофические изменения и атрофия. Почки увеличены, плотны, поверхность разреза восковидная. Причины амилоидной дистрофии различные. Сюда относятся хронические инфекционные заболевания, при которых имеют место нагноения и некрозы, например актиномикоз, туберкулез; реже это происходит при хронических болезнях, протекающих без нагноения и некрозов. Причиной амилоидоза может быть продолжительное и обильное употребление кормов, богатых белками (например, откармливание гусей). Как правило, этот вид дистрофии наблюдается у лошадей – продуцентов сывороток.
Исход общего амилоидоза неблагоприятный, так как в измененных органах происходят дистрофические изменения атрофия и некроз паренхимы.
Смешанные диспротеинозы
Смешанные диспротеинозы – это нарушение белкового обмена клетки и межклеточного вещества. Дистрофические процессы возникают при нарушении обмена сложных белков – нуклеопротеидов, гликопротеидов и хромопротеидов.
Нарушение обмена нуклеопротеидов
Нуклеопротеиды состоят из белка и нуклеиновых кислот (ДНК и РНК). Конечным продуктом обмена нуклеопротеидов являются мочевая кислота и ее соли. В нормальных условиях эти продукты распада в растворенном состоянии выделяются из организма преимущественно почками. При нарушении обмена нуклеопротеидов происходит избыточное образование мочевой кислоты, и ее соли откладываются в тканях; наблюдается это при мочекислом диатезе и мочекислом инфаркте почек.
Мочекислый диатез – отложение мочекислых солей в различные ткани и органы. Обычно это отмечают на суставных поверхностях пальцев конечностей, в сухожилиях, в хрящах ушной раковины, почках и на серозных покровах. На месте отложения кристаллов мочевых солей тканевые элементы подвергаются некрозу, вокруг омертвевших участков развивается воспалительная реакция с разрастанием соединительной ткани.
Чаще мочекислым диатезом заболевают птицы (куры, утки), реже – млекопитающие. У птиц мочекислые соли в виде густой беловатой массы откладываются на серозных оболочках грудобрюшной полости, на перикарде и эпикарде, в почках и на суставных поверхностях пальцев ног. Под наложениями выявляется воспаленный серозный покров. Почки увеличены в объеме, усеяны беловатым налетом, а на поверхности разреза обнаруживаются беловато-серые или желтовато-белые очажки. Под микроскопом видны лучистые кристаллы уратов; эпителий почечных канальцев в состоянии зернистой дистрофии и некроза, а строма инфильтрирована лимфоидными и гигантскими клетками. Поражение, характеризующееся отложением мочекислых солей в суставы пальцев ног, называется подагрой. При этом суставы опухают, деформируются, образуются плотные узлы.
Мочекислый инфаркт почек – физиологическое состояние, встречающееся у новорожденных животных в первые семь суток, после чего оно исчезает. Связано это с изменением обменных процессов. В крови временно повышается концентрация мочевой кислоты, которая полностью не успевает выделяться с мочой из организма. Макроскопически на поверхности разреза почек в мозговом слое радиально располагаются красновато-желтые полоски, представляющие собой скопление мочевых солей в просвете прямых канальцев и в строме почек. У взрослых животных при воспалении и некрозе слизистой оболочки мочевого пузыря и почечной лоханки может быть инкрустация (вкрапление) мочекислых слей в омертвевшую ткань.
Отложение мочевой кислоты в органах вызывает необратимые (некротические) изменения пораженных тканей.
Нарушение обмена гликопротеидов
Гликопротеиды – сложные соединения белка с полисахаридами, содержащими гексозы, гексозамины и гексуроновые кислоты.
Слизистая дистрофия как патологический процесс имеет место в эпителиальных клетках слизистых оболочек, клетках ряда желез и соединительной ткани. Она является следствием нарушения обмена глюкопротеидов и характеризуется накоплением в клетках муцинов и мукоидов. В эпителии слизистая дистрофия может быть следствием гиперсекреции слизистых желез с повышенным слущиванием эпителиальных клеток и превращением их в слизеподобную массу. В соединительной ткани слизистой дистрофии подвергается межуточное вещество, в котором накапливаются мукоидные субстанции.
В присутствии воды слизь набухает, а от добавления уксусной кислоты или спирта осаждается и выпадает в виде тонкой, нежной волокнистой сети. Этим слизь отличается от слизеподобных веществ (мукоидов), образующихся в тканях как в нормальных, так и в патологических условиях. Слизь, как и амилоид, обладает метахромозией. Так, при окраске крезилвиолетом, тионином нормальная ткань окрашивается в синий, а слизь – в красный цвет.
Слизистая дистрофия эпителиальных клеток бывает хорошо выражена при катаральных воспалениях в слизистых оболочках, особенно органов дыхания и пищеварения. В физиологических условиях выделение слизи – продукта секреции бокаловидных клеток – происходит следующим образом. Сначала в клетках появляются мельчайшие прозрачные капельки слизи, которые, сливаясь между собой, образуют капли большей величины. Клетка увеличивается в объеме, разбухает, и наконец слизь изливается в виде секрета после чего клетка спадается и восстанавливает свой прежний вид. Затем на ней снова начинают появляться капельки слизи.
Слизистая дистрофия эпителиальных клеток сопровождается усиленным образованием и отделением слизи, некрозом и отторжением омертвевших эпителиальных клеток, остатки которых примешиваются к слизи.
Слизистой дистрофии могут подвергаться различные виды соединительной ткани, в том числе хрящи и кости, а также опухоли соединительнотканого типа. В соединительной ткани происходит набухание и как бы растворение фибрилл.
В костях при слизистой дистрофии вначале исчезает известь, а затем происходит разжижение остеоидной субстанции. Измененная ткань под микроскопом представляется в виде однородной бесструктурной массы, из которой под действием кислот и спирта выпадают нити муцина. Наиболее частой причиной, способствующей появлению слизистой дистрофии соединительной ткани, является нарушение трофики тканей при хронических инфекционных заболеваниях, интоксикациях, нарушениях эндокринных желез и опухолях.
При устранении причин, вызвавших слизистую дистрофию, происходит восстановление ткани.
5. Нарушение обмена хромопротеидов (пигментов). Экзогенные и эндогенные пигменты
Всем тканям и органам животных свойственна определенная окраска – пигментация. Одни пигменты находятся в тканях в растворенном состоянии, другие имеют вид зернистых, аморфных и кристаллических отложений. Все они образуются самим организмом, обнаруживаются в физиологических условиях и называются эндогенными. Кроме того, при некоторых патологических условиях в организм животного и человека могут проникать не свойственные ему в норме пигменты из внешней среды. Они называются экзогенными.
Эндогенные пигменты подразделяются в свою очередь на три группы в зависимости от источника своего образования.
1. Гемоглобиногенные, которые возникают из гемоглобина при его различных превращениях. Сюда относятся изучаемые в патоморфологии ферритин, гематоидин, гемосидерин и билирубин.
2. Протеиногенные пигменты, которые не имеют отношения к гемоглобину и являются производными тирозина и триптофана. К ним относят меланин, андренохромы и пигмент энтерохромафинных клеток.
3. Липидогенные пигменты, связанные с обменом жиров. Сюда относятся липохромы, липофусцин и цероид.
Гемоглобиногенные пигменты образуются в результате физиологического и патологического распада эритроцитов, в состав которых входит высокомолекулярный хромопротеид гемоглобин, придающий крови специфическую окраску.
Ферритин – резервный железопротеид. Образуется из пищевого железа в слизистой оболочке кишечника и поджелудочной железе и при распаде эритроцитов и гемоглобина в селезенке, печени, костном мозге и лимфоузлах. В этих органах его можно выделить гистохимической реакцией на берлинскую глазурь.
Гемосидерин – мелкозернистый, аморфный железосодержащий пигмент золотисто-бурого или коричневого цвета. Располагается внутриклеточно, а в случаях распада клеток свободно лежит в тканях. Гемосидерин образуется клетками при фагоцитозе эритроцитов или из растворенного в плазме гемоглобина. Появление гемосидерина в тканях называется гемосидерозом, который бывает общим и местным.
Общий гемосидероз возникает при внутрисосудистом гемолизе, например при сепсисе, инфекционной анемии лошадей, пироплазмозе, при некоторых отравлениях (мышьяк, фосфор и др.). Освободившийся из эритроцитов гемоглобин растворяется в плазме и частично выделяется с мочой. Другая часть поглощается клетками ретикуло-эндотелия и превращается в гемосидерин, возникает общий гемосидероз. Гемосидерин образуется только внутриклеточно. Отложения гемосидерина происходят прежде всего в селезенке, затем в печени, костном мозге, в лимфатических узлах, а также в почках в порядке выделительной функции. Указанные органы принимают гемосидерин, обнаруживаются в клетках ретикулоэндотелия и в эпителии извитых канальцев почек. Гемосидерин растворим в кислотах, не растворим в щелочах, спирте и эфире, не обесцвечивается перекисью водорода. Для дифференциации гемосидерина от других внутриклеточных включений применяются следующие реакции.
· Реакция Перлса: при обработке гистологических срезов железосинеродистым калием (желтая кровяная соль) в присутствии соляной кислоты пигмент окрашивается в зеленовато-синий цвет («берлинская глазурь»).
· От прибавления сернистого аммония гемосидерин чернеет, а при дальнейшей обработке железосинеродистым калием и соляной кислотой пигмент приобретает синий цвет («турнбулева синь»).
Местный гемосидероз отмечается при внесосудистом гемолизе эритроцитов, что наблюдается при кровоизлияниях. Гемосидерин накапливается в цитоплазме клеток по периферии кровоизлияния.
Гематоидин тоже образуется при распаде гемоглобина. Этот пигмент железа не содержит, имеет форму кристаллов, которые выглядят как ромбические образования или напоминают пучки игл ярко – оранжевого цвета. При скоплении пигмента возникают разнообразные фигуры в виде звездочек, метелок, снопов и т. д. Реже гематоидин встречается в виде аморфной зернистости или глыбок. Этот пигмент растворяется в щелочах, разлагается крепкой азотной и серной кислотами, трудно растворим в спирте и эфире, перекисью водорода не обесцвечивается.
Гематоидин образуется в центральных частях кровоизлияний, где нет клеток и доступа кислорода.
Билирубин. Этот пигмент постоянно образуется и постоянно претерпевает различные превращения, участвуя в метаболизме нормального организма. Он образуется в ретикулоэндотелиальной системе при физиологическом разрушении эритроцитов, поступает в печень и там включается в состав желчи, формируемой печеночными клетками. Билирубин растворен в желчи и обусловливает свойственное ей окрашивание. По своим свойствам этот пигмент близок к гематоидину и дает положительную реакцию Гмелина: при воздействии азотной кислоты образуются цветные кольца. В норме желчь находится в желчных протоках и желчном пузыре, откуда выводится в двенадцатиперстную кишку. При патологических условиях нарушается нормальное образование и выделение желчи; билирубин поступает в кровь, что сопровождается окрашиванием тканей в желтый цвет. Такое желтое окрашивание всех органов, а в особенности склеры глаз, видимых слизистых оболочек, серозных покровов и интимы сосудов, называется желтухой, которая по происхождению и патогенезу делится на три вида: гемолитическую, паренхиматозную и механическую.
· Гемолитическая желтуха возникает при внутрисосудистом гемолизе эритроцитов. Большие количества продуктов распада гемоглобина поступают в клетки ретикулоэндотелиальной системы. Так усиленно продуцируется билирубин или близкий к нему пигмент, поступающий непосредственно в кровь.
· Паренхиматозная желтуха обусловлена нарушением оттока желчи из печени, который возникает вследствие нарушения функции печеночных клеток. Эти клетки утрачивают способность выделять желчь в желчные капилляры, поэтому желчь диффундирует в кровь через стенки кровеносных и лимфатических капилляров. Причины паренхиматозных желтух различные. Это главным образом инфекционные болезни и отравления.
Протеиногенные пигменты включают в себя меланин, андренохомы и пигмент энтерохоминных клеток.
Меланин – этот пигмент обусловливает окраску кожи, волос, оперения птиц, глаз. В норме содержание меланина зависит от вида животного, породы, возраста и индивидуальных его особенностей. При микроскопии меланин обнаруживается в виде бурых или черных зернышек, лежащих в протоплазме клеток. В химическом отношении меланопротеид содержит серу, углерод и азот, но лишен железа и жира. В кислотах и щелочах он не растворяется, окрашивается азотнокислым серебром в черный цвет и обесцвечивается от действия перекиси водорода. Образование меланина происходит в клетках мальпигиева слоя эпидермиса и сетчатки глаза. Клетки, образующие меланин, называются меланобластами.
Нарушения меланогенеза проявляются повышенным образованием меланина, накоплением его в несвойственных местах, исчезновением или отсутствием пигмента. Данные расстройства могут быть приобретенными или врожденными и носить распространенный или местный характер.
Избыточное образование меланина в коже и отложение его во внутренних органах называют общим меланозом. Встречается он чаще у крупного и мелкого рогатого скота, особенно у телят и овец. Считают, что этот процесс кормового происхождения. Меланин откладывается в печени, легких и на серозных покровах, реже – в оболочках головного и спинного мозга, которые приобретают темно-коричневый или буро-черный цвет.
Местная избыточная пигментация кожи связана с доброкачественным или злокачественным разрастанием меланобластов с образованием меланом.
Они нередко возникают у лошадей серой масти и у собак. Источники появления их – родимые пятна.
Врожденное недостаточное образование меланина или его полное отсутствие в организме называется альбинизмом. Такое состояние свойственно некоторым видам и породам животных (белые мыши, крысы, кролики и др.).
Местную врожденную депигментацию кожи обозначают термином vitiligo. В некоторых случаях после длительных воспалений и других поражений (ранения, язвы, случная болезнь лошадей) на коже образуются беспигментные пятна, называемые лейкодермией.
Липидогенные пигменты. Сюда относятся липохромы, липофусцин и цероид. В их состав входят жировые и белковые вещества.
Липофусцин – гликолипопротеид, имеет вид зерен или глыбок бурого цвета. Образование его связано с окислительным процессом – аутооксидацией фосфолипидов и жиров. Окрашивается суданом III и шарлахом в красный цвет, не дает реакции на железо. В кислотах и щелочах не растворяется; от азотнокислого серебра в противоположность меланину не чернеет. У животных липофусцин обнаруживают в сердечной, скелетной и гладкой мускулатуре, в почках, надпочечниках, печени, нервных клетках, семенных пузырьках и семенниках.
Патологическая пигментация липофусцином обычно проявляется при атрофии сердечной мускулатуры, печени, почек и в клетках центральной нервной системы.
Пигменты гемофусцина, обнаруживаемого в печени у лошадей при инфекционном энцефаломиелите, и цероида, образование которого связано с гиповитаминозом Е, по физико-химическому составу идентичны липофусцину.
Липохромы – пигменты желтого цвета, придающие желтую окраску жировой клетчатке, коре надпочечников, желтку яиц, сыворотке крови и т. д. К липохромам также относится лютеин – пигмент желтого тела яичника. Эти пигменты растворяются в реактивах – жирорастворителях и представляют собой липид, в которых растворены окрашенные углеводороды – каротиноиды и флавины. Образование липохрома и лютеина связано с метаболизмом жира и белков. При атрофии жировой клетчатки у старых и истощенных животных жир приобретает насыщенно желтый цвет.
Экзогенные пигменты
Так называются различные окрашенные вещества, попадающие в организм из внешней среды, которые могут менять естественную окраску органов или придавать им другой оттенок. Чаще всего экзогенные пигменты наблюдаются в легких, регионарных лимфатических узлах, реже – в селезенке, печени, почках. Отложение посторонних материалов в легких называется пневмокониозом. Это может наблюдаться при продолжительном пребывании животных в местах, где воздух загрязнен пылевыми частицами различного происхождения. Наибольшее значение имеет запыление легких угольной пылью – антракоз.
Под плеврой и внутри легочных долей находятся скопления угля в виде участков черного цвета или в виде диффузного запыления. Под микроскопом угольные частицы видны вокруг кровеносных сосудов, в альвеолярном эпителии и интерстиции. Угольная пыль скопляется также в средостенных и бронхиальных лимфатических узлах. При значительном отложении угольные частицы своим действием могут вызывать воспалительные изменения в легких с последующим разрастанием соединительной ткани. При запылении легких известковыми частицами появляются беловатые очаги (халикоз). Если легкие запыляются кремнеземом, глиноземом или глыбками кварца, возникает силикоз, который сопровождается склерозом легких.
В случае продолжительного лечения животных препаратами, содержащими серебро, последнее откладывается в эпителии сосудистых клубочков, в базальную мембрану почечных канальцев (аргироз почек). Соли серебра обнаруживаются также в печени, клетках Купфера и в стенках сосудов. Макроскопически ткани при аргирозе приобретают серую (стальную) окраску.
Как можно переесть до дистрофии. Наше тело состоит из разных тканей, но две в них известны всем – жировые отложения и мускулы. Про жировые отложения сказано очень много, и все не самое хорошее, про мускулы тоже – только уже с самым благожелательным отношением.Это две
Из книги Гомеопатическая клиническая фармакология автора Эрнст Фаррингтон33-я ЛЕКЦИЯ Rubiaceae - Мареновые Rubiaceae:1. Rubia titctoiria (Марена).2. Galium (Тоже красная краска).3. Cinchona.4. Ipecacuanha.5. Coffea.6. Mitchella.7. Gambier.Сегодня перед нами семейство растений, из которого мы получаем три очень ценных средства, Cinchona, Ipecacuanha и Coffea. Это семейство дает нам также Gambier (Gambogia,
Из книги История медицины: конспект лекций автора Е. В. Бачило35-я ЛЕКЦИЯ Scrophulariaceae - Норичниковые China. Из этого семейства растений мы получаем Digitalis, Gratiola, Leptandra viginica, Euphrasia, Verbascum и Linaria. У нас имеется немного симптомов для каждого из этих средств, и те, которые известны, достаточно определенны, чтобы их легко запомнить. Важнейшим
Из книги Патологическая анатомия автора Марина Александровна Колесникова37-я ЛЕКЦИЯ Solanaceae - Пасленовые Solanaceae:1. Belladonna.2. Hyoscyamus.3. Stramonium.4. Solan um nigr.5. Tabacum.6. Dulcamara.7. Capsicum.Средства, образующие эту группу по своей симптоматологии очень сходны друг с другом. Едва ли найдется хоть один симптом у этих средств, который не встречался бы почти в том же виде
Из книги Практическая гомеопатия автора Виктор Иосифович Варшавский42-я ЛЕКЦИЯ Минеральная группа В прилагаемой таблице я разместил для вашего изучения элементы по их взаимному соотношению до некоторой степени так же, как мы находим это в химии. Поэтому они не расположены в порядке, принятом в фармакологии. Но ведь это не абсолютный
Из книги Общая патологическая анатомия: конспект лекций для вузов автора Г. П. ДемкинЛЕКЦИЯ № 1. Вводная лекция. Медицинская символика различных времен и народов История медицины – это наука о развитии, совершенствовании медицинских знаний, медицинской деятельности разных народов мира на протяжении всей истории человечества, которая находится в
Из книги Медитативные упражнения для глаз для восстановления зрения по методу профессора Олега Панкова автора Олег Панков3. Паренхиматозные и белковые дистрофии Паренхиматозные дистрофии делятся на белковые, жировые и углеводные.Белковая дистрофия – это дистрофия, при которой нарушается белковый обмен. Процесс дистрофии развивается внутри клетки. Среди белковых паренхиматозных
Из книги Тренинги и игры для мышц глаз. Уникальные упражнения для восстановления зрения по методу профессора Олега Панкова автора Олег Панков6. Смешанные дистрофии О смешанных дистрофиях говорят в тех случаях, когда морфологические проявления нарушенного метаболизма накапливаются как в паренхиме, так и в строме, стенке сосудов и тканей. Они возникают при нарушении обмена сложных белков – хромо-протеидов,
Из книги Верни себе зрение. Лекции о естественном восстановлении зрения автора Владимир Георгиевич ЖдановПОРАЖЕНИЯ МЫШЦЫ СЕРДЦА (ПОРОКИ СЕРДЦА, ДИСТРОФИИ МИОКАРДА, АТЕРОСКЛЕРОЗ, НЕДОСТАТОЧНОСТЬ КРОВООБРАЩЕНИЯ) Арника 3Х, 3 - при гипертрофии миокарда, вызванной его перегрузкой.Аурум - гипертрофия миокарда при гипертонической болезни, атеросклерозе.Барита карбоника 3, 6, 12 -
Из книги автораЛекция 5. Минеральные дистрофии 1. Рахит, остеомаляция, фиброзная остеодистрофия 2. Камни и конкременты, их морфологическая характеристика, химический состав и значение для организма животных 3. Углеводная дистрофия 1. Рахит, остеомаляция, фиброзная
Из книги автораКоррекция зрения при близорукости, астигматизме, дистрофии сетчатки, глаукоме Эти упражнения способствуют развитию чувствительности центральной ямки (макулы) сетчатки, увеличению остроты зрения и улучшению кровоснабжения глаз, тренируют все шесть глазных мышц и
Из книги автораТренинг «Знак в овале» при близорукости, дистрофии сетчатки, глаукоме, косоглазии Эти упражнения способствуют развитию чувствительности центральной ямки (макулы) сетчатки, увеличению остроты зрения и улучшению кровоснабжения глаз.Упражнение 1 Смотрите на центральную
Из книги автораЛекция 1 Еще раз здравствуйте, уважаемые соратники.Начинаем наше первое занятие в Народном университете здорового образа жизни по методу Геннадия Андреевича Шичко. Курс будет посвящен коррекции зрения по методу Шичко-Бейтса. Это курс общего оздоровления и избавления от
Из книги автораЛекция 2 Итак, здравствуйте, уважаемые соратники.Начинаем наше второе занятие в Народном университете здорового образа жизни по методу Геннадия Андреевича Шичко. Курс посвящен коррекции зрения по методу Шичко-Бейтса. Это курс общего оздоровления и избавления от вредных
Из книги автораЛекция 3 Здравствуйте, уважаемые соратники, начинаем наше третье занятие в Народном университете здорового образа жизни по методу Геннадия Андреевича Шичко. Курс посвящен коррекции зрения по методу Шичко-Бейтса. Это курс общего оздоровления и избавления от вредных