Nel corpo umano è sintetizzato in quantità insufficiente per garantire una vita normale, pertanto deve essere fornito con il cibo. Per i bambini questo amminoacido è indispensabile.
L'aminoacido istidina fa parte delle proteine, pertanto è detto proteogenico. È necessario per la crescita e lo sviluppo di tutti gli organi e tessuti, svolge un ruolo importante nella sintesi dell'emoglobina, un trasportatore di ossigeno nel sangue, fa parte del centro attivo di molti enzimi ed è un precursore di importanti composti: l'istamina , carnosina, anserina.
L'istidina è un amminoacido eterociclico diamminomonocarbossilico.
La molecola dell'istidina ha una coda di acido carbossilico e due teste amminiche, una delle quali è inclusa nel composto ciclico. Avendo due teste amminiche, l'amminoacido ha proprietà basiche, cioè V soluzione acquosa sposta il pH (pH) sul lato alcalino (> 7). L'amminoacido ha proprietà altamente idrofile, cioè si scioglie bene in acqua. Nelle proteine globulari si trova principalmente sulla superficie.
L'istidina è chiamata supercatalizzatore per la sua importanza nella catalisi enzimatica, perché è il sito attivo di molti enzimi.
bisogno biologico.
Il fabbisogno giornaliero di istidina è di 1,5-2 g per un adulto, per neonati: 34mg/kg. peso, cioè 0,1 - 0,2 g.
Biosintesi dell'istidina
La biosintesi dell'istidina è molto complessa, è una cascata di 9 reazioni, non sorprende che il corpo preferisca ottenere l'amminoacido nella sua forma finita. I composti iniziali per la sintesi dell’istamina sono: acido adenosina trifosforico (ATP) E 5-fosforibosil-1-pirofosfato (FRPP).
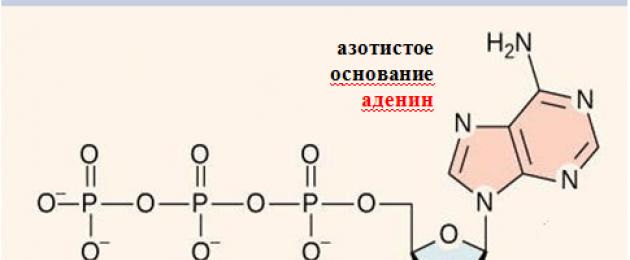
L’ATP è il carburante su cui lavora il corpo, il composto che fornisce energia. Lei ha struttura complessa ed è costituito da una base purinica di adenina, uno zucchero ribosio a cinque membri e tre code: residui di acido fosforico.

Il 5-fosforibosil-1 pirofosfato (FRPP) è un composto formato da ribosio-5-fosfato, uno zucchero ribosio a cinque membri con una coda di acido fosforico attaccata. Il ribosio-5-fosfato si forma come prodotto finale ciclo pentoso-fosfato, una cascata di reazioni per la conversione del glucosio - zucchero ordinario.

Il ribosio-5-fosfato attacca a sé due code di fosforo della molecola di ATP e si trasforma in 5-fosforibosil-1-pirofosfato (FRPP), necessario per la sintesi dell'istidina. Pertanto, i prodotti iniziali della sintesi sono: glucosio zuccherino e 2 molecole di ATP.
La sintesi della molecola dell'istidina è iniziata. Il trasportatore è attivo e funzionante. Una molecola di ATP è attaccata alla molecola di 5-fosforibosil-1-pirofosfato (FRPP).

Allo stesso tempo, la coda del pirofosfato viene staccata dalla molecola FRPP e il nucleo purinico della base azotata dell'ATP è attaccato al carbonio dello zucchero ribosio a cinque membri nella molecola FRPP.
Nella seconda fase, altri due residui di fosforo vengono separati dal mostro formato, che, in seguito stato iniziale apparteneva all'ATP.
Si forma il composto fosforibosilAMP.

Terza fase. Idrolisi, cioè l'attaccamento dell'acqua al nucleo purinico, che originariamente appartiene alla molecola di ATP. L'anello di carbonio si rompe, l'ossigeno dell'acqua si unisce al carbonio e una coppia di idrogeni va agli azoti vicini, ciascuno con un idrogeno, in modo che nessuno si offenda.

Quarta fase. L'anello dello zucchero ribosio a cinque membri si apre, l'anello del ribosio si apre e una molecola d'acqua viene scissa.

Nella quinta fase avviene la metamorfosi. Entra in reazione glutammina, che dà il residuo azotato e prende il residuo idrossilico - OH, trasformandosi in acido glutammico (glutammato).

L'acido glutammico e la glutammina sono due composti che scambiano costantemente teste di azoto. L'ammoniaca che si forma durante il lavoro viene catturata dall'acido glutammico, che viene convertito in glutammina, la forma di trasporto del trasferimento dei gruppi azoto. La glutammina è utilizzata in una varietà di reazioni di sintesi, quindi è stata utile per la formazione dell'anello imidazolico dell'istidina.
La reazione di scambio della testa azotata della glutammina con l'acido glutammico si presenta così:

Il composto che va alla sintesi dell'istidina viene riorganizzato, la corona viene separata da esso - il ribonucleotide - 5-aminoimidazolo-4-carbossammide - un prodotto intermedio della sintesi dell'ATP. Andrà alla sintesi dell'ATP.

L'altro prodotto di scissione contiene cinque atomi di carbonio dallo scheletro originale dello zucchero ribosio, un atomo di carbonio e uno di azoto separati dalla molecola di ATP originariamente reagita e un atomo di azoto introdotto dalla glutammina. Allo stesso tempo, l'anello imidazolico si chiude.
Il risultato è un bianco per l'istidina.
Nella sesta fase viene scissa un'altra molecola d'acqua
Passaggio 7: la molecola di acido glutammico dona la sua testa amminica per diventare α-chetoglutarato. La testa amminica dell'acido glutammico (glutammato) viene aggiunta alla preforma di istidina.
Il composto perde la coda di fosforo, trasformandosi in alcol
SU fase finale l'alcol risultante viene ossidato dalla molecola NAD e l'alcol viene convertito in un amminoacido.

L'intero ciclo di trasformazione è simile al seguente:

Sostanze - precursori per la sintesi dell'istidina sono:
- Glucosio, che viene convertito in fosforibosil pirofosfato (PRPP) nel ciclo del pentoso fosfato. Lo scheletro carbonioso dello zucchero diventerà lo scheletro carbonioso di un amminoacido
- Due molecole di ATP, una dona una coda di fosforo per la sintesi di FRPP, l'altra dona una base purinica per la sintesi dell'anello istidina imidazolico
- Acido glutammico, che viene consumato in modo molto economico: inizialmente la molecola di acido glutammico cattura l'ammoniaca, trasformandosi in glutammina, necessaria per la sintesi dell'istidina. Durante la reazione, la glutammina dona un gruppo azoto, trasformandosi nuovamente in acido glutammico, che può essere utilizzato per la deaminazione per donare un gruppo azoto allo stock di istidina.
- Due molecole di NAD per ossidare l'alcol in un amminoacido.
Un altro schema della stessa cascata di reazioni:

Gli enzimi sono coinvolti in tutte le fasi della sintesi:
- ATP-fosforibosil transferasi
- Pirofosfoidrolasi
- Fosforibosil AMP cicloidrolasi
- Fosforibosil forimino-5-amminoimidazolo-4-carbossammide ribonucleotide isomerasi
- Glutammina amido transferasi
- Imidazologlicerolo - 3 - fosfato deidratasi
- Istidinolo fosfato aminotransferasi
- Istidinolo fosfato fosfatasi
- Istidinolo deidrogenasi
L'aminoacido istidina è semiessenziale negli adulti e assolutamente indispensabile nei bambini, perché svolge numerose funzioni nell'organismo. funzioni importanti.
bisogno biologico
Il fabbisogno giornaliero minimo di istidina per un adulto è di 12 mg / 1 kg. peso corporeo, ad es. per una persona di 60 kg. Sono necessari 0,7 g al giorno. Il fabbisogno giornaliero ottimale per un adulto è di 1,5 - 2 g. La dose massima consentita di istidina è di 5-6 g / giorno.
Per i neonati, il fabbisogno di istidina è di 34 mg/kg. peso, cioè 0,1 - 0,2 g.
La necessità di istidina aumenta con uno sforzo fisico intenso, durante il periodo di recupero dopo gravi infortuni, ferite e operazioni.
Il contenuto di istidina negli alimenti
Nello spezzatino l'istidina è del 15-20% in più rispetto alla carne fritta e del 35-40% in più rispetto alla carne cruda.
Il pesce cotto contiene il 25-30% in più di istidina rispetto al pesce crudo.
Proteina prodotti erboristici in media, viene digerito del 20% peggio di quello di origine animale e la proteina dei finferli viene digerita solo del 30%, in relazione alla quale sono stati introdotti coefficienti aggiuntivi.
Per migliore conservazione aminoacidi presenti nei cereali e nella frutta secca, devono essere conservati in contenitori ermeticamente chiusi, protetti dalla luce diretta i raggi del sole.
Cereali e legumi vengono consumati non in forma secca, ma sotto forma di cereali, solitamente il rapporto tra grano e acqua in piatto prontoè 1:1 per i legumi e 1:2 per i cereali.
Con una dieta normale Abbastanza l'istidina può essere ottenuta da piccole porzioni di carne e pesce: circa 150 g di un piatto di pesce o di carne già pronto contengono il fabbisogno giornaliero di un amminoacido. Avrai bisogno di 200-300 grammi di formaggio o ricotta, questa è una porzione sana per il consumo quotidiano. Semi e noci avranno bisogno di 300-400 grammi, quindi i vegetariani completi dovrebbero pensare: o una carenza di aminoacidi o un grave eccesso di calorie, perché questi prodotti sono molto ricchi di calorie. I cereali non possono essere considerati la principale fonte di istidina, poiché 1,5 - 2 kg. il porridge può essere mangiato solo da Gargantua o da una persona seria attività fisica. Così mangiavano i contadini nel Medioevo: una grande quantità di cereali ad alto contenuto calorico veniva compensata dal duro lavoro della terra.
Carenza di istidina
IN condizioni normali A alimentazione normale Non si osserva carenza di istidina negli adulti. La carenza di istidina è possibile con diete estreme o fame, quando le persone sono costrette o rifiutano volontariamente di consumare cibi proteici. Si manifesta una carenza di aminoacidi dolore muscolare, debolezze. IN midollo osseo smettono di produrre globuli rossi (eritrociti), il che porta all’anemia, ma aumenta la coagulazione del sangue, con il rischio di coaguli di sangue. Con una carenza di istidina, il deficit uditivo è associato alla carne fino a scomparire completamente. Il desiderio sessuale è drasticamente ridotto, gli uomini possono svilupparsi disfunzione erettile.
si sviluppa la cataratta. Potenziali problemi di stomaco e duodeno. L'immunità è ridotta, il che porta a batteri e infezione virale, aumenta la tendenza alle allergie, i bambini sviluppano la dermatite eczematosa: infiammazione della pelle con prurito, lacrimazione, formazione di croste.
Bambini privati latte materno e con un'alimentazione inadeguata, restano indietro nella crescita e nello sviluppo, fino a ritardo mentale.
Eccesso di istidina
A dieta normale l'istidina non si accumula nel corpo e non si osservano sintomi di eccesso. Tuttavia, con l'uso di preparazioni farmacologiche di L-istidina, reazioni avverse,
L'istidina rimuove il rame e lo zinco dal corpo, un eccesso di istidina provoca reazioni allergiche e attacchi di asma bronchiale, negli uomini può portare a eiaculazione precoce.
Per evitare lo sviluppo di complicazioni, i preparati di istidina possono essere utilizzati solo per indicazioni cliniche Sotto controllo medico.
Controindicazioni
Preparati di istidina NON APPLICARE in presenza delle seguenti condizioni:
- malattia mentale Parole chiave: disturbo bipolare, schizofrenia, lesioni cerebrali organiche
- Malattie allergiche, asma bronchiale
- Ipotensione arteriosa(bassa pressione sanguigna)
- Sovrappeso- l'istidina favorisce l'aumento di peso
- Gravidanza, allattamento
- malattie croniche fegato e reni
Effetti collaterali
Con un sovradosaggio di preparati farmacologici di L-istidina, è possibile quanto segue: effetti collaterali:
- reazioni allergiche tipo immediato: Edema di Quincke, forte calo pressione sanguigna con perdita di coscienza (collasso arterioso), shock anafilattico.
- Disordini mentali
Effetti collaterali meno gravi in cui è necessario ridurre il dosaggio del farmaco:
- Dal lato tratto gastrointestinale: nausea, vomito, dispepsia (disturbi della digestione nello stomaco)
- Dal lato del sistema nervoso centrale e periferico: mal di testa, vertigini, tremore (tremori degli arti), disturbi della coscienza, parestesie (sensazioni di "strisciare", "spilli e aghi")
- Dal sistema nervoso autonomo: incremento locale temperatura (ipertermia locale), febbre, bassa pressione sanguigna, broncospasmo
- Reazioni allergiche: eruzione cutanea.
Conclusione
L'istidina è importante amminoacido richiesto, il cui bisogno è soddisfatto con la normale alimentazione. Una dieta variata che includa carne, pesce e latticini fornirà la quantità necessaria e sufficiente di istidina vita piena. Preparazioni farmacologiche e gli integratori alimentari di L-istidina possono essere usati per trattare condizioni sotto controllo medico, ma non per salute generale persone normali a causa dei rischi complicazioni pericolose e molti effetti collaterali.
introduzione
| Nome banale | Istidina / Istidina |
| Codice di tre lettere | Il suo |
| Codice a lettera singola | H |
| Nome IUPAC | Acido L-α-ammino-β-imidazolilpropionico |
| Formula strutturale | |
| Formula lorda | C₆H₉N₃O₂ |
| Massa molare | 155,16 g/mol |
| Caratteristiche chimiche | idrofilo, protonabile, aromatico |
| PubChem CID | 6274 |
| Sostituibilità | Insostituibile |
| codificato | CAU e CAC |
 |
L'istidina è un alfa-amminoacido con un gruppo funzionale imidazolico. Fu scoperta l'istidina Dottore tedesco Kossel Albrecht nel 1896. Inizialmente si pensava che questo aminoacido fosse essenziale solo per i neonati, ma studi a lungo termine hanno dimostrato che è importante anche per gli adulti. Per una persona, il fabbisogno giornaliero di istidina è di 12 mg per kg di peso corporeo.
Insieme alla lisina e all'arginina forma un gruppo di aminoacidi basici. Incluso in molti enzimi, è un precursore nella biosintesi dell'istamina. Si trova in grandi quantità nell'emoglobina.
L'anello imidazolico dell'istidina è aromatico a tutti i valori di pH. Contiene sei elettroni pi greco: quattro provenienti da due doppi legami e due da una coppia di azoto. Può formare legami pi greco, ma ciò è complicato dalla sua carica positiva. A 280 nm non è in grado di assorbire, ma nella gamma UV inferiore assorbe anche più di alcuni amminoacidi.
L'istidina è ricca di alimenti come tonno, salmone, filetto di maiale, filetto di manzo, petto di pollo, soia, arachidi, lenticchie, formaggio, riso, grano.
È stato dimostrato che l'integrazione di istidina causa un rapido rilascio di zinco nei ratti con un aumento da 3 a 6 volte del tasso di escrezione.
Biochimica
 |
Il precursore dell'istidina, come il triptofano, è il fosforibosil pirofosfato. Il percorso della sintesi dell'istidina si interseca con la sintesi delle purine.
La catena laterale imidazolica dell'istidina è un ligando di coordinamento comune nelle metalloproteine e fa parte dei siti catalitici in alcuni enzimi. Nelle triadi catalitiche, l'azoto basico dell'istidina viene utilizzato per generare un protone da serina, treonina o cisteina e attivarlo come nucleofilo. L'istidina viene utilizzata per trasferire rapidamente protoni estraendo il protone con il suo azoto basico e creando intermedi caricati positivamente, quindi utilizzando un'altra molecola, un tampone, per estrarre il protone da acido nitrico. Nell'anidrasi carbonica, il trasferimento di protoni dell'istidina viene utilizzato per trasportare rapidamente i protoni da una molecola d'acqua legata allo zinco per rigenerare rapidamente le forme attive dell'enzima. L'istidina è presente anche nelle eliche dell'emoglobina E ed F. L'istidina aiuta a stabilizzare l'ossiemoglobina e a destabilizzare l'emoglobina legata al CO. Di conseguenza, il legame del monossido di carbonio è solo 200 volte più forte nell’emoglobina, rispetto a 20.000 volte nell’eme libero.
Alcuni aminoacidi possono essere convertiti in intermedi nel ciclo di Krebs. I carboni di quattro gruppi di amminoacidi formano intermedi del ciclo: alfa-chetoglutarato (alfa-CT), succinil-CoA, fumarato e ossalacetato. Gli aminoacidi che formano l'alfa-KG sono glutammato, glutammina, prolina, arginina e istidina. L'istidina viene convertita in formiminoglutammato (FIGLU).
L'amminoacido è un precursore della biosintesi dell'istamina e della carnosina.
 |
L'istidina fa parte di centri attivi molti enzimi, è un precursore nella biosintesi dell'istamina (vedi Fig. 2). L'enzima istidina ammoniaca liasi converte l'istidina in ammoniaca e acido urocanico. Questo enzima è carente nel raro disturbo metabolico istidinemia. Negli antinobatteri e nei funghi filamentosi come la Neurospora crassa, l'istidina può essere convertita nell'antiossidante ergotioneina.
Funzioni principali:
sintesi proteica;
assorbimento raggi ultravioletti e radiazioni;
produzione del rosso e del bianco cellule del sangue;
produzione di istamina;
rilascio di epinefrina;
secrezione succo gastrico;
antiaterosclerotico,
azione ipolipemizzante;
escrezione di sali metalli pesanti;
salute articolare.
Sistemi e organi:
- organi del tratto gastrointestinale;
- fegato;
- ghiandole surrenali;
- sistema muscoloscheletrico;
- sistema nervoso(guaine mieliniche delle cellule nervose).
Conseguenze della carenza:
- perdita dell'udito;
- ritardo mentale sviluppo fisico;
-fibromialgia.
Malattie:
- istidinemia.
Conseguenze dell'eccesso: L'eccesso di istidina può contribuire alla carenza di rame nel corpo.
Caratteristiche fisico-chimiche
 |
La catena laterale imidazolica dell'istidina ha un pKa di circa 6,0. Ciò significa che a valori di pH fisiologicamente appropriati, variazioni relativamente piccole del pH possono modificare la carica media della catena. Al di sotto di pH 6, l'anello imidazolico è prevalentemente protonato, come nell'equazione di Henderson-Hasselblach. Quando protonato, l'anello imidazolico ha due legami NH e una carica positiva. La carica positiva è distribuita uniformemente tra i due atomi di azoto. La Figura 3 mostra la curva di titolazione dell'istidina (file Excel con calcoli). Dalla curva di titolazione consegue che il gruppo carbossilico principale ha pK a1 = 1,82, il gruppo amminico protonato dell'amidazolo ha pK a2 = 6,00 e il gruppo amminico protonato principale ha pK a3 = 9,17. A pH = 7,58, l'istidina esiste come ione bipolare (zwitterione) quando la carica elettrica totale della molecola è 0. A questo pH, la molecola di istidina è elettricamente neutra. Questo valore di pH è chiamato punto isoelettrico e viene indicato come pI. Il punto isoelettrico viene calcolato come media aritmetica di due valori pK a adiacenti.
Per istidina: pI \u003d ½ * c (pK a2 + pK a3) \u003d ½ * (6,00 + 9,17) \u003d 7,58
.
La Figura 4 mostra forme diverse esistenza della molecola di istidina. Questo dovrebbe essere inteso come segue: a un certo pK a appare la forma corrispondente, quindi la percentuale del suo contenuto aumenta gradualmente.
Contatti proteina-proteina
Vedrai (in ordine):
1) modello ball-and-stick di istidina (prima di premere qualsiasi pulsante)
2) vista generale del legame peptidico usando l'esempio di istidina e glicina (ID PDB: 1W4S, 198 e 199) (dopo aver cliccato su "Avvia")
3) vista generale del legame idrogeno della spina dorsale utilizzando l'esempio di istidina e valina (ID PDB:1W4S, 974:A e 964:A) (dopo aver fatto clic su "Continua")
4) legame idrogeno a catena laterale (ID PDB: 5EC4, 119 e 100) (di seguito dopo i successivi clic su "Continua")
5) legame idrogeno nella catena laterale (ID PDB: 5EC4, 93 e 72)
6) legame idrogeno a catena laterale (ID PDB: 5HBS, 48 e 63)
7) legame idrogeno a catena laterale (ID PDB: 5HBS, 137 e 135)
8) legame idrogeno nella catena laterale (ID PDB: 5E9N, 219 e 284)
9) legame idrogeno nella catena laterale (ID PDB: 3X2M, 112 e 14)
10) ponte salino (ID PDB: 1us0, 240 e 284)
11) ponte salino (ID PDB: 1US0, 187 e 185)
12) possibile interazione di picchettamento (ID PDB: 5E9N, 137 e 7)
13) possibile interazione di picchettamento (ID PDB: 5E9N, 10 e 50)
L'istidina è in grado di formare non solo legami idrogeno con la partecipazione della spina dorsale, ma anche con la partecipazione della catena laterale. Inoltre, a causa della polarità della molecola, è possibile la formazione di ponti salini con aminoacidi carichi negativamente (rappresentati schematicamente in giallo). Inoltre, l'istidina aromatica può entrare in interazioni di impilamento con altri amminoacidi aromatici. L'istidina non entra in interazioni idrofobiche a causa della sua idrofilicità.
Le interazioni proteina-proteina sono alla base di molti processi fisiologici associati all'attività enzimatica e alla sua regolazione, trasporto elettronico, ecc. Il processo di formazione complessa di due molecole proteiche in soluzione può essere suddiviso in più fasi:
1) libera diffusione delle molecole in soluzione lunga distanza da altre macromolecole
2) convergenza delle macromolecole e il loro orientamento reciproco dovuto a interazioni elettrostatiche a lungo raggio con la formazione di un complesso preliminare (diffusione-collisione),
3) trasformazione del complesso preliminare in quello finale, cioè in una configurazione tale in cui viene svolta la funzione biologica.
In alternativa, il complesso diffusione-collisione può disintegrarsi senza la formazione di un complesso finale. Durante la trasformazione del complesso preliminare nel complesso finale, le molecole del solvente vengono spostate dall'interfaccia proteina-proteina e si verificano cambiamenti conformazionali nelle macromolecole stesse. Ruolo importante questo processo è giocato da interazioni idrofobiche e dalla formazione di legami idrogeno e ponti salini.
Fattori che regolano le interazioni proteina-proteina:
Contatti DNA-proteine
 |
La stabilità dei complessi nucleoproteici è fornita dall'interazione non covalente. In varie nucleoproteine, la stabilità del complesso è assicurata da Vari tipi interazioni.
Nella fig. 5 mostra l'interazione dell'istidina e gruppo fosfato spina dorsale del DNA. Questa interazione è dovuta alla carica positiva dell'istidina. Sono state trovate molte interazioni simili (tutte si formano secondo un unico principio, quindi non ha senso elencarle tutte).
Note e fonti:
Il lavoro è stato svolto insieme a Teplovaya Anastasia //
Istidina // LifeBio.wiki.
Ricerca informatica e Modellazione, 2013, V. 5 No 1 P. 47−64 // S.S. Khrushcheva, A.M. Abaturova e altri // Modellazione delle interazioni proteina-proteina utilizzando il pacchetto software di dinamica browniana multiparticellare ProKSim.
Interazioni proteina-proteina // Wikipedia.
Nucleoproteine //
Istidina? Una sana longevità è possibile solo con una corretta e alimentazione equilibrata. Affinché tutti i sistemi e gli organi funzionino correttamente, dobbiamo ricevere quotidianamente un gran numero di sostanze utili. E in questo elenco aminoacido istidina non occupa l'ultimo posto. È necessario per il flusso di un numero di processi biochimici. Sicuramente molti non sanno dell'enorme il ruolo dell'istidina nella vita del corpo. Pertanto, ti invitiamo a leggere proprietà utili questa sostanza. Descriveremo anche come ciò aminoacidi nello sport e medicina.
Istidina nella forma naturale e nel dosaggio ottimali presenti nei prodotti delle api - come ad es polline, pappa reale e covata di fuchi, che fanno parte di molti complessi vitaminici e minerali naturali di Parapharm: Leveton P, Elton P, Leveton Forte, Apitonus P, Osteomed, Osteo-Vit, Eromax", "Memo-Vit" e "Kardioton". Ecco perché prestiamo così tanta attenzione a ciascuno sostanza naturale, parlando della sua importanza e dei benefici per un corpo sano.
Amminoacido condizionatamente essenziale
istidina: per il fegato e i nervi
L'istidina è un amminoacido che mondo scientifico ci sono ancora controversie. Alcuni scienziati sostengono che non è sintetizzato nel corpo umano e quindi deve essere regolarmente fornito con il cibo. Altri, invece, citano dati di ricerca, secondo i quali, al n grandi quantità questa sostanza può essere prodotta nel corpo. Pertanto, sempre più spesso, l'istidina, insieme all'arginina, viene classificata come un gruppo speciale: « amminoacidi condizionatamente essenziali. Leggermente meno comune è il nome "amminoacido semiessenziale".
Comunque, ma piccole quantità l'istidina, che l'organismo produce autonomamente, non è sufficiente per mantenere la salute. Inoltre, nei bambini di età inferiore a un anno, la sintesi di questa sostanza non avviene affatto. Pertanto, è necessario monitorare la propria dieta, cercando di diversificare la propria dieta.
Che cosa è l'istidina
In natura, l'istidina è comune: è presente nella maggior parte degli organismi viventi. È un componente delle proteine e si trova anche in forma libera. Anche nel corpo umano questo amminoacido si trova in grandi quantità. Questa sostanza appartiene al gruppo dei proteogenici, il che significa che è necessaria per la produzione di proteine. IN forma pura l'istidina lo è polvere incolore che fonde a 287 gradi (L-isomero). Questo composto è altamente solubile in acqua, ma scarsamente in etanolo. Quando decarbossilato l'istamina viene prodotta nel corpo. Per ricevere medicinali Nome latino- istidina) viene isolata dall'emoglobina e dal sangue e anche sintetizzata. A proposito, oggi il mondo produce più di 200 tonnellate di questa sostanza all'anno.
Istidina: storia
importante scoperta scientifica
Storia di un'importante scoperta scientifica avvenne alla fine del XIX secolo, in un'epoca in cui la chimica si stava sviluppando molto attivamente in Europa. Il noto fisiologo e biochimico tedesco A. Kossel nel 1896 isolò la sturina dagli idrolizzati solfati. Nello stesso anno, il chimico svizzero S. Hedin riuscì a ottenere l da altre proteine, e lavorò indipendentemente dal suo collega. Anche un grande contributo allo studio data sostanza introdotto da W. Pauli.
A. Kossel è noto per aver creato metodo classico isolamento quantitativo di "basi esoni", a cui, oltre a includere tale aminoacidi come l'arginina e la lisina. Grazie ai suoi risultati, gli scienziati hanno successivamente scoperto che le proteine sono di natura polipeptidica. Questo biochimico ha anche condotto ricerche biologia cellulare, studiato Composizione chimica nucleo cellulare, era impegnato nell'isolamento e nella descrizione acidi nucleici. Per il suo lavoro è stato premiato premio Nobel in Fisiologia o Medicina 10 dicembre 1910.
Senso istidina per il corpo.
"Il mattone del corpo"
Nonostante questa sostanza sia poco conosciuta da una vasta gamma di persone, l'importanza dell'istidina per l'organismo Grande. Non sarebbe esagerato chiamare questo amminoacido "mattone del corpo". Innanzitutto, è coinvolto nella sintesi proteica e, quindi, aiuta a costruire i muscoli. In secondo luogo, l'istidina fa parte di molti enzimi, come la gastrina, che è coinvolta nel sistema digestivo, migliorando l'assorbimento di numerose vitamine.
Anche questa connessione migliora bilancio dell'azoto nel corpo, aiuta il corretto funzionamento del fegato. un ruolo significativo gioca nel lavoro del sistema immunitario - con la sua partecipazione si verifica la formazione di leucociti ed eritrociti. Inoltre, si trova in grandi quantità nell'emoglobina. Inoltre, l'istidina è un componente per la produzione di una sostanza così importante come la L-carnosina.
Di più istidina corporea necessario Per sintesi istamina, un ormone unico che è coinvolto in 23 major funzioni fisiologiche. Ad esempio, la salute sessuale sia degli uomini che delle donne dipende dal suo contenuto nel sangue. Un altro grande merito dell'istamina è la lotta contro l'istamina infezioni varie. IN l'anno scorso gli scienziati notano che molte persone hanno un aumento del contenuto di istamina nel sangue, causato da malattie come infarto, ipertensione, obesità, carie e diversi tipi allergie. Istaminaè un mediatore di reazioni allergiche, si espande piccolo vasi sanguigni, restringe quelli grandi. I mediatori dell'allergia sono sostanze che vengono rilasciate dalle cellule o create a seguito di processi biochimici nel corpo, necessarie per il corretto decorso di una reazione allergica.
Allo stesso tempo, non dimenticare gli altri proprietà utili :
- aiuta i bambini a crescere;
- partecipa alla regolazione dell'acidità del sangue;
- allevia le allergie;
- aiuta a riprendersi dopo una grave malattia;
- contribuisce alla normalizzazione del sonno;
- necessario per la formazione delle guaine mieliniche delle cellule nervose;
- importante per operazione normale del sistema cardiovascolare.
Ha anche proprietà adattogene, riducendo l'impatto sul corpo di fattori distruttivi.
Cosa succede quando mancanza di istidina?
È stato stabilito che a mancanza di istidina i bambini rallentano la crescita e lo sviluppo. Per gli adulti, questa condizione è pericolosa perché può portare a artrite reumatoide. Inoltre, con una carenza di questo amminoacido, il recupero delle aree ferite del corpo peggiora e quindi il recupero dopo le operazioni può essere ritardato. Inoltre, si manifesta un altro effetto: la condizione della pelle e delle mucose peggiora.
I medici ne sono sicuri difetto nell'organismo porta a malattie dello stomaco e cataratta. Anche sistema immunitario indebolito che è particolarmente pericoloso per i bambini. Sono stati registrati casi in cui i bambini soffrivano di dermatite a causa della mancanza di questo aminoacido nel cibo. È stato notato che con una mancanza di istidina nel corpo, le persone lamentano un esaurimento. Inoltre, la libido diminuisce, l'udito peggiora e si sviluppa la fibromialgia. Possono essere menzionati anche altri sintomi. disavanzo :
- Malattie di Alzheimer e Parkinson;
- carenza di zinco;
- disturbi del linguaggio;
- cambiamenti nell'andatura;
- ridotta attività mentale;
- irritabilità;
- distrazione;
- pubertà ritardata;
- reazioni allergiche atipiche.
La mancanza di un amminoacido nel corpo porta a un disturbo come l'istedinemia. È raro malattia genetica, a seguito del quale il corpo smette di produrre un enzima che scompone l'istidina. In questi casi diminuisce sviluppo mentale, la parola e le funzioni motorie sono disturbate.
Eccesso di aminoacidi
Effetti collaterali
È necessario dire cosa ottenere sovrabbondanza di aminoacidi difficile, perché è ben assorbito dal corpo. Ma dosi esorbitanti della sostanza possono portare a reazioni allergiche, manifestazioni asmatiche e anche a ridurre il tempo dei rapporti sessuali negli uomini. Qui sarebbe opportuno dirlo effetti collaterali che causano la droga :
- debolezza;
- mal di testa;
- disturbo della coscienza;
- dispepsia;
- nausea;
- abbassare la pressione sanguigna;
- tremore delle mani;
- eruzioni cutanee.
In caso di sovradosaggio con tale medicinale, possono verificarsi collasso, edema di Quincke e shock anafilattico. Non è consigliabile utilizzare questo aminoacido per i pazienti asma bronchiale, ipertensione arteriosa E malattie organiche Sistema nervoso centrale.
Istidina : sostanza nello sport
È stato dimostrato che l'istidina partecipa alla sintesi delle proteine. Pertanto, i muscoli crescono e diventano forti, il che è importante per gli atleti. Provoca anche un aumento della secrezione somatotropina, che stimola la crescita della cartilagine, delle ossa e dei muscoli.
Anche istidina come sostanza nello sportÈ apprezzato perché da esso viene sintetizzata la L-carnosina nel corpo. Come sapete, è un forte antiossidante che si trova nel cervello e nei muscoli. Aumenta la resistenza prevenendo l'accumulo di prodotti di decomposizione. In particolare neutralizza l'acido che si produce durante un'intensa tensione muscolare.
Oltretutto inseriti in vari sport supplementi nutrizionali , che vengono utilizzati per la crescita muscolare e il recupero dagli infortuni. Si è rivelato particolarmente efficace in ammissione congiunta con beta-alanina, quindi l'azione reciproca degli aminoacidi è potenziata. Se usi in questo modo potrai migliorare i risultati, sia negli sport di forza che nell'atletica.
Questa sostanza fa parte di complesso vitaminico Leveton Forte. Questo farmaco è a base di erbe e prodotti delle api, aiuta ad aumentare la resistenza e le prestazioni.
Istidina in medicina:
grandi prospettive
Per le sue numerose proprietà istidina in medicina oggi è onnipresente. Poiché fa parte di molti enzimi, ha un effetto benefico sul fegato. Anche considerato un buon rimedio per il trattamento dell'epatite, aiuta con l'artrite, l'orticaria. Ecco perché questa sostanza è un componente di molti farmaci. In particolare, come rimedio viene prescritta l'istidina cloridrato ulcera peptica stomaco ed epatite. Spesso l'amminoacido viene utilizzato come uno dei componenti trattamento complesso aterosclerosi.
Nel 1976, gli scienziati sovietici V.S. Yakushev e R. I. Livshits hanno condotto una serie di esperimenti sugli animali, durante i quali hanno scoperto che limita la formazione di malondialdeide nei tessuti durante l'infarto miocardico sperimentale. Tutto ciò lo rende promettente per il trattamento delle malattie cardiovascolari.
Vale la pena dire che le prospettive per istidina in medicina molto significativo. In uno degli studi recenti, gli scienziati hanno scoperto che l'istidina va bene con. I medici sono sicuri che una tale combinazione sia un'ottima medicina contro la SARS e altre malattie. raffreddori. Dopo una serie di esperimenti, si è scoperto che i pazienti che lo assumevano istidina con zinco recuperato molto più velocemente. Vale la pena notare che questo oligoelemento migliora l'assorbimento degli aminoacidi. A sua volta, l'istidina trasporta lo zinco nelle cellule, aumentandone le prestazioni.
Inoltre, la sostanza viene utilizzata per l'esposizione alle radiazioni e per la rimozione dei metalli pesanti, è utilizzata come trattamento per l'AIDS. Inoltre, l'istidina si è rivelata una cura per le malattie renali.
Quali prodotti
contiene istidina
Perché , abbiamo bisogno di riceverlo costantemente. Non è difficile reintegrare le scorte di questo aminoacido nell'organismo, ma non tutti lo sanno quali alimenti contengono istidina . Chiamiamo le fonti di aminoacidi negli alimenti di origine animale:
- manzo;
- pollo;
- pesce (salmone, sgombro, ippoglosso);
- latticini (yogurt, panna acida);
Contengono in quantità significative questa sostanza e molti prodotti vegetali:
- arachidi;
- Lenticchie;
- semi di soia;
- segale;
- grano;
- grano saraceno;
- cavolfiore;
- Patata;
- funghi;
- banane;
- melone.
Tariffa giornaliera
aminoacidi
Per sapere quanto cibo mangiamo, devi conoscere tariffa giornaliera aminoacidi istidina. Quindi, una persona ha bisogno di 1,5-2 grammi di questa sostanza al giorno. Per compilazione corretta dieta, è possibile utilizzare la seguente formula: 10 mg di aminoacidi per chilogrammo di peso. Gli atleti che sperimentano uno stress significativo e necessitano di una dieta speciale possono assumere più aminoacidi. Si ritiene che la quantità di istidina consumata con il cibo non debba superare i 7-8 grammi al giorno. Allo stesso tempo, alcune fonti contengono informazioni che dose terapeutica di questo composto può arrivare fino a 20 grammi.
Riassumendo il nostro ragionamento, possiamo dire questo amminoacido condizionatamente essenziale l'istidina è molto importante per la salute. Oltre a partecipare alla formazione delle proteine, lo è componente importante molti enzimi. Aiuta anche il fegato a svolgere le sue funzioni, sistema immunitario e cuore. Senza esso "mattone del corpo" la nostra vita sarebbe impossibile.
- In contatto con 0
- Google Plus 0
- OK 0
- Facebook 0